Obsah:
Pod pojmem histologické vyšetření se skrývá mikroskopická analýza vzorku nádorové tkáně, který byl odebrán buď metodou punkční biopsie (core-needle, tru-cut, core-cut), či v rámci vyšetření nádoru vcelku odstraněného.
Zvláštní kategorii představuje cytologické vyšetření nádorů prsu, které umožní stanovení diagnózy velice rychle (někdy i během desítek minut), na druhou stranu má svá omezení (vzhledem k tomu, že se hodnotí pouze jednotlivé buňky a nikoli tkáň jako celek, neumožňuje posoudit chování nádoru vůči okolí, rovněž stanovení stupně diferenciace – viz níže – je limitováno). Proto je v současnosti dávána přednost vyšetření histologickému – tj. vyšetření tkáňového vzorku.
Základním významem histologického vyšetření, které je prováděno před operací z punkční biopsie je určení diagnózy – zda se jedná o nádor či nikoli, zda jde o nádor nezhoubný či zhoubný a o jaký konkrétní typ nádoru jde. To umožní naplánování odpovídajícího chirurgického zákroku.
U operačně odstraněného nádoru má histologické vyšetření poskytnout ošetřujícímu lékaři dostatek informací pro volbu nejvhodnější následné terapie.
Základní údaje, které onkolog od tohoto vyšetření očekává, jsou:
- přesná velikost nádoru,
- histologický typ nádoru (viz níže)
- stupeň diferenciace nádoru - zhodnocení, nakolik nádorová tkáň napodobuje původní mikroskopickou strukturu prsní žlázy,
- další informace o agresivitě nádoru (fakt, zda prorůstá do krevních či lymfatických cév, případně zda vrůstá do okolních tkáňových struktur, jako jsou kůže či sval),
- informace o postižení lymfatických uzlin a rozsahu tohoto postižení.
Nedílnou součástí histologického vyšetření je rovněž vyšetření imunohistochemické a v některých případech i molekulárně genetické (viz níže).
Histologické vyšetření je prováděno na ústavech či odděleních patologie, pro provádění tohoto vyšetření musí mít patolog nejvyšší možné specializační vzdělání (atestaci 2.stupně). Zvlášť obtížné případy se řeší v rámci konzultací se spádovými centry, která mají s těmito vyšetření největší zkušenost.
Výsledek standardního histologického vyšetření je obvykle k dispozici během 3-5 pracovních dní od odběru. V případech, kde je nutno mít výsledek během kratší doby je možné použití metody tzv. rychlé biopsie, kdy je vyšetřena nádorová tkáň po hlubokém zmrazení a v takovém případě je výsledek k dispozici velmi rychle (např. již během operace, což umožní chirurgovi přizpůsobit diagnóze rozsah operačního zákroku - tzv. peroperační biopsie).
V případě, kdy jsou prováděna další speciální vyšetření (např. imunohistochemie – viz níže), prodlužuje se délka vyšetření o několik dní. Ve zcela ojedinělých případech, kdy je nález nejasný a je třeba jej konzultovat na jiném pracovišti, pak může také dojít k prodloužení délky vyšetření. Obecně ale platí, že pacientka, která odchází po chirurgickém výkonu z nemocnice domů by již měla mít výsledek histologického vyšetření k dispozici.
Mikroskopická klasifikace karcinomu prsu
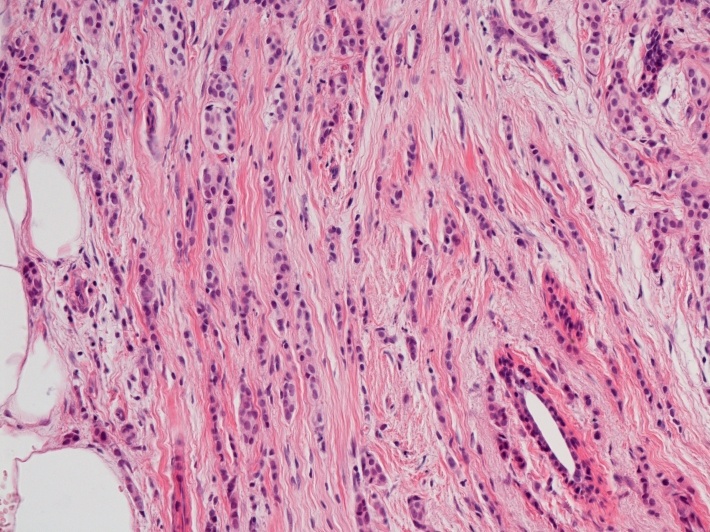 Normální prsní žláza se skládá z několika laloků, které se dále dělí do jednotlivých lalůčků. V každém lalůčku se vyskytují partie, v nichž se za normálních okolností tvoří u kojících žen mléko (tzv. aciny či lobuly) a dále větvící se strom drobných vývodů, které toto mléko odvádějí k bradavce (tzv. dukty).
Normální prsní žláza se skládá z několika laloků, které se dále dělí do jednotlivých lalůčků. V každém lalůčku se vyskytují partie, v nichž se za normálních okolností tvoří u kojících žen mléko (tzv. aciny či lobuly) a dále větvící se strom drobných vývodů, které toto mléko odvádějí k bradavce (tzv. dukty).
Podle toho, zda nádorová tkáň napodobuje spíše buňky lobulů či duktů se rozlišují dvě základní skupiny karcinomů prsu – tzv. duktální a lobulární karcinom.
Podle toho, zda nádorové buňky již získaly schopnost prorůstání z původních lobulů či vývodů do okolní tkáně (vaziva a tuku) se rozlišují nádory neinvazivní (tzv. in situ rostoucí) a nádory invazivní.
Kombinací obou výše zmíněných kritérií pak lze rozlišit čtyři základní skupiny nádorů:
- lobulární karcinom in situ,
- duktální karcinom in situ,
- duktální invazivní karcinom (asi 70-80% všech invazivních karcinomů),
- lobulární invazivní karcinom (asi 10-15% všech invazivních karcinomů).
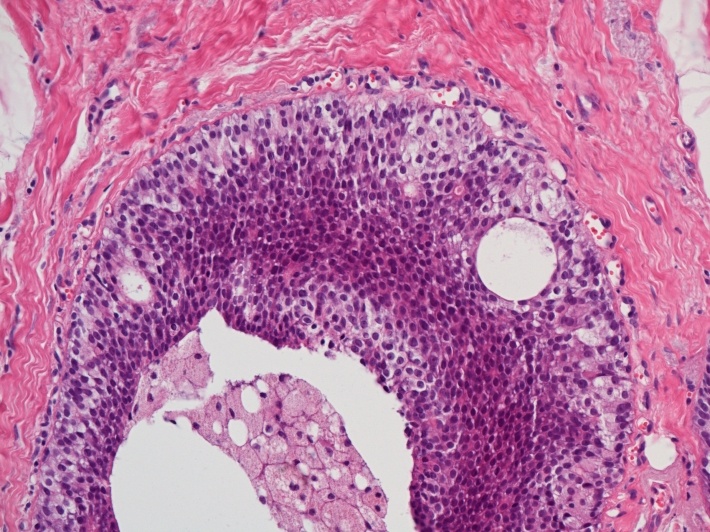 Zatímco karcinomy rostoucí in situ nemají schopnost metastazovat a jejich hlavní nebezpečí spočívá ve vzniku lokální recidivy, invazivní karcinomy již pronikly do okolní tkáně, případně získaly přístup k lymfatickým či krevním cévám a proto existuje nebezpečí jejich metastatického šíření v těle.
Zatímco karcinomy rostoucí in situ nemají schopnost metastazovat a jejich hlavní nebezpečí spočívá ve vzniku lokální recidivy, invazivní karcinomy již pronikly do okolní tkáně, případně získaly přístup k lymfatickým či krevním cévám a proto existuje nebezpečí jejich metastatického šíření v těle.
Kromě výše popsaných čtyř základních typů karcinomu prsu se vyskytuje celá řada dalších, vzácnějších podtypů, celkově představujících cca 10% všech invazivních karcinomů (medulární karcinom, mucinózní karcinom, metaplastický karcinom, světlobuněčný karcinom, apokrinní karcinom, a další).
Kromě určení histologického typu nádoru je nezbytné posouzení stupně diferenciace (tzv. grade) – zatímco dobře diferencované nádory (grade 1) rostou nejpomaleji a nejméně agresivně, málo diferencované (dediferencované) karcinomy (grade 3) rostou rychle, mají tendenci k šíření do okolí a metastazování.
Imunohistochemické vyšetření
Kromě standardního mikroskopického vyšetření, které slouží k určení velikosti a typu nádoru, k určení stupně jeho diferenciace je nezbytné zhodnotit rovněž další faktory vypovídající o povaze nádoru a jeho chování, zejména přítomnost některých bílkovin v nádorových buňkách, které hrají důležitou roli v jejich metabolismu.
Na prvním místě jde o přítomnost hormonálních receptorů , které jsou za normálních okolností přítomny v buňkách zdravé prsní žlázy. Přítomnost těchto receptorů v buňkách nádorových znamená, že tumor si doposud zachovává závislost na regulaci ženskými pohlavními hormony (estrogenem a progesteronem ), čehož lze následně využít v tzv. antihormonální terapii (Tamoxifenem, inhibitory aromatázy). V případě, že buňka tyto receptory již nevytváří, ztrácí se závislost na hormonální regulaci a tato léčba je zpravidla neúčinná.
Další důležitou molekulou je onkoprotein HER-2/neu (někdy také označovaný jako c-erbB-2), který bývá zvýšeně přítomen u asi 10 – 15 % karcinomu prsu. Jedná se o bílkovinu, která je přítomna v membráně nádorových buněk a slouží jako receptor, po jehož aktivaci dochází ke zrychlení růstu nádorových buněk, zvýšení jejich invazivity, šíření v těle a k celkovému zhoršení prognózy .
V posledních letech existuje možnost zablokování těchto receptorů pomocí monoklonálních protilátek (trastuzumab - Herceptin, pertuzumab - Perjeta), případně zablokování funkce receptorů pomocí tzv. inhibitoru tyrosinkinázy (lapatinib - Tyverb). Pro efekt výše zmíněných léků je nezbytné, aby nádorové buňky obsahovaly tento receptor, proti kterému jsou léky cíleny.
U všech karcinomů prsů je proto vyšetřována přítomnost hormonálních receptorů a HER2/neu pomocí laboratorní metody zvané imunohistochemie. U případů, které jsou imunohistochemicky HER2 silně pozitivní (jsou označovány jako 3+) či slabě pozitivní (2+) je před zahájením léčby ještě ověřována přítomnost zvýšeného počtu kopií genu (tzv. amplifikace), které tento protein kódují. Toto vyšetření se provádí rovněž na patologii, označuje se jako in situ hybridizace – FISH, CISH nebo SISH.
Zatímco nádory, které jsou imunohitochemicky silně pozitivní (3+) obsahují takřka vždy zvýšené množství kopií genu HER2/neu (tj. jsou amplifikované), u nádorů slabě pozitivních je zastoupení amplifikovaných případů výrazně nižší a pohybuje se jen mezi 20 a 30 % z 2+ pozitivních nádorů.
Údaje o expresi hormonálních receptorů a onkoproteinu HER-2/neu jsou nedílnou součástí protokolu o vyšetření karcinomu prsu. Vzhledem k tomu, že antiHER-2 léčba je finančně značně náročná a je jednoznačně prokázáno, že její efekt lze očekávat pouze u žen s HER2 pozitivním karcinomem, je pozitivita každého nádoru odhalená na menším pracovišti patologie ještě následně ověřována v jedné z osmi referenčních laboratoří, které jsou pro toto vyšetření v České republice ustanoveny (Všeobecná fakultní nemocnice v Praze, Fakultní nemocnice Motol, Fakultní nemocnice Hradec Králové, Fakultní nemocnice Olomouc, Masarykův onkologický ústav Brno, Bioptická laboratoř Plzeň, Biolab Praha, CGB laboratoř Ostrava). Pro léčbu anti-HER2 jsou vhodné pouze ty nádory, které jsou buď imunohistochemicky silně pozitivní (3+), nebo vykazují amplifikaci genu HER-2/neu. O použití této léčby však nerozhoduje patolog, ale ošetřující onkolog, který se opírá nejen o výsledky vyšetření patologem, ale i o další klinická data.
