Uvedená doporučení se týkají především systémové léčby adenokarcinomu pankreatu (PDAC), okrajově jsou zmíněny i možnosti radioterapie a léčby chirurgické. Jedinou potenciálně kurativní léčebnou metodou je radikální chirurgická resekce tumoru, která by měla být prováděna pouze ve vybraných centrech specializovaných na operativu nádorů pankreatu. Zejména u nemetastatických pacientů je nutné posouzení resekability a strategie léčby v prostředí multidisciplinární komise.
Primární resekce je indikována u pacientů s iniciálně resekabilním onemocněním, přičemž definice resekability vychází především ze vztahu nádoru k vena portae, vena mesenterica superior, truncus coeliacus, arteria mesenterica superior a arteria hepatica communis, zohledněna by měla být i hodnota CA 19-9 a celkový stav pacienta. Mezi základní typy radikálních operačních výkonů patří u nádorů hlavy pankreatu hemipankreatoduodenektomie (HPDE nebo PDE), u nádorů těla a kaudy pankreatu levostranná/distální pankreatosplenektomie (RAMPS) a u pokročilejších nádorů pak totální pankreatektomie s lymfadenektomií a splenektomií (po které dochází ke kompletní endokrinní i exokrinní insuficienci pankreatu s rozvojem obtížně zvladatelného diabetu mellitu). Po splenektomii je vhodná následná vakcinace proti obvyklým patogenům.
U všech pacientů je doporučena vstupní genetická konzultace a vyšetření známých hereditárních syndromů včetně mutace BRCA1 a 2. Testování somatického genového profilu by mělo být zváženo v případech, kde by jejich identifikace mohla ovlivnit systémovou léčbu, zejména u pokročilého onemocnění a v případě KRAS wild type tumorů (NTRK fúze, somatické mutace BRCA1/2, MSI-H, případně další). U všech pacientů je rovněž nutné věnovat zvýšenou pozornost podpůrné léčbě, zejména zajištění drenáže žlučových cest, terapie bolesti, kompenzaci diabetu a nutriční podpoře.
7.1 Resekabilní a hraničně resekabilní karcinom pankreatu
Stadium 0, IA, IB, IIA, IIB
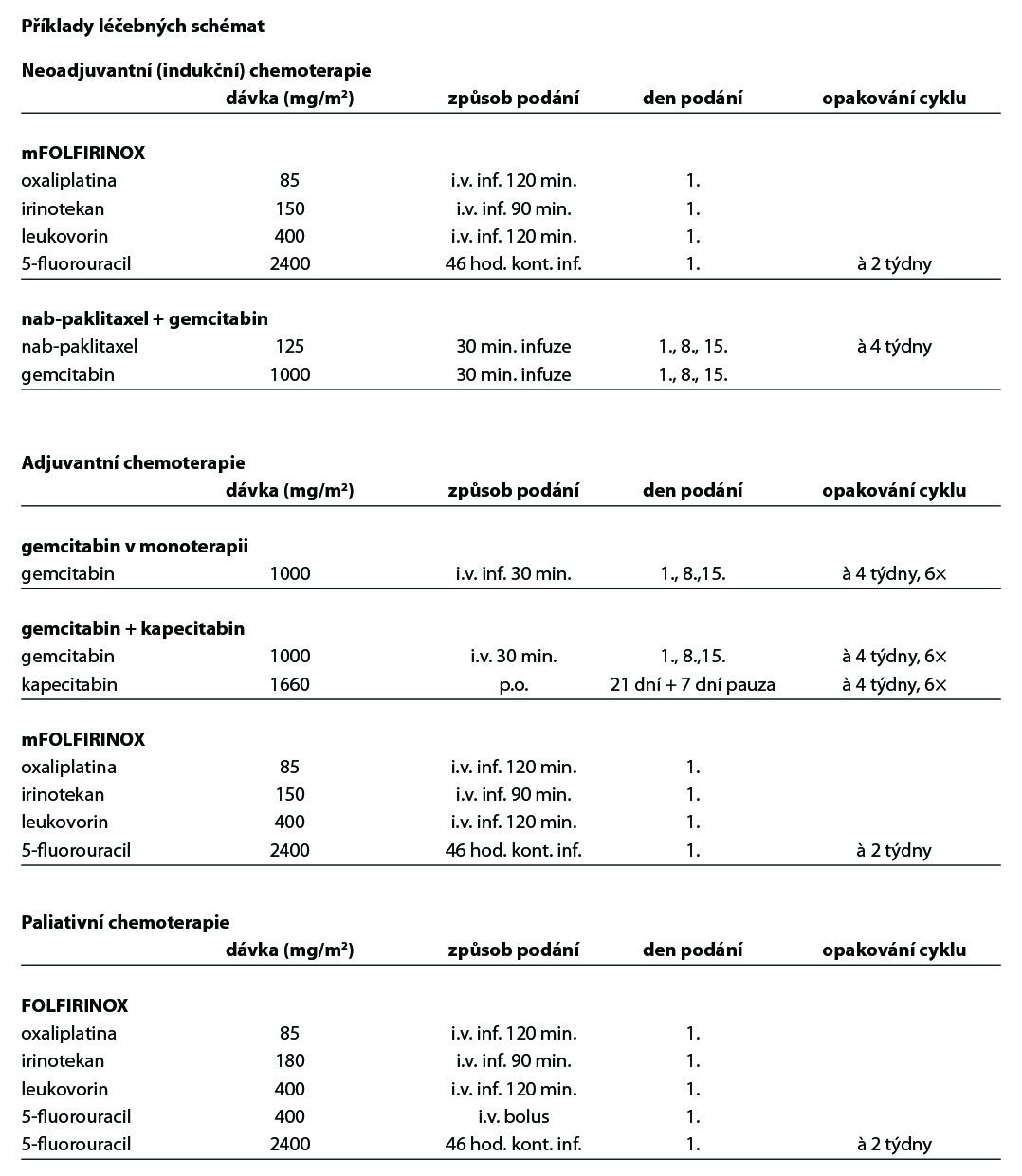
- Po radikální operaci je doporučena adjuvantní chemoterapie (CHT) po dobu 6 měsíců. U pacientů v dobrém celkovém stavu (PS 0-1) je režimem první volby mFOLFIRINOX (dle výsledků studie PRODIGE 24/CCTG PA.6), který oproti gemcitabinu prokázal výrazné prodloužení mediánu celkového přežití (medián OS 54,4 vs 34,8 měsíců) a přežití bez známek onemocnění (medián DFS 21,6 vs 12,8 měsíců). U pacientů v horším celkovém stavu nebo ve věku nad 75 let zůstává standardem gemcitabin v monoterapii, případně režim gemcitabin + kapecitabin.
- Podle metaanalýzy adjuvantní chemoradioterapie (CHRT) nezlepšovala dobu do relapsu ani celkové přežití ve srovnání se samotným operačním zákrokem a její místo v adjuvantní léčbě není v současnosti jasné. Pooperační CHRT je možné indikovat u R1 resekcí.
- U hraničně resekabilních pacientů je doporučeno podání indukční CHT případně CHRT jako alternativy primární operace. Používají se režimy mFOLFIRINOX nebo gemcitabin + nab-paklitaxel jako u metastatického onemocnění.
Pozn.: nab-paklitaxel má úhradu pouze u metastatického PDAC
7.2 Lokálně pokročilý (neresekabilní) karcinom pankreatu
Stadium III
- Doporučována je paliativní CHT režimy mFOLFIRINOX nebo gemcitabin + nab-paklitaxel jako u metastatického onemocnění
(2A). - Studie porovnávající CHRT se samotnou CHT přináší rozporuplné výsledky.
- Ke zvážení je podání CHRT případně stereotaktické radioterapie u vybraných pacientů bez progrese po minimálně 3měsíční éčbě iniciální CHT.
Pozn.: nab-paklitaxel má úhradu pouze u metastatického PDAC
7.3 Metastatický karcinom pankreatu
Stadium IV
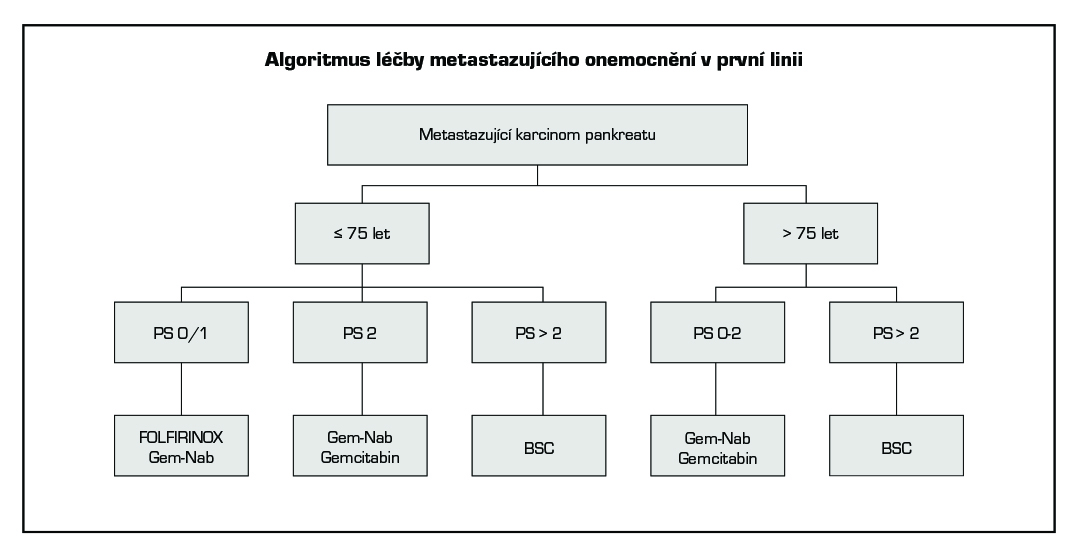
Paliativní systémová léčba je doporučena u pacientů s výkonnostním stavem PS 0-2 (viz algoritmus).
- U nemocných PS 0-2 je vhodné zahájení paliativní CHT bezprostředně po potvrzení diagnózy, CHT není možné zahájit bez histologické, ev. cytologické verifikace. Nicméně v případě, kdy se bioptická verifikace karcinomu 2× po sobě nezdaří, ale klinický nález, nález na CT a hladina nádorového markeru CA 19-9 odpovídají diagnóze PDAC, není dle recentních ESMO guidelines další biopsie indikována a je možné začít s onkologickou léčbou.
- Je doloženo prodloužení mediánu OS a QOL u nemocných PS 0-2.
- FOLFIRINOX je terapií volby u pacientů v dobrém celkovém stavu (PS 0-1), mladších 75 let, s normální hodnotou bilirubinu a bez limitujících komorbidit (1). V klinické studii režim FOLFIRINOX signifikantně prodlužuje přežití pacientů oproti gemcitabinu v monoterapii. Medián OS: 11,1 vs 6,8 měs. HR: 0,57 (95% CI: 0,45-0,73; P <0,001.
- Gemcitabin + nab-paklitaxel (paklitaxel vázaný na albumin) je terapií volby u pacientů v dobrém celkovém stavu (PS 0–2). Kombinace signifikantně prodlužuje přežití oproti gemcitabinu v monoterapii (1). Medián OS: 8,5 vs 6,7 měs. HR: 0,72 (95% CI: 0,62-0,78; P < 0,001. Do klinické studie byli zařazováni pacienti bez věkového omezení.
- Gemcitabin v monoterapii se doporučuje u pacientů v horším celkovém stavu a/nebo s limitujícími komorbiditami (1).
- Gemcitabin + cisplatina je terapeutickou alternativou pro vybrané pacienty s patogenními mutacemi v genech homologní rekombinace – především BRCA 1 a 2 (2B).
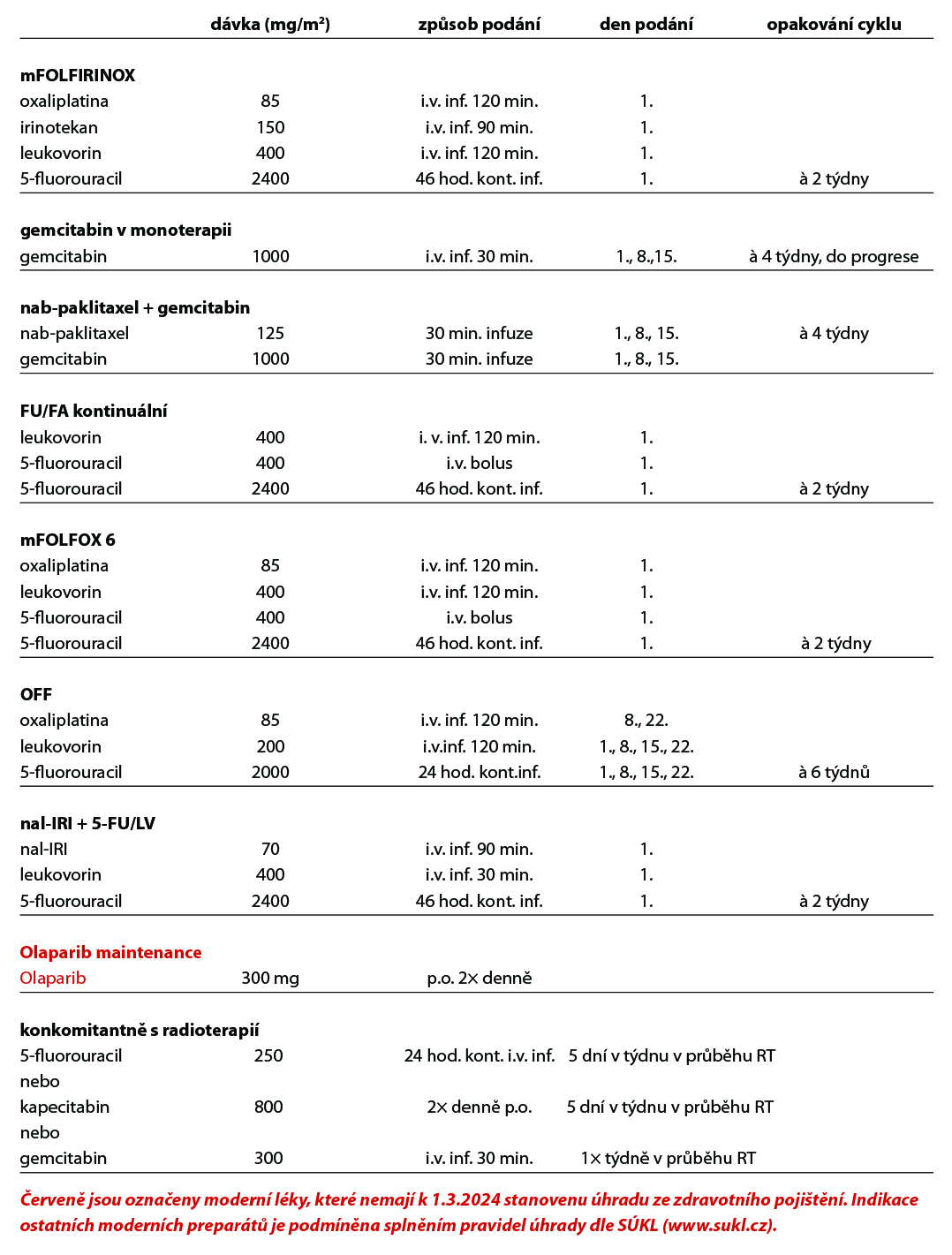
- Maintenance terapie Olaparibem je indikována u pacientů v dobrém celkovém stavu (PS 0-1) s prokázanou germinální mutací BRCA1/2 při absenci progrese po minimálně 16 týdnech iniciální chemoterapie s platinovým derivátem (např. FOLFIRINOX). Olaparib oproti placebu signifikantně prodloužil medián PFS (7,4 vs 3,8 měs., HR 0,53, p = 0,004).
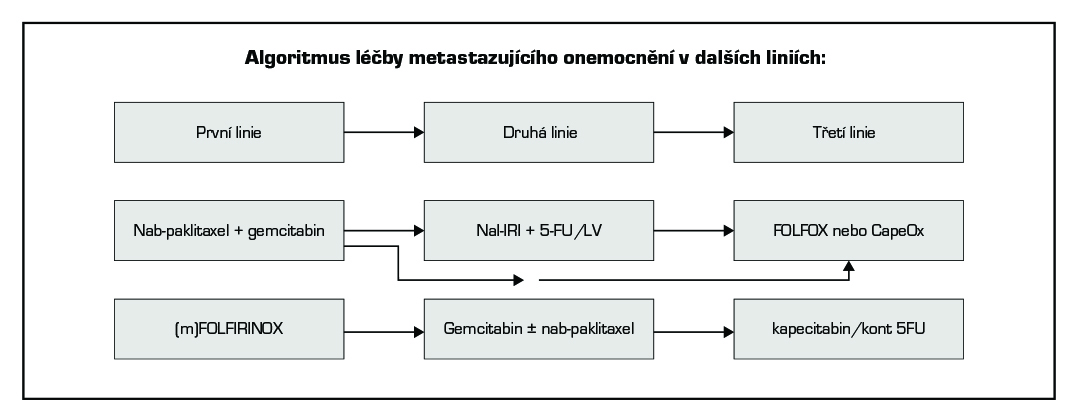
- Nali-IRI (pegylovaný lipozomální irinotekan) v kombinaci s 5-FU a leukovorinem prokázal benefit v přežití oproti chemoterapii 5-FU/leukovorin samotné a je indikován ve druhé linii léčby při progresi po terapii založené na gemcitabinu. Medián OS: 6,1 vs 4,2 měs., HR 0,67 (95% CI: 0,49-0,92; p=0,012).
- Ve druhé linii léčby lze použít režim s kontinuálním 5-fluorouracilem (případně v kombinaci s oxaliplatinou) u pacientů, kteří byli v první linii léčeni režimem s gemcitabinem a gemcitabin v monoterapii či v kombinaci u nemocných léčených v první linii režimem s 5-fluorouracilem.
Poznámky:
Vzhledem k stále omezeným terapeutickým možnostem léčby metastazujícího onemocnění je doporučeno:
- při detekci MSI-H zvážit léčbu inhibitory PD-1,
- při detekci mutací BRCA1/2 (případně dalších DDR genů – např. PALB2) zahájit léčbu chemoterapií na bázi platiny a následně zvážit udržovací terapii PARP inhibitory (olaparibem),
- při detekci NTRK fůze zvážit léčbu NTRK inhibitory (entrectinib / larotrectinib).
- při detekci BRAF mutace zvážit léčbu BRAF/MEK inhibitory
- při detekci KRAS G12C mutace zvážit léčbu KRAS G12C inhibitory (sotorasib)
Vyšetřovací algoritmus při aktivní léčbě metastazujícího onemocnění (mimo klinické studie):
• Hodnocení efektu léčby za 2–3 měsíce od inicializace systémové léčby.
• Kontrastní multifázová MDCT je preferovanou zobrazovací modalitou.
• CA 19-9 je jediný sérový marker pro hodnocení léčebné odpovědi.
Doporučení pro dispenzarizaci u pacientů po radikální resekci :
• klinické vyšetření + CA 19–9 první 2–3 roky à 3–6 měsíců, následně minimálně 1× ročně
• CT vyšetření na zvážení při symptomech a elevaci CA 19-9
Literatura:
- Conrory T, Pfeiffer P, Vilgrain V et al. Pancreatic cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2023
Nov;34(11):987-1002 - Tempero MA et al. NCCN Guidelines Version 1.2024 Pancreatic Adenocarcinoma, dostupné z: https://www.nccn.org/professionals/physician_gls/pdf/pancreatic.
pdf





