Léčba zářením – radioterapie, lépe však náplň oboru vystihuje název radiační onkologie, je klinickým oborem, který v posledních 5-8 letech prošel v naší republice významnou přístrojovou obměnou. V každém komplexním onkologickém centru je k dispozici moderní ozařovací technika a základním zdrojem jsou lineární urychlovače s fotonovým a elektronovým zářením. V následujícím textu vysvětlujeme nové možnosti moderních lineárních urychlovačů.
Radioterapie řízená obrazem (IGRT; image guided radiotherapy)
Tato speciální technika ozařování využívá zobrazovacích metod v ozařovně před nebo v průběhu ozařování. Pro správné ozáření je totiž důležité, aby pacient na ozařovacím stole ležel pokaždé v naprosto stejné poloze jako při plánování ozařování. Odchylky polohy v průběhu ozáření mohou vznikat např. změnou polohy i malým pohybem, náplní orgánů (močový měchýř, konečník), dýcháním. Velmi zjednodušeně IGRT zajišťuje přesné zaměření svazků na ozařovači. Během ozáření je kontrolována poloha pacienta pravidelným snímkováním, zda nedochází k významným odchylkám.
Používají se Rtg snímky, které jsou provedeny přímo lineárním urychlovačem, elektronicky uloženy do systému a následně porovnány s digitální rekonstrukcí snímků z CT vyšetření při plánování radioterapie. U novějších přístrojů vybavených přídavným Rtg zdrojem je možné provedení CT vyšetření pacienta přímo pod ozařovacím přístrojem (cone beam CT) – toto ozařovací přístroje s jinými svazky záření nedokážou. Vždy je hodnocena jak jednotlivá velikost odchylky nastavení, tak i systematická chyba. V případě potřeby je provedena korekce srovnávacích značek umístěných na pacientovi, resp. na fixační masce.
Radioterapie s modulovanou intenzitou (IMRT; intensity modulated radiotherapy)
IMRT technika radioterapie kopíruje cíleně nepravidelný tvar ozařovaného objemu. Tvarováním ozařovaného pole je modulována i intenzita svazku a tak dochází k dalšímu zlepšení distribuce dávky (např. šetření míchy při ozařování krku nebo konečníku při ozařování prostaty). Zároveň lze dosáhnout i rozdílného rozložení dávky v ozařovaném objemu. Navíc se získá prudký dávkový spád do okolí a lépe se šetří okolní zdravé tkáně.
Dozimetrické výhody použití IMRT techniky (rozložení dávky záření) jsou dosaženy díky modulaci dávkového rozložení především u radioterapie nádorů nosu, paranazálních dutin a baze lební, tedy lokalit, které bylo dříve velice obtížné dávkově homogenně pokrýt, aniž by současně nebyly ozářeny okolní rizikové orgány. Další dozimetrickou výhodou je možnost šetřit velké slinné žlázy s cílem snížit riziko pozdní xerostomie (suchost v ústech). S výhodou se technika využívá i při ozařování prostaty, kdy je šetřen konečník nebo při ozařování gynekologických nádorů nebo konečníku, kdy jsou šetřeny střeva a močový měchýř před zářením.
VMAT technika radioterapie (Volumetric Modulated Arc Therapy)
Jedná se o formu radioterapie IMRT (radioterapie s modulovanou intenzitou), kdy se k modulaci intenzity svazku záření (přesněji fluence) pomocí lamel kolimátoru (systém lamel v hlavici přístroje upravující tvar ozařovaného pole) přidává modulovaný pohyb ramene (gantry) urychlovače, modulace dávkového příkonu a u nejmodernějších přístrojů také dynamická změna polohy clon (jaw tracking).
Dodání dávky probíhá za současného pohybu ramene a hovoříme tak o objemově modulované radioterapii kyvem – Volumetric Modulated Arc Therapy (VMAT), starší označení pro techniku bylo IMAT (Intensity Modulated Arc Therapy). S pomocí této techniky lze dosáhnout vysoce konformního prozáření cílového objemu (nádoru) a zároveň zajistit potřebný strmý spád dávky do okolí, aby bylo zajištěno maximální šetření zdravých tkání.
Nezanedbatelným přínosem je také rychlost dodání potřebné dávky záření. Zkrácení doby potřebné pro ozáření je nejen komfortem pro pacienty, ale snižuje se také riziko pohybu pacienta během ozáření a tím se také snižuje riziko nepřesného ozáření. Dalšími pozitivními efekty tohoto způsobu radioterapie jsou zkrácení čekací doby a zvýšení využitelnosti přístroje.
Simultánní integrovaný boost (SIB)
Pro princip navýšení dávky v určitém menším objemu za současného ozařování dalších struktur (většího objemu) se používá pojem simultánní integrovaný boost (SIB). Technikou SIB se zvyšuje dávka v podobjemu s nejvyšším rizikem recidivy (makroskopický tumor, lůžko tumoru), např. mozkovna je celá ozařována 3 Gy, ale v místě ložiska (metastáza, tumor) je dávka navýšena na 4 Gy.
Řízené dýchání při ozařování prsu
Součástí léčby po operaci prsu pro zhoubný nádor je i ozařování. Jedna z častých otázek žen je vliv záření na srdce. Kontrola (ne)ozáření srdce je důležitou součástí tvorby ozařovacího plánu.
Radioterapie se připravuje pomocí CT vyšetření, na kterém je dobře vidět umístění srdce. Díky němu lze záření zacílit tak, aby procházelo jen prsem a srdce co nejvíce minulo (obr. 1). U většiny žen v případě použití moderních urychlovačů je dávka záření v oblasti srdce tak malá, že nepředstavuje žádné riziko. U menší části je ale srdce blízko u prsu a část záření jím prochází (obr. 2). V takovém případě lze použít ozařování v nádechu (obr. 3), pomocí kterého se srdce opět dostane do bezpečné vzdálenosti. A ozařuje se pouze v nádechu; urychlovač se tedy opakovaně vypíná a spouští. Nádech (polohu hrudníku) kontroluje speciální snímací zařízení položené na hrudníku.

Obr. 1: Srdce je vzdálené od prsu, nehrozí žádné riziko, standardní 3D technika radioterapie fotony lineárního urychlovače. Barevné linie v obrázcích: růžová barva – srdce; modrá linie – objem ozařovaného prsu; barevná plocha – ozářená oblast
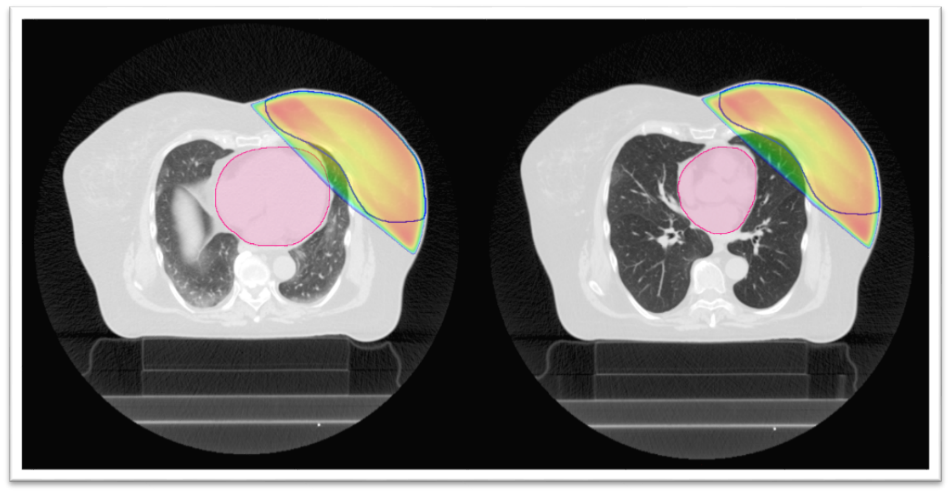
Obr. 2 (vlevo): Srdce v blízkosti prsu a část záření skrz něj prochází, proto lékař rozhodne o ozařování v nádechu.
Obr. 3 (vpravo): Ozařování v nádechu („řízené dýchání“) – na ozařovacím plánu je patrné výrazné zlepšení ve smyslu ochrany srdce před zářením.
Barevné linie v obrázcích: růžová barva – srdce; modrá linie – objem ozařovaného prsu; barevná plocha – ozářená oblast
Intrakraniální stereotaktická radioterapie a radiochirurgie
Intrakraniální stereotaktická radioterapie a radiochirurgie je speciální ozařovací technika, kterou se cíleně ozařují malé objemy nádorových ložisek v mozkovně (intrakraniální). Technika s tímto složitým názvem se v Masarykově onkologickém ústavu provádí již více než deset let. Nyní po nutné modernizaci potřebného vybavení (nové lineární urychlovače a fixační zařízení) lze tuto léčebnou metodu nabídnout více pacientům.
Při vhodné velikosti a uložení nádoru v mozku se s výhodou využívá ozařování vysokými dávkami záření, v krajním případě pak ozáření jednou jedinou, velice vysokou, dávkou fotonového záření. V tomto případě pak léčba probíhá, na rozdíl od klasické několikatýdenní radioterapie, v průběhu jednoho dne a napodobuje tak chirurgický výkon (radiochirurgie).
Při aplikaci vysoké dávky záření je extrémně důležitá přesnost ozáření tak, aby bylo zajištěno, že vysoká dávka záření zasáhne nádor a ne okolní zdravou tkáň. Tato dávka způsobí nekrózu zasaženého ložiska, ne však ihned jeho vymizení. Nutného znehybnění a fixace pacienta k ozařovacímu stolu nyní dosahujeme novým stabilizačním systémem se submilimetrovou přesností nastavení (celý proces přesného nastavení polohy pacienta se historicky nazývá stereotaktickým).
Dříve používaný systém invazivní fixace do stereotaktického rámu (napevno připevněného speciálními šrouby do hlavy) je nyní nahrazen speciální maskou a otiskovou fixací horní čelisti se srovnatelnou přesností, jejíž použití je navíc bezpečnější a pacienty více akceptované.
Historicky se rozlišuje stereotaktická radioterapie (SRT - stereotactic radiotherapy), kde je aplikovaná dávka rozdělena do několika frakcí, a radiochirurgie (SRS - stereotactic radiosurgery), u níž je aplikována celá dávka jednorázově. V současnosti se tento terminologický rozdíl stírá.
Extrakraniální stereotaktická radioterapie (radiochirurgie)
Extrakraniální stereotaktická radioterapie/radiochirurgie využívá k léčbě nádorových ložisek velmi přesné aplikace vysokých dávek záření v malém počtu frakcí (1-5). V praxi se pro tuto metodu léčby používá označení SBRT či SABR odvozené z anglických zkratek „stereotactic body radiotherapy/stereotactic ablative radiotherapy“. Její rozvoj umožnila lepší vybavenost radioterapeutických pracovišť (moderní fixace pacientů, svazky záření „šité stereotaxi na míru“, možnosti prostorové navigace svazků na cíl, přesná a rychlá aplikace dávky, atd.).
Při odpovídajícím přístrojovém vybavení lze tuto metodu v dnešní době využít při léčbě nádorových ložisek v plících, játrech, dutině břišní, pánvi či ve skeletu. Dlouhodobý lokální efekt řadí tento způsob léčby mezi výkony radikální i přesto, že v řadě případů se jedná v širším slova smyslu o paliaci (léčba metastatických ložisek). V řadě indikací má však SBRT/SABR jednoznačně kurativní potenciál (primární plicní tumory atd.).
Technika SBRT/ SABR se provádí standardně lineárním urychlovačem (X – nůž) či systémy z něj odvozenými (robotický urychlovač Cyber Knife, Tomoterapie a další). Nezbytnou součástí přístrojů je možnost obrazové navigace (IGRT – radioterapie řízená obrazem). Vysoké dávky záření koncentrované do malého cílového objemu dosahují maximálního letálního účinku. Aplikovaná dávka se pohybuje až v desítkách Grayů (Gy), např. 3 x 18-20 Gy, 5 x 11-12 Gy nebo jednorázově 1x 10-30 Gy. Díky přímému nekrotizujícímu účinku na buňky je při takto vysokých dávkách překonána buněčná radiorezistence. Nekrotizovaná tkáň se následně během několika měsíců fibroticky mění.
Vysoká přesnost doručení dávky umožňuje ozáření cílových objemů nacházejících se v těsné blízkosti radiosenzitivních orgánů (např. míchy, ledvin, tenkého střeva apod.); další indikací SBRT/SABR jsou nádory v již dříve ozářeném terénu nebo nádory primárně radiorezistentní. Přesnosti léčby je dosaženo zvýšenou úrovní fixace pacienta (maska, rám, vakuová dlaha, stlačení žaludeční krajiny atd.), kontrolou polohy pacienta (využití obrazové navigace, aplikace a sledování zlatých zrn, CT vyšetření urychlovačem přímo na ozařovacím stole – cone beam CT, sledování dýchacích pohybů atd.). Vše dohromady umožňuje použití velmi malých bezpečnostních lemů, což při použití vysoce konformních technik radioterapie s velkým dávkovým spádem zaručuje minimální poškození přilehlých zdravých tkání.
Extrakraniální stereotaktická radioterapie je velmi efektivní a výborně tolerovanou lokální metodou léčby nádorových onemocnění s minimem vedlejších účinků.
Akcelerované ozáření nádoru prsu brachyterapií
Léčba zhoubného nádoru prsu je kombinovaná. Po operačním výkonu, při kterém je odstraněna část prsu s nádorem, většinou následuje (mimo jiné) pooperační ozáření s cílem snížit riziko recidivy – nového objevení nádoru v prsu. Pooperační ozáření v nižších stadiích choroby může být provedeno formou ozáření pouze oblasti původního uložení nádoru – tzv. lůžka nádoru, kde je největší riziko vzniku recidivy nádoru.
Samostatná intersticiální brachyterapie je jedna z metod ozáření v místě lůžka nádoru prsu. Brachyterapie je metoda tzv. „vnitřního ozáření“, kdy se do daného objemu tkáně, orgánu zavádí radioaktivní zdroj iridia (zdroj má asi 1 mm průměr a délku 5 mm). Výhodou této metody je kratší doba (1 týden) trvání léčby (akcelerace, tj. „zrychlení“) proti standardnímu ozáření zevní radioterapií lineárním urychlovačem (5-7 týdnů).
Při samostatné intersticiální brachyterapii jsou nejdříve v celkové anestézii zavedeny do místa původního uložení (lůžka) nádoru plastikové trubičky (vodiče radioaktivního zdroje). Plastikové trubičky jsou ohebné, zůstávají po celou dobu ozařování zavedeny v prsu. V dalším průběhu výkonu není anestézie již nutná. Samotné ozařování pak probíhá 2x denně, celkem 4-5 dnů. Při každém ozáření se vodiče připojí k přístroji, který automaticky zavádí zdroj do požadovaného objemu prsu. Zdroj záření ozáří cíleně pouze lůžko nádoru (s bezpečnostním lemem) a tím se sníží ozáření okolních zdravých tkání (kůže, podkoží, plíce, srdce aj.). Vlastní ozáření trvá asi 5 minut a většinou se provádí v 8 ozáření (frakcích), 2x denně. Bezprostředně po posledním ozáření jsou katetry z prsu odstraněny prostým vytažením; tento výkon je nebolestivý. Léčba samostatnou intersticiální brachyterapií vyžaduje hospitalizaci, jejíž celková doba je přibližně 10 dnů. Nahradí se stejným léčebným efektem a nižšími pozdními následky léčbu zevní radioterapii.
MR-Linac přístroj
MR-LINAC (Magnetic Resonance Imaging Guided Linear Accelerator) využívá zobrazování magnetickou rezonancí souběžně s radioterapií k léčbě nádorových onemocnění celého těla s výraznou výhodou v oblasti nádorových ložisek uložených v měkkých tkáních.
Aplikace dávky záření na MR-LINAC je plně integrována s magnetickou rezonancí. To znamená, že systém může aplikovat záření a současně monitorovat cílovou oblast pomocí MR vyšetření.
Ve srovnání s tradičními lineárními urychlovači, které používají k vizualizaci cílové oblasti a anatomie okolních struktur pro nastavení a aplikaci léčby zobrazování na bázi rentgenového záření, nabízí MR-LINAC vynikající kvalitu obrazu s vysokým rozlišením na základě MR snímkování s největší výhodou pro ložiska uložená v měkkých tkáních.
S výhodou se používá pro stereotaktickou radioterapii kraniální I extrakraniální. Systém je spojen s možností adaptivní radioterapie, tedy vytvoření přesného ozařovacího plánu na základě aktuálního MR vyšetření na ozařovacím přístroji.
Adaptivní radioterapie
Základním principem adaptivní radioterapie je aktivní systematická modifikace původního plánu (tzv. replanning) na základě změn objemu nebo topografie cílového objemu či rizikových orgánů, což souvisí většinou se změnou-zmenšením objemu nádoru během léčby. Cílem adaptivní radioterapie je maximálně přesná aplikace dávky do cílového objemu za současné redukce dávky v rizikových orgánech v okolí. V praxis to znamená vytvoření nového ozařovacího plánu na základě aktuálního nálezu při CT či MR vyšetření.
CyberKnife
Přístroj CyberKnife firmy Accuray je díky své ojedinělé konstrukci unikátem na poli radioterapeutických ozařovačů. Odlehčený 6 MV lineární urychlovač je umístěný na robotickém rameni se 6 stupni volnosti. Léčebný svazek je kolimován vyměnitelnými wolframovými tubusy o průměrech 5-60 mm, moderní přístroje této řady pak disponují kolimátorem IRIS, který umožňuje měnit velikost pole, bez nutnosti výměny pevných tubusů.
O sledování polohy ozařovaného cílového objemu se starají dva ortogonální rentgenové zdroje, které snímkují pacienta pod úhlem 45°. Kontinuální sledování polohy spolu s volností pohybu ozařovače kolem pacienta a průběžné korekce polohy pacienta umožňují velmi přesné ozáření i pohybujících se cílových objemů. CyberKnife je tak vhodný k provádění bezrámové radiochirurgie.
Tomoterapie
Tomoterapie je ozařovací systém firmy Accuray. Zdrojem ionizujícího záření je zde 6 MV lineární urychlovač, ovšem konstrukce přístroje se od klasických lineárních urychlovačů značně liší. Zde principiálně vychází z diagnostických CT přístrojů. Zdroj záření obíhá v 360° kolem pacienta za současného posunu pacientského stolu. Ozáření tak probíhá helikálně po tomovrstvách. Stejný zdroj, tedy 6 MV lineární urychlovač pak slouží k provedení MVCT (Megavoltage computed tomography) před vlastním ozářením a přístroj tak umožňuje každodenní provedení 3D IGRT kontrolu. Vlastní ozařovací technika je IMRT, kdy modulaci svazku zajišťuje binární vícelamelový kolimátor.
Halcyon
Jedná se o nový typ lineárního urychlovače, který má uzavřenou konstrukci gantry. V léčbě využívá vysoký dávkový příkon, terapii kyvem (RapidArc, VMAT) IGRT a duálního vícelamelového kolimátoru. Přístroj byl vyvinut pro zrychlení komfortní radioterapie. Jeho dalším vývojovým stupněm je lineární urychlovač Ethos, který více využívá možností adaptivní radioterapie při každodenním ozařování.
Protonová radioterapie
Mezi výhody a přínosy protonové radioterapie ve srovnání se současnými modalitami v radiační onkologii se uvádí:
- specifický průběh křivky hloubkové dávky
- možnost přizpůsobení šířky Braggova píku rozměrům cílového objemu nádoru
- snížení integrální dávky s dopadem na snížení výskytu sekundárních malignit.
Mezi rizika protonové radioterapie patří:
- vysoká citlivost na tkáňové nehomogenity
- nepřesnosti z pohybu cílového objemu a kritických orgánů (OAR)
- nepřesnosti se zohledněním rozdílu fyzikální a biologické dávky.
Přítomnost kostí ve svazku protonů způsobuje významný posun a degradace Braggova piku v proximálních oblastech cílového objemu a může vést k výraznému poddávkování. Naopak v případě přítomnosti vzduchové mezery (plíce, tělní dutiny, hlen, náplň střev, močového měchýře) se Braggův pík posouvá vzdáleněji a může způsobit poškození přítomných kritických struktur.
Fotonovou technologií IMRT spojenou s IGRT lze obvykle ozářit cílový objem stejnou dávkou jako protony. Ozařování fotony je přitom nezbytně doprovázeno ozářením velkého objemu zdravých tkání nízkou až střední dávkou, spojeného s potenciální morbiditou. Protony ve velké míře snižují zářením zasažený objem tkání, což představuje hlavní argument pro jejich využití.
Na druhé straně, protony při srovnání s fotony narážejí na řadu problémů, které mají za následek potenciálně větší rozdílnost mezi plánovanou a podanou dávkou záření. Neurčitosti při plánování ozařování protony jsou oproti fotonům větší.
V klinické praxi chybí zatím dlouhodobé (více než dvacetileté) údaje, umožňující porovnat celoživotní riziko vzniku sekundárních malignit obou modalit, fotonové a protonové terapie. Přesto předpokládaná výhoda redukce vzniku sekundárních malignit může odůvodnit indikaci léčby protony u pediatrických nebo mladých pacientů, zejména při nutnosti ozařování velkých objemů
Radioterapie karbonovými ionty
Sarkomy a chordomy jsou považovány za radiorezistentní onemocnění a jejich léčba často vyžaduje ozáření vyššími dávkami a velkých objemů, tedy i většího objemu zdravých tkání. V určitých lokalizacích lze očekávat významný dozimetrických benefit ozařování protony. Při ozařování sarkomů pánve u fertilních žen může případnou dozimetrickou nevýhodu fotonového svazku upravit chirurgická extrapozice vaječníků.
Tradiční indikace ozařování chordomů lebeční báze protonovým svazkem se traduje z období, kdy možnosti konformního fotonové radioterapie byly menší, než je tomu dnes. Očekávaný biologický účinek protonů při ozařování sarkomů bude podobný jako v ostatních lokalizacích. Při ozařování karbonovými ionty (carbon ion beam radiotherapy, CIRT), díky hustší ionizaci, lze očekávat vyšší efektivitu. Ověření tohoto předpokladu vyžaduje klinické důkazy, podobně jako u nových lécích. Jedná se o experimentální léčbu radiorezistentních nádorů. Naší republice jsou nejblíže pracoviště v Heidelbergu a Winner Neue Stadt.
Závěr
Vzhledem k fyzikálním charakteristikám ozařovacích svazků (fotony, protony, elektrony, neutrony aj.) nelze dosáhnout nulových hodnot záření v tkáních přilehlých cílovému objemu. Cílem moderní léčby zářením je dosáhnout minimální toxicity radioterapie. K diskusi zůstává problematika tzv. finanční toxicity různých ozařovacích technik, tzn. neúměrný nárůst výdajů na léčbu bez ohledu na její nákladovou efektivitu. Jedná se o jakousi analogii s moderními přípravky cílené protinádorové léčby a imunoterapie, kde je pojem finanční toxicita nově zaváděn a musí být brán v potaz v každodenní diagnosticko-terapeutické rozvaze.