Obsah:
- Rakovina kůže
- Anatomie a funkce kůže
- Co to vlastně je rakovina kůže?
- Jak se rakovina kůže projevuje?
- Jak vlastně rakovina kůže vzniká? Je dědičná? Existují rizikové faktory jejího vzniku?
- Lze rakovině kůže předejít?
- Diagnóza rakovina kůže - jak se stanovuje?
- Jak ovlivňuje stádium kožní rakoviny volbu léčby?
- Jak se rakovina léčí?
- Co se děje po ukončení léčby?
- Co když se rakovina vrátí?
- Kde mohu najít další informace?
Rakovina kůže
Rakovina kůže je onemocnění, které postihuje nejprve kůži a v některých případech může prorůstat do hlouběji uložených partií těla nebo zakládat dceřiná ložiska (metastázy) v jiných orgánech. Některé z těchto nádorů mohou působit destruktivně pouze v místě svého vzniku a poškozovat tak nejen kůži, ale i okolní sliznice, svalovinu, kosti, chrupavky nebo okolní orgány jako je oko, jiné ohrožují na životě metastazováním. V článku si uvedeme některé epidemiologické údaje těchto onemocnění a seznámíme s diagnostikou, léčbou a dalšími následnými postupy.
Anatomie a funkce kůže
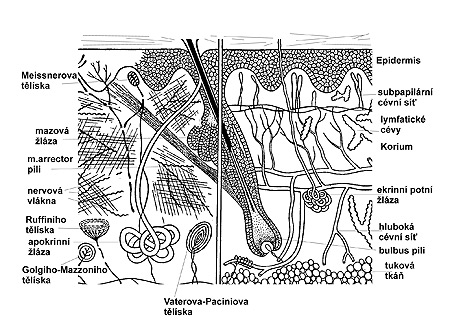
Kožní povrch představuje plochu v průměru 1,5 až 2 m2 a hmotnost kůže odpovídá zhruba jedné pětině tělesné hmotnosti, což je u dospělého člověka přibližně 15 kg. Tato čísla dokumentují, že kůže je největším orgánem lidského těla. Její skladba umožňuje co nejlépe vykonávat ochrannou funkci jako orgánu na rozhraní mezi organismem a zevním prostředím. Na kožním povrchu jsou nerovnosti, záhyby a rýhy. Mimika v obličeji způsobuje pro každého člověka více méně typické vrásky. Pro konkrétní osobu jsou charakteristické tzv. Purkyňovy kresby (dermatoglyfy) na bříškách prstů, čehož se využívá k identifikaci osob (daktyloskopie). Jejich průběh je podmíněn uspořádáním papil koria, které závisí na konfiguraci kolagenních a elastických vláken se střední vrstvě kůže, která se jmenuje dermis, česky škára. Typické odchylky od běžného obrazu nacházíme u některých geneticky podmíněných chorob.
Na barvu kůže má vliv řada vnitřních i zevních faktorů. Je to zejména množství kožního pigmentu melaninu, tloušťka rohové vrstvy, stupeň prokrvení, množství hemoglobinu v krvi a jeho saturace kyslíkem. Charakter barevného vzhledu podmiňuje i obsah vody (hydratovaná kůže je méně průsvitná a působí bělejším dojmem) a lipidických látek v epidermis nebo karotenu v podkožní tukové tkáni.
Kůže se skládá ze tří základních částí: epidermis (pokožka), dermis (korium, cutis, škára) a tela subcutanea (subcutis, podkoží) (obr. 1).
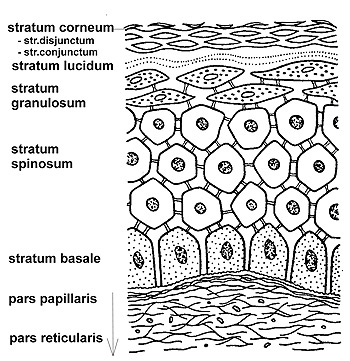 Kožní nádory se mohou tvořit buď z pigmentotvorných buněk, které jsou umístěny v nejspodnější vrstvě pokožky (epidermis - obr. 2), nebo z většinové populace vlastních epidermálních buněk keratinocytů. Další zhoubné kožní nádory mohou vznikat i z některých krevních buněk a napadat kůži, jsou však méně časté a v tomto článku se jim nebudeme podrobně věnovat. Totéž platí i pro některé vzácné zhoubné nádory kůže, které pocházejí z různých kožních struktur resp. buněk.
Kožní nádory se mohou tvořit buď z pigmentotvorných buněk, které jsou umístěny v nejspodnější vrstvě pokožky (epidermis - obr. 2), nebo z většinové populace vlastních epidermálních buněk keratinocytů. Další zhoubné kožní nádory mohou vznikat i z některých krevních buněk a napadat kůži, jsou však méně časté a v tomto článku se jim nebudeme podrobně věnovat. Totéž platí i pro některé vzácné zhoubné nádory kůže, které pocházejí z různých kožních struktur resp. buněk.
Kůže má pro člověka celou řadu významných funkcí. Tvoří fyzikální, chemickou a biologickou bariéru vůči zevnímu prostředí, má schopnost vylučování některých látek z organismu a naproti tomu příjímání jiných látek ze zevního prostředí. Může velké množství látek metabolizovat. Rozsah výměny látkové probíhající v ní představuje dokonce až třetinu metabolismu největší chemické “továrny” v těle - jaterní tkáně. Kůže se podílí na udržování stálé teploty organismu, je schopna registrovat řadu podnětů ze zevního prostředí, je z velké části zodpovědná za obranyschopnost organismu, umí ukládat pro další využití vodu, tuk a další látky. V neposlední řadě má významnou psychosociální funkci, reprezentuje nás navenek a podává o nás základní informaci v běžných mezilidských vztazích.
Co to vlastně je rakovina kůže?
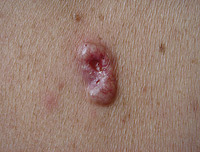
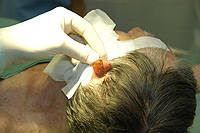
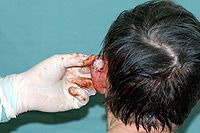
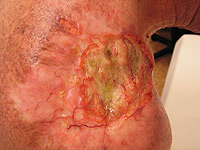
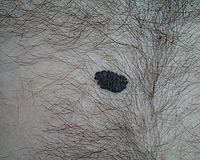
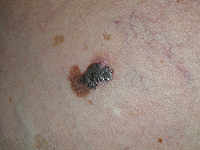
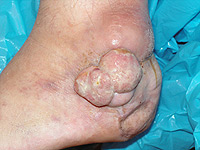
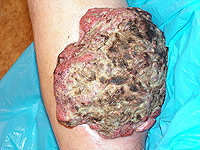
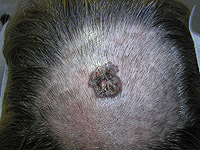
Na kůži vzniká velké množství různých druhů nádorů. Mnohé z nich jsou nezhoubné, působí pouze kosmetický problém. Jak jsme si již uvedli, pod pojmem rakovina kůže obvykle vnímáme zhoubný nádor. Ty jsou u lidí nejpočetnějšími zhoubnými nádory vůbec. Již víme, že nejčastějšími z nich jsou nádory vznikající ze struktur nejpovrchnější kožní vrstvy-epidermis, pokožky. Jedná se o bazaliom (Obr. 3), což je nádor poškozující téměř výhradně místo svého vzniku a jeho bezprostřední okolí. Totéž platí ve většině případů, ale bohužel ne stoprocentně i pro spinaliom (Obr. 4). Ten už totiž může vytvářet vzdálená dceřiná ložiska jinde v těle a poškozovat tak nejen okolí místa svého vzniku, tak i jiné orgány (proto jej důsledně operujeme - Obr. 5) a ohrožovat tak nemocného na životě (Obr. 6). Z tohoto pohledu je nejnebezpečnější formou kožní rakoviny maligní melanom, který se zpočátku projevuje na první pohled nenápadnou skvrnkou (Obr. 7, Obr. 8) a může končit rozsáhlými orgánovými metastázami jako v kůži (Obr. 9 a Obr. 10), mízních uzlinách, mozku, plicích, játrech aj.
Jak se rakovina kůže projevuje?
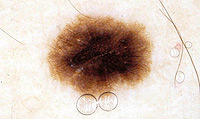
Obrovskou výhodou diagnostiky kožní rakoviny je skutečnost, že kožní změny jsou volně přístupné ke sledování každému z nás. Mohlo by se tedy zdát, že není důvod, aby pacient přišel k lékaři s kožním nádorem pozdě. Bohužel v mnoha případech je tomu naopak. Souvisí to pravděpodobně s tím, že řada z nás se dlouho rozmýšlí, zda se jedná o podezřelou změnu, zda je dobře, aby lékař včas zahájil léčbu anebo si prostě relativně malého a na první pohled často i podceňovaného kožního projevu na méně přístupném místě nevšimne. Podle druhu kožní rakoviny se liší i její klinický obraz, takže nelze dát univerzální návod, jak kožní nádor vypadá. Některé příklady uvádíme na přiložených obrázcích. Kožní rakovina může být v některých případech zaměněna za jinou kožní změnu, např. nezhoubný kožní výrůstek (benigní nádor), rozšířenou cévu, klidné pigmentové znaménko apod. Proto existuje několik pomůcek, jak tuto diagnostiku alespoň částečně usnadnit. Jedním z takových postupů jsou ABCDE kritéria rozlišující mezi mateřskými znaménky a melanomem (více informací např. na www.melanomy.cz nebo www.melanom.cz).
Jak vlastně rakovina kůže vzniká? Je dědičná? Existují rizikové faktory jejího vzniku?
Již ze všech možných údajů prakticky s jistotou víme, že sluneční záření a citlivá kůže kožního typu I, II jsou faktory, které výrazně zvyšují riziko vzniku rakoviny kůže. Dalším faktorem je tzv. pozitivní rodinná anamnéza, což jinými slovy znamená, že ohroženou skupinou jsou ti, jejichž přímí pokrevní příbuzní již měli kožní rakovinu. Stejně tak to platí i pro jedince, kteří již onemocněli rakovinou kůže v minulosti. Ti mají například u melanomu 10x větší pravděpodobnost opětného vzniku melanomu než je tomu u zdravých. Osoby, jež mají na kůži větší počet pigmentových znamének, mají také zvýšené riziko vzniku melanomu. Protože se předpokládá, že tato znaménka se vytvářejí v útlém dětství působením ultrafialového záření, je jedním z preventivních mechanismů účinná ochrana dětí před sluncem. Někdy se na vzniku rakoviny kůže spolupodílí i oslabený imunitní systém organismu.
Lze rakovině kůže předejít? - text najdete v části Prevence
Diagnóza rakovina kůže - jak se stanovuje?
Kůže je pro vyšetření dobře přístupná a dermatovenerolog (kožní lékař) má dostatek znalostí k tomu, aby byl schopen vyslovit diagnózu řady chorob včetně kožních nádorů často z pouhého pohledu nebo z běžného klinického vyšetření.
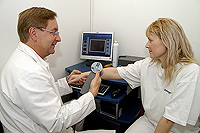
Dermatoskopie přinesla zkvalitnění této diagnostiky především u pigmentových projevů. Je to metoda, která používá zvláštním způsobem upravenou osvětlenou lupu. Rozdíl oproti prosté lupě spočívá v tom, že na spodní části okuláru se zvětšovacím sklem je ještě jedno ploché sklo, které se přímo dotýká při vyšetření kůže. Navíc štěrbina mezi kůží a tímto sklem je zvlhčena gelem nebo tekutinou. Toto vlhké prostředí vyplní veškeré kožní nerovnosti pod sklem, čímž se zruší běžný odraz světla z kožního povrchu. To umožní posuzovat kožní struktury (obvykle pigmentové) v hlubších partiích kůže.
Digitalizace tohoto obrazu, která probíhá buď tak, že analyzujeme obraz z připojeného digitálního fotoaparátu, nebo se přímo jedná o online analýzu obrazu z dermatoskopického zařízení, tvořeného výše popsanou optikou s videokamerou (Obr. 13). To umožňuje expertní analýzu. Speciální software posuzuje znaménko nebo jinou pigmentovou změnu podle ABCD kritérií. Data zpracuje, zhodnotí a zároveň porovnává strukturu obrazu s fotografiemi, které má uloženy v paměti, a vyhodnotí pravděpodobnost přítomnosti zhoubného nebo nezhoubného projevu (Obr. 14).
Jaké jsou výhody tohoto vyšetření:
- zvětšení projevu až 50x
- obraz lze zastavit na obrazovce monitoru a pohodlně si ho prohlédnout
- archivace snímku (uložení v paměti počítače) a posouzení vývoje změn v různých časových odstupech
- podává i zkušenému dermatologovi pomocnou ruku při diferenciální diagnostice a během několika sekund odhaduje stupeň závažnosti toho konkrétního kožního nálezu
- obraz lze vytisknout pro klinickou i domácí archivaci nebo jej elektronicky přeposlat pacientovi nebo dalším odborníkům k posouzení
Pokud je tímto postupem projev označen jako podezřelý, odstraní se dermatochirurgicky a podrobí se histologickému vyšetření v mikroskopu. Jedná se většinou o drobný výkon v místním znecitlivění. Mikroskopické vyšetření tkáňového vzorku, které slouží k definitivnímu stanovení diagnózy, se dá provést pouze z nepoškozeného kvalitního materiálu. Velmi tedy záleží na šetrném vyjmutí útvaru, případně nádoru, které se nám podaří prakticky výhradně s použitím skalpelu. Jako kožní lékaři důrazně odrazujeme především při podezření na melanom od leptání znamének různými chemikáliemi, mrazení tekutým dusíkem nebo odpařování laserem či elektrickým operačním nástrojem. Takováto likvidace podezřelé tkáně nám ve většině případů zabrání ve stanovení důležité mikroskopické diagnózy a zároveň i zkontrolování, zda se znaménko podařilo odstranit celé. Tato informace je velmi důležitá, protože v případě neúplného vyndání útvaru můžeme následným malým chirurgickým výkonem odstranění včas a spolehlivě dokončit.
Určitě není namístě si pokládat otázku: "mám si to vůbec nechat vyřezávat?" Je-li již jednou vysloveno podezření na zhoubný nádor, před dalšími nepříjemnostmi vás může spolehlivě ochránit pouze kvalitně provedený dermatochirurgický, tedy operační výkon. Je třeba zdůraznit, že zákrok nijak nezhorší prognózu onemocnění, pro které se provádí. Z podstaty věci je tomu právě naopak. Odstraníme-li co nejdříve nádorovou tkáň, sníží se riziko, že se z ní uvolní nádorové buňky, které by mohly založit dceřiná ložiska – metastázy.
Nádorové buňky se mohou z původního ložiska šířit různými cestami, z nichž u maligního melanomu a někdy i u spinaliomu je nejčastější šíření mízními cévami. V dřívějších dobách se proto se od určité tloušťky melanomu odstraňovaly veškeré mízní uzliny v příslušné spádové oblasti. Ty totiž slouží jako jakýsi filtr v potrubí, který může nádorové buňky vychytat a nějakou dobu zabránit jejich rozšíření dále do organismu. Nedovede je ale zlikvidovat, takže při jejich ponechání v uzlině se může vytvořit druhotné nádorové ložisko. Později se zjistilo, že lymfa (míza) teče obvykle nejprve do jedné uzliny a potom teprve protéká do dalších uzlin v okolí a také nádorové buňky se tedy nejprve zachytí v první uzlině a teprve později se mohou šířit do okolních uzlin. Proto se hledaly způsoby, jak tuto první spádovou (sentinelovou) uzlinu objevit. V dnešní době tato metoda již existuje. K vyhledání první spádové uzliny využívá kombinaci označení radioizotopem a barvivem. K tomuto zákroku jsou indikováni všichni pacienti s klinicky velmi podezřelým nádorem, u kterého očekáváme tloušťku větší než 1 mm nebo pacienti, u kterých byl již melanom odoperován a histopatolog změřil tloušťku rovnou nebo větší 1 mm. Tato indikace vychází z celosvětově platných doporučení.
V praxi takový zákrok vypadá tak, že pacient obvykle za krátkodobé hospitalizace absolvuje výkon v místním znecitlivění, kdy se vyjme již zmíněná spádová uzlina, která se podle lokalizace melanomu nachází většinou ve třísle, v podpaží nebo na krku (Obr. 15). Před tímto zákrokem se provede vlastní označení, které má 2 fáze. Nejprve se na pracovišti nukleární medicíny vstříkne podkožně v okolí nádoru nebo jizvy po něm malé množství radioaktivně značených částic, které se mízní cestou dostanou do hledané mízní uzliny a v ní se vychytají. Těsně před operací se ještě do stejného místa podkožně vstříkne roztok patentní modři, který se stejným způsobem dostane do mízní uzliny. Operace se pak zahajuje po předchozí kontrole místa nad uzlinou speciální sondou, která je schopna změřit intenzitu záření vysílaného označenou mízní uzlinou. Toto vyšetření umožňuje najít nejbližší místo na kůži, pod kterým je uzlina uložena, a tím provést chirurgické odstranění spádové uzliny co nejšetrněji. I během operace se k vyhledávání průběžně používá sterilní vyhledávací sonda a přesné dohledání umožní navíc barevné označení patentní modří.
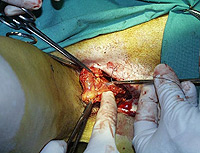 Uzlina se odešle k histologickému a histochemickému vyšetření. V případě, že se v ní najdou nádorové buňky, provede se následně odstranění všech uzlin ve spádové oblasti. Pokud tomu tak není, je pacient, u kterého by se dříve tato tzv. "elektivní lymfadenektomie" provedla, tohoto méně příjemného výkonu ušetřen.
Uzlina se odešle k histologickému a histochemickému vyšetření. V případě, že se v ní najdou nádorové buňky, provede se následně odstranění všech uzlin ve spádové oblasti. Pokud tomu tak není, je pacient, u kterého by se dříve tato tzv. "elektivní lymfadenektomie" provedla, tohoto méně příjemného výkonu ušetřen.
V tuto chvíli již víme, jak hluboko nádor prorůstal do kůže a zda se nádorové buňky šířily mízními cestami (histologické vyšetření sentinelové uzliny). Od určité tloušťky nádoru je ještě třeba doplnit informaci o tom, zda se nádorové buňky nedostaly i do jiných vnitřních orgánů krevní cestou. K tomu nám slouží kromě základního interního a neurologického klinického vyšetření i zobrazovací metody. Mezi tyto základní vyšetřovací metody patří sonografie (ultrazvukové vyšetření) břicha, mízních uzlin, RTG plic. Individuálně se pacient vyšetří i na oddělení nukleární medicíny pomocí scintigrafie skeletu, na rentgenovém pracovišti pomocí počítačové tomografie mozku(CT mozku) a v obzvláště komplikovaných případech se přistupuje i k vyšetření PET-CT (pozitronová emisní tomografie kombinovaná s CT vyšetřením).
Moderním postupem je dnes zjišťování množství cirkulujících melanomových buněk v krevním řečišti pomocí vyhledávání markerů na jejich povrchu metodou real-time RT PCR (podpořeno několika výzkumnými granty Interní grantové agentury Ministerstva zdravotnictví ČR). Tato metoda se zatím provádí pouze na Dermatovenerologické klinice Fakultní nemocnice Královské Vinohrady. Její výhodou je včasné zjištění rizika vzniku metastáz ještě dříve než to jsou schopna detekovat předchozí vyšetření.
Jak ovlivňuje stádium kožní rakoviny volbu léčby?
Prognózu a další léčebný postup u kožních nádorů významně ovlivňuje jejich celková tloušťka, případně další parametry. Proč právě tloušťka nádoru? Čím je nádor tlustší, tím se prognóza onemocnění zhoršuje. Velmi významná je tato korelace především u maligního melanomu. Za magickou hranici mezi příznivější a méně příznivou prognózou se považuje tloušťka 1 mm (v histopatologické nomenklatuře se udává jako Breslowův index). Ani pro pacienty s tloušťkou nádoru pod 1 mm to ale neznamená, že by už nemuseli po chirurgickém odstranění nádoru na kožní pracoviště docházet. Rozdílem je to, že se u nich ve většině případů vystačí s běžnou klinickou kontrolou, která se zaměřuje především na místní kožní nález a vyšetření mízních uzlin. Není nutný následný doplňující chirurgický zákrok ani podávání léků.
Tloušťka nádoru nad 1 mm ale už vyžaduje ještě různá další opatření.
Pro posouzení prognózy a volbu dalšího léčebného postupu je na základě získaných údajů ze všech vyšetření třeba zařadit pacienta do příslušeného stádia. Obecně řečeno platí, že pacienti s prokázaným postižením melanomem pouze kůže, se zařadí do stádia I nebo II. Ve stádiu III se nachází pacienti s primárním melanomem kůže a prokázaným průnikem melanomových buněk do spádových mízních uzlin (mikroskopické postižení zjištěné na podkladě vyšetření sentinelové uzliny nebo makroskopické postižení diagnostikované klinicky nebo pomocí sonografie). Do stádia III se dále řadí pacienti s kožními nebo podkožními metastázami melanomu, které se nacházejí buď v bezprostředním okolí nádoru nebo v prostoru mezi nádorem a spádovou mízní uzlinou. Do stádia IV se dostanou pacienti se vzdálenými metastázami na kůži, mízních uzlinách nebo vnitřních orgánech.
Jak se rakovina léčí?
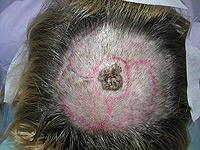
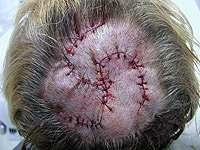
Už jsme si uvedli v kapitole o diagnostice, že nejlepší diagnostickou a při správném postupu i léčebnou formou u většiny nádorů je chirurgická excize. Obr. 16, Obr. 17, Obr. 18 nám ukazuje bazaliom ve kštici, rozkreslení plánu operace a kštici těsně po skončení výkonu. U maligního melanomu u nízkorizikových pacientů (stádium I a IIa) nenásleduje po chirurgickém odstranění melanomu žádná další léčba.
Rizikovější pacienti (obvykle se jedná o pacienty ve stádiu IIb a III) jsou po dobu 1-2 let léčeni následnou tzv. adjuvantní imunoterapií. Tato terapie není cytostatickou léčbou, ale jedná se o podávání interferonu alfa, dnes i experimentálně moderních biologik, resp. cílených preparátů. Interferon alfa je látka, která je za normálních okolností tvořena v malém množství buňkami imunitního systému. Její účinek je závislý na druhu organismu, ve kterém se vytváří. To znamená, že interferon alfa koně, účinkuje pouze u koní, lidský interferon alfa pouze u lidí. Proto se interferon alfa nedá získávat od jiných biologických druhů než lidí, ale podobně jako insulin, se ve větším množství dá připravit biotechnologickými metodami. Takový interferon je identický s lidským a může se dávkovat ve vyšším množství, než je jeho koncentrace za normálních okolností. Vysoká hladina interferonu alfa v krvi výrazně podpoří vlastní obranyschopnost organismu a nasměruje ji proti nádorovým buňkám, které by se mohly šířit do tkání. V několika klinických studiích byl prokázán jeho tlumící vliv na růst a množení nádorových buněk, ale i jeho příznivý účinek na regresi (zmenšení) nádoru.
Podávání interferonu alfa je pro nemocného relativně jednoduché. Pacient si obvykle sám vstřikuje podkožně z předplněné injekční stříkačky nebo speciálního dávkovacího pera stanovené množství léku. Forma aplikace se dá přirovnat k podávání insulinu u pacientů s cukrovkou, i když není tak častá.
Další léčebné možnosti u pacientů s různým postižením ve III. stádiu
| Chirurgie | Chirurgické (operační) řešení se využívá při odstraňování kožních a podkožních metastáz, zejména pokud jsou ojedinělé. Provádí se v místním znecitlivění. |
| Aktinoterapie | Aktinoterapie neboli ozáření se provádí při léčbě mnohočetných kožních, podkožních metastáz nebo metastáz ve spádových mízních uzlinách, které není možno odstranit operačně (z důvodu lokalizace, množství nebo stavu pacienta). |
| Intralezionální imunoterapie | Vstříknutí imunoterapeuticky působícího preparátu (nejčastěji interferon alfa nebo interleukin 2) injekčně přímo do kožní nebo podkožní metastázy. |
| Kryoterapie | Zmrazení kožní metastázy kryokauterem. |
| Laserová terapie | Odpaření ložiska kožní metastázy CO2 laserem. |
| Izolovaná končetinová cytostatická perfúze | Léčebný postup, který se používá k léčbě mnohočetných kožních nebo podkožních metastáz lokalizovaných na jedné končetině. Zabezpečení mimotělního oběhu postižené končetiny umožňuje aplikovat vysoké koncentrace cytostatika aniž by to významně zatížilo celý organismus. |
| Lokální terapie imiquimodem | Místní aplikace imiquimodu, látky, která působí imunostimulačně. Považuje se za experimentální přístup při léčbě kožních metastáz. |
| Exenterace mízních uzlinpostižené spádové oblasti | K tomuto zákroku jsou indikováni pacienti s průkazem metastáz v regionálních mízních uzlinách zjištěných na podkladě pozitivní sentinelové uzliny (viz výše) nebo klinicky/sonograficky přítomných metastáz v těchto uzlinách. Jedná se o zákrok v celkové anestézii, kdy se z postižené oblasti (nejčastěji z podpaží či třísel) odstraní všechny mízní uzliny. Nevýhodou této nutné operace je možnost vzniku lymfatického otoku postižené končetiny. Je nutné, aby byl pacient po takovém zákroku co nejdříve odeslán na oddělení rehabilitace k zahájení lymfodrenáží a cvičení, aby se předešlo vzniku těchto komplikací. |
| Experimentální podání “cílené” léčby | V dnešní době se pro pokročilejší stádia melanomu používá biologická nebo cílená léčba. Při cílené léčbě blokujeme aktivitu některých prorůstových protein v nádorových buňkách jako je například BRAF, cKIT, nRAS, MEK a další. V adjuvantní léčbě se zatím používá experimentálně blokování BRAF u pacientů, kteří mají tento gen mutovaný. |
Pacienti ve stádiu IV jsou léčeni podle typu postiženého orgánu, stavu nemocného a dalších kritérií chirurgicky, aktinoterapií, chemoterapií cytostatiky, imunoterapií nebo chemoimunoterapií a biologickou a cílenou léčbou. Orgánovými metastázami jsou nejčastěji postiženy plíce, játra, mozek, kosti a další orgány. Zlatým standardem cytostatické léčby u pacientů s pokročilým maligním melanomem je chemoterapeutikum dakarbazin. Moderní biologická a cílená léčba přinesla naději nemocným v pokročilém stádiu maligního melanomu s metastázami a lokálně progredujícího nebo metastazujícího bazaliomu.
Na našem trhu jsou z prostředků zdravotního pojištění hrazeny dva preparáty pro metastazující maligní melanom – biologikum ipilimumab (Yervoy) a cílený preparát vemurafenib (Zelboraf).
Biologikum ipilimumab (Yervoy) odblokovává receptor CTLA-4, čímž odbrzdí aktivitu imunitního systému. Ten se zaktivizuje do vysokých obrátek a umožní organizmu, aby se lépe vypořádal s přítomností nádorové tkáně. Nežádoucími účinky takto aktivovaného imunitního systému může být nastartování autoimunních reakcí, které mohou poškozovat vlastní tkáň střeva doprovázenou průjmy s krvácením, štítnou žlázu, hypofýzu a další. Lék se podává v infuzích v množství podle hmotnosti pacienta celkem ve 4 dávkách po 3 týdnech. Ze statistiky víme, že na léčbu pozitivně zareaguje v průměru 15 % procent nemocných a u 20 % pozorujeme stabilizaci onemocnění. Při posuzování výsledků zobrazovacích metod jako je RTG, počítačová tomografie, magnetická rezonance, scintigrafie nebo PET-CT se můžeme setkat s takzvanou pseudoprogresí, kdy se mohou metastázy přechodně zvětšovat. Není to ale dáno zmnožováním nádorové tkáně, ale prosáknutím metastáz zánětlivými buňkami bílé krevní řady, které postupně nádorovou tkáň následně likvidují. V experimentálních studiích je k dispozici I další preparát s podobnými protinádorovými účinky – anti PD1, kterému se podle předběžných výsledků klinického zkoušení přisuzuje dokonce ještě výrazně vyšší efekt, tedy že mnohem více pacientů příznivě zareaguje na léčbu, a rychlejší nástup účinku.
Preparát vemurafenib (Zelboraf) cíleně blokuje mutovaný protein BRAF, který najdeme asi u poloviny melanomů. Jedná se o takzvanou “malou molekulu”, což znamená, že se účinná látka vstřebává i při perorálním podávání, tedy užívání v tabletách. Lék se bere denně a viditelný efekt na zmenšování nádorové tkáně je u pacientů s BRAF mutací velmi rychlý. Nevýhodou této terapie je vytvoření rezistence, kdy si růst nádoru najde zřejmě jinou aktivační dráhu než je ta, kterou lékem úspěšně blokujeme. Nejzřetelnější nežádoucí účinky jsou naštěstí z dermatologické oblasti, takže si s nimi kožní lékař, který preparáty kromě onkologů také podává, snadno poradí. Jedná se o fotosenzibilitu, tedy spálení se na sluníčku při nesprávné nebo nedostatečné fotoprotekci, a vznik sekundárních nádorů na kůži ze skupiny keratoakantomů nebo spinaliomů. Častěji také nemocní popisují při léčbě zvýšenou únavu. Také tento preparát má další následovníky v oblasti klinického zkoušení. K dispozici máme podobně působící dabrafenib, který se zkouší i v kombinaci s blokátorem MEK proteinu stejné metabolické proliferační dráhy trametinibem.
Rozsáhlý lokálně progredující nebo dokonce metastazující bazaliom je naštěstí extrémně vzácné onemocnění. Při výskytu kolem 25000 nových bazaliomů v České republice ročně léčíme na Dermatovenerologické klinice FNKV v současnosti 23 takových případů a v celé ČR jich nebude ani o polovinu více, takže se pohybujeme na počtech kolem jednoho promile všech léčených. Při mutilujících nálezech v obličeji se zasažením oka, nosních chrupavek a kostí nebo zevního i vnitřního ucha jsme často dosud neměli účinnou léčbu. Tam, kde chirurgické řešení, fyzikální metody, fotodynamická terapie, lokální imunoterapie a chemoterapie nebo radioterapie selhala, pacient často rezignoval a ponechal bazaliom zvolna růst. Dnes je v rámci již uzavřeného klinického zkoušení nebo po dohodě se zdravotní pojišťovnou k dispozici cílený preparát vismodegib (Erivedge), který blokuje patologicky aktivovanou proliferační dráhu hedgehog a tím zastavuje růst bazaliomu a kůže se hojí. Preparát je velmi vhodný i u pacientů s Gorlinovým Goltzovým syndromem, kde běžně užívaná radioterapie nekontrolovaný růst bazaliomů dokonce urychluje a naopak vismodegib tu působí nejen léčebně, ale i preventivně, protože u těchto často mladých pacientů brání vzniku nových nádorů.
U některých typů nádorů (nikdy však u melanomu) můžeme použít při jednoznačné diagnóze i jiné léčebné postupy - například zmrazení, elektrokoagulaci, seškrábnutí, použití léku Aldara (imiquimod), Solaraze (diclofenac s kyselinou hyaluronovou), Efudix (5-fluorouracil) nebo Picato (ingenol mebutát). Jednou z nejefektivnějších metod lokální terapie je fotodynamická terapie, kdy se po tříhodinové inkubaci krémem s fotosenzibilizátorem osvítí léčená plocha intenzivním červeným světlem. Tím se selektivně zničí jen patologické nádorové buňky. Fotodynamickou terapii lze použít pouze u tumorů tenčích než 2 mm. U bazaliomu je tedy vhodné nejprve změřit tloušťku nádoru ultrazvukem nebo u větších bazaliomů při zvažování nechirurgické léčby ověřit tloušťku i diagnózu probatorní excizí kruhovým rotačním nožem, tzv. „průbojníkem“.
Co se děje po ukončení léčby?
Pacienti po prodělané chirurgické léčbě musí docházet na následné kontroly, říká se tomu dispenzarizace. Je nutné dodržovat časový harmonogram návštěv, který určí ošetřující lékař v závislosti na stádiu pacienta.
Tyto pravidelné kontroly mají své opodstatnění ze dvou hlavních důvodů a jsou nejznámější především u maligního melanomu:
- Se zvyšujícím se stádiem pacienta se zvyšuje i riziko vzniku dceřiných ložisek - metastáz.
- Pacienti s jedním melanomem jsou ohroženi vznikem druhého, tzv. duplicitního melanomu 10 x častěji než ostatní populace.
A tak se při každé kontrole v rámci dispenzarizace provádí fyzikální vyšetření kůže, včetně kštice, sliznic, dlaní a plosek. Dále se důkladně vyšetří jizva po odstraněném melanomu a palpačně i spádové mízní uzliny. V pravidelných intervalech se také v závislosti na stádiu onemocnění provádí zobrazovací metody ke zjištění případných metastáz.
Vzhledem k tomu, že 50 % metastáz u maligního melanomu vzniká během 5 let od chirurgické léčby primárního tumoru, jsou v tomto období nutné intenzivní a časté kontroly. Pozdní metastázy (po 10 letech po odstranění melanomu) jsou sice vzácné, ale možné, a proto by měla být následná péče, byť v omezené míře, doživotní.
Nesmíme zapomenout, že tyto kontroly plní i důležitou psychosociální funkci. Často se u těchto pacientů vyskytují nadměrné obavy, které může lékař správným vysvětlením celé problematiky a rozhovorem rozptýlit.
Co když se rakovina vrátí?
Recidiva se může zjistit při pravidelné kontrole u lékaře nebo její projevy zjistí přímo pacient či jeho okolí. Je třeba, aby se co nejdříve našlo vhodné řešení pro tohoto konkrétního nemocného a zvýšila se šance na další bezpříznakové období.
Kde mohu najít další informace?
O kožních nádorech se můžete informovat u vašeho nejbližšího dermatovenerologa, e-mailem například na adrese melanom@fnkv.cz nebo na webových stránkách www.melanom.cz a www.melanomy.cz.
Prof. MUDr. Petr Arenberger, DrSc.