Obsah:
- O nádorech hlavy a krku
- Diagnostika
- Léčba
- Prognóza, prevence, dispenzarizace
- Nádory nosohltanu
- Nádory slinných žláz
- Závěr
- Literatura
Mezi nádory hlavy a krku patří nádory horního dýchacího traktu, polykacích cest, slinných žláz, dále nádory vyrůstající z kůže této oblasti, nádory cév, nervů a dalších tkání. Přesto, že většina nádorů ORL oblasti je poměrně dobře přístupná klinickému vyšetření, velká část nemocných přichází k lékaři až v pokročilém stadiu onemocnění. V současné době vstupujeme do nového období, kdy se v léčbě karcinomů hlavy a krku stávají dostupnými nové látky, nové léčebné postupy, které umožňují lepší formulaci léčby pro většinu pacientů.1
Epidemiologie
Nádory oblasti hlavy a krku představují v zemích Evropské unie u mužů čtvrté nejčastější nádory. Výskyt je charakterizován stoupajícím množstvím od severu směrem ke Středozemnímu moři. Nejnižší hodnoty jsou ve Švédsku a Anglii. Nejvyšší výskyt byl zaznamenán ve Francii, kde jsou nádory oblasti hlavy a krku stejně časté jako nádory plic.2 Výskyt nádorů oblasti hlavy a krku u žen je výrazně nižší než u mužů. Také geografické rozložení je rozdílné, vyšší hodnoty výskytu jsou ve Francii, Švýcarsku, Skotsku a Dánsku, nízké ve Španělsku, Itálii, Finsku a některých zemích východní Evropy. V České republice byl v roce 2018 zaznamenán výskyt nádorů oblasti hlavy a krku 1 237 diagnostikovaných mužů a 539 diagnostikovaných žen.
Ročně u nás umírá na nádory hlavy a krku kolem 800 lidí v průměrném věku 59,72 let. Podrobné informace o výskytu nádorů oblasti hlava/krk uvádí Dušek a spol. v publikaci Czech Cancer Care in Numbers.3 České republice patří celosvětově 26. místo ve výskytu nádorů této lokality.
Anatomie a funkce
Pojem nádory hlavy a krku se používá zejména pro nádory polykacího a dýchacího ústrojí, postihující rty, dutinu ústní, nos, vedlejší nosní dutiny, hltan, hrtan, slinné žlázy a místní lymfatickou tkáň, dále se v této oblasti setkáváme s kožními nádory, nádory v oblasti ucha, očnice a s nádory štítné žlázy.4
Pro značnou rozdílnost místa vzniku jsou způsob místního nádorového růstu, vzdálené šíření a tím i příznaky značně odlišné. Pro optimální hodnocení, diagnózu i léčbu je velmi důležité místo vzniku nádoru.
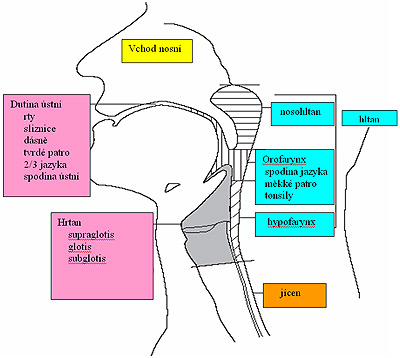
Dutina ústní představuje rty, bukání sliznici, přední 2/3 jazyka, spodinu ústní, tvrdé patro, horní a dolní dáseň.
Hltan (farynx) je svělově vazivová trubice v rozsahu od spodiny lební to úrovně 6 krčního obratle, kde přechází v jícen. Dělí se na orofarynx, nasofarynx (epifarynx) a laryngofarynx (hypofarnyx). Oblast orofaryngu z onkologického hlediska zahrnuje přední stěnu (kořen jazyka a vallcerula epiglottica), boční stěnu (patorvá mandle, tonzila, fossa tonsillaris a patrové oblouky, patrové oblouky, dále zadní stěnu a horní stěnu (spodní plocha měkkého patra a uvula palatina). Oblast epifaryngu představuje horní část hltanu, která komunikuje s nosní dutinou, sestává ze stropu, zadní stěny, boční stěny a spodní stěny (horní plocha měkkého patra). Oblast hypofaryngu je spodní částí hltanu, sestává z přechodu hltanu v jícen (postkrikoidní oblast), piriformních sinů a zadní stěny hypofaryngu. V sousedství a v návaznosti na hltan se nachází hrtan (larynx), jehož funkce je spojena nejen s dýcháním, ale i s tvorbou hlasu. Kostra hrtanu je tvořena několika chrupavkami. Hrtan se skládá ze 3 anatomických oblastí: supraglottické, glottické a suglottické. Supraglottická oblast (vchodová část hrtanu) se nachází nad hlasivkami a obsahuje příklopku hrtanovou (epiglottis), aryepiglotické řasy, arytenoidní řasy a nepravé hlasové vazy. Část glotická představuje pravé hlasové vazy, mezi nimiž je hlasová štěrbina. Část subglotická se nachází pod hlasivkami a volně navazuje na průdušnici (tracheu).
Etiologie
Vznik karcinomů v oblasti hlavy a krku může být vyprovokován nejrůznějšími příčinami, nejvíce zde působí vlivy zevního prostředí. Převážná většina se vyskytuje u kuřáků cigaret (v tabákovém kouři je uváděno více než 40 karcinogenů). Časnější výskyt je prokázán při současném nadužívání tabáku a alkoholu. Alkoholu se zde přisuzuje role kokarcinogenu, to jest látky, která sama o sobě nemá schopnost vyvolat nádorový růst, avšak v přítomnosti látky která je schopna nádorový růst vyvolat, avšak v přítomnosti karcinogenů, dokonce i velmi slabého, vyvolává a podporuje vznik zhoubného novotvaru. Konzumace alkoholických nápojů navíc snižuje obranyschopnost organismu před karcinogenními látkami. Relativní riziko pro vznik karcinomu je u těžkých pijáků 2 až 6 x vyšší, při abusu tabáku je vyšší 5 až 25x. Karcinogenní účinek byl prokázán také u marihuany. Při vzniku nádorů hlavy a krku hrají roli i některé typy virů, zvláště HPV (lidský papilomavirus) ve vztahu k nádorům orofaryngu, který je v poslední době v centru pozornosti, dále genetická predispozice, karcinogenní látky v zaměstnání (nikl, chrom, olovo, azbest, fluor, arzén, uhlovodíky v sazích, dehtu a průmyslových olejích) a expozice na radiační záření. Může zde sehrát roli i nízká hygiena dutiny ústní a špatná výživa. Výskyt se zvyšuje se stoupajícím věkem, nádory v této oblasti jsou typické pro osoby starší 50 let. Dle randomizované studie stoupá incidence benigních i maligních nádorů parotis s počtem hovorových hodin mobilním telefonem až trojnásobně5.
Všeobecné příznaky
- Nádory hlavy a krku mohou zůstat dlouhou dobu bez klinických příznaků nebo napodobovat běžná zánětlivá onemocnění horních cest dýchacích.
- Nádory nosu se projevují zhoršenou nosní průchodností anebo výraznou sekrecí z nosu, především je-li s příměsí krve. Na nádor by měla upozornit i jednostrannost příznaků.
- Nádory vedlejších nosních dutin rostou velmi pomalu a často bezpříznakově.
- Nádory dutiny ústní a hltanu se projeví pocitem cizího tělesa v krku či ústech, krvácením ztíženým anebo bolestivým polykáním.
- Nádory hrtanu se liší příznaky dle primární lokalizace a dle pokročilosti onemocnění.
- Karcinom hlasivek se projevuje již v časných stádiích chrapotem, v ostatních lokalizacích dýchací trubice se většinou nádorové onemocnění zjistí až v pokročilejším stadiu, kdy se u nemocných může objevit pocit cizího tělesa v krku, vykašlávání krve, polykací či dýchací potíže.
- Nádory slinných žláz se zpočátku projevují jako nebolestivého zduření. Později v důsledku růstu nádoru do okolí dochází k bolestivosti a u příušní žlázy navíc i k obrně lícního nervu.
- Zduření na krku, ve většině případů nebolestivé, bývá projevem metastatického šíření nádorového onemocnění do spádových lymfatických uzlin anebo přímého prorůstání primárního nádoru.
Klinické příznaky onemocnění jsou různé. Klinické rozdíly mezi jednotlivými nádory nelze vysvětlit pouze jejich anatomickou lokalizací ale i biologickými rozdíly. Postižena může být v různých stupních řeč, polykání, čich, dýchání a jiné významné funkce, důležité pro kvalitu života a přežití. Na nádorové onemocnění dále nespecificky ukazují i některé celkové příznaky, jako úbytek tělesné váhy nebo zvýšená teplota.
Příznaky nádorů hlavy a krku dle lokalizace 4
| Nádory oblasti nosu, nosohltanu a vedlejších nosních dutin | huhňavost nosní neprůchodnost (zejména jednostranná) krvácení z nosu (zejména jednostranné) zápach z nosu porucha čichu bolest hlavy porucha sluchu (zejména jednostranná) bolesti uší (zejména jednostranná) zduření na krku zduření v obličeji obrny hlavových nervů dvojité vidění zhoršení zraku |
| Nádory v oblasti orofaryngu a hypofaryngu | bolesti v krku a uších pocit cizího tělesa bolestivost při polykání obtíže při polykání zápach z úst krvácení z dutiny ústní zduření na krku |
| Nádory hrtanu | chrapot dušnost pocit cizího tělesa bolesti v hrtanu polykací obtíže váhový úbytek zduření na krku |
| Nádory velkých slinných žláz | zduření v oblasti slinných žláz (příušní, podjazykové a čelistí) bolestivost v těchto krajinách parestézie nebo obrna lícního nervu |
| Nádory ucha | vleklý výtok z ucha často s příměsí krve, nedoslýchavost ušní šelest bolesti ucha závratě obrna lícního nervu |
Diagnóza
Nemocní s nádory oblasti hlavy a krku vyžadují přístup týmu, který se skládá z více lékařských odborností, především z otorinolaryngologů – chirurgů hlavy a krku, odborníků na záření, klinických onkologů, odborníků na zobrazovací diagnostiku a patologů. Účelná je také účast čelistního chirurga, plastického chirurga, ve vybraných případech i neurochirurga a oftalmologa.
Základem stanovení diagnózy je historie onemocnění, zaměřená na místní a celkové příznaky a rizikové faktory. Následuje klinické vyšetření. Řada nádorů je dobře přístupná vyšetření zrakem, pohmatem a přímými nebo nepřímými endoskopickými metodami. Ze všech zjištěných novotvarů je doporučeno vzít vzorek na histologické vyšetření. Mezi vyšetření vedoucí ke stanovení diagnózy a místního rozsahu onemocnění patří:
- Zobrazovací metody: rentgenový snímek, počítačová tomografie nebo zobrazení magnetickou rezonancí. Tato vyšetření přináší zásadní informace o hloubce a rozsahu nádorového postižení a o spádových lymfatických uzlinách.
- Sonografie krku umožní posoudit vztah rozsáhlého nádoru ke krční tepně a posoudit metastatické postižení krčních uzlin (cca u 50% pacientů s maligním nádorem hlavy a krku mohou nehmatné uzliny obsahovat metastázy).
- Zobrazení krčních tepen pomocí kontrastní látky.
- Vyšetření tělních dutin dýchacích a polykacích cest zrakem v celkové narkóze umožňuje upřesnění diagnózy vícečetných nádorů.
- Vyšetření vzorku nádorů pomocí mikroskopu (histologické vyšetření).
- V rámci ověřování vzdálených metastáz se provádí rentgenový snímek hrudníku, případně počítačová tomografie hrudníku, sonografie břicha nebo scintigrafie skeletu.
Zobrazovací metody u nádorů hlava/krk
Zobrazovací metody mají nezastupitelnou roli při identifikaci, stagingu a sledování nádorů hlavy a krku. V diagnostickém algoritmu se využívá velká většina, především moderních metod jako je výpočetní tomografie (CT), magnetická rezonance (MR) a hybridní metody jako PET-CT a PET-MR. Hybridní zobrazení pomocí PET indikujeme zvláště u pátrání po primárním nádoru u metastáz neznámého origa. Rovněž tuto metodu považujeme za indikovanou u nemocných s pokročilými operabilními nádory, u nichž by případná vzdálená metastáza byla kontraindikací rozsáhlého onkologického výkonu. Nelze však zapomínat ani na osvědčené metody jako rentgenový snímek a vyšetření ultrazvukové, jež jsou stále neopomenutelné. Oblast hlavy a krku je navíc anatomicky značně komplikovaná, což jen přispívá k nutnosti využít celou škálu zobrazovacích metod.
Rentgenový snímek nehraje sice zásadní roli, nicméně například sumační snímek hrudníku v rámci posouzení případného metastatického rozsevu do plic je stále využíván, a to především díky výborné dostupnosti i nízké radiační zátěži ve srovnání s CT. Rentgenové snímky samotné oblasti hlavy a krku hrají jen minimální roli, především u posuzování tumorózních postižení. I využití poloaxiální projekce k posouzení vedlejších dutin je dnes stále více nahrazováno CT a především MR vyšetřením.
Ultrazvukové vyšetření (UZ) má vysokou senzitivitu při identifikaci povrchové krční adenopatie, specificita je už nižší, nicméně existují možnosti odlišení uzliny reaktivně zvětšené od infiltrované patologickým procesem. Jednak je to již dlouhou dobu známý LT index posuzující tvar uzliny, a v poslední době pak čím dále více používané kontrastní látky pro UZ vyšetření, které velmi podrobně zobrazí typ vaskularizace uzliny, což může napomoci při diferenciální diagnostice jejího postižení.
CT vyšetření bylo do nedávné doby zlatým standardem stagingu tumorózních onemocnění hlavy a krku, je však stále více nahrazování MR vyšetřením a hybridními metodami (viz dále). CT je sice rychlé a relativně jednoduché vyšetření, musí však při něm být použita intravenózní jodová kontrastní látka a vyšetření samotné má nezanedbatelnou radiační zátěž. Navíc jeho citlivost pro odlišení patologické infiltrace v měkkých tkáních zdaleka nedosahuje schopností MR. Nadále je však používanou metodou, poněvadž může komplexně posoudit stadium T, stejně jako N.
má nejvyšší senzitivitu i specificitu pro posouzení měkkotkáňových expanzí, jak již bylo uvedeno výše. A není to jen nejlepší kontrastní rozlišení měkkých tkání, ale i využití speciálních metod, jako je zobrazení difúze, dynamické postkontrastní zobrazení a též MR spektroskopie, které mohou přinést další důležité informace o povaze léze. V neposlední řadě je nutné uvést absenci škodlivých vedlejších účinků u tohoto vyšetření.
V poslední době se stále více prosazuje užití hybridních metod. Jednak již plně zavedeného PRT-CT, ale nově i PET-MR, které má právě díky MR podstatně vyšší senzitivitu i specificitu při posuzování měkkotkáňových expanzí nejen v oblasti hlavy a krku. Jedná se sice o časově náročné vyšetření, jeho význam je však nesporný.
Stadia onemocnění a vztah k volbě léčby
Stadium onemocnění je nejdůležitějším faktorem pro výběr léčebného postupu a předpověď přežití. Základem je klasifikace dle AJCC (American Point Committee on Cancer). Rozsah primárního nádoru (staging) je rozhodujícím faktorem pro další postup a prognózu.
T Stadium I T1 N0 M0
Stadium II T2 N0 M0
Stadium III T3 N0 M0 a T 1-3 s N1s
Stadium IV T4 N0 – N2,N3
N NX regionální uzliny nemohou být určeny
N0 bez známek regionálních uzlin
N1 metastáza do jedné ipsilaterální lymfatické uzliny, menší než 6 cm
N2 N2a jedna ipsilaterální uzlina, 3 až 6 cm
N2b mnohočetné ipsilaterální lymfatické uzliny menší než 6 cm
N2c bilaterální nebo kontralaterální lymfatické uzliny menší než 6 cm
B3 lymfatické uzliny větší než 6 cm
M M0 absence vzdálených metastáz
M1 přítomnost vzdálených metastáz.
V posledním, osmém vydání TNM klasifikace zhoubných novotvarů (česká verze 2017), jsou nádory orofaryngu nově klasifikovány ve 2 skupinách – jako nádory p16 negativní (nebo orofaryngeální karcinomy bez provedené p16 imunohistochemie) a nádory p16 pozitivní. Změny se promítají jak do T, tak N klasifikace – podrobnosti viz James D. Brierley, Mary K. Gospodarowicz a Christin Wittekind: TNM klasifikace zhoubných novotvarů, 8.vydání
Tato změněná klasifikace poněkud „změkčuje“ kritéria pro TNM klasifikaci u p16 pozitivních nádorů vzhledem k jejich výrazně lepší prognóze.
Pětileté přežití nemocných s nádory oblasti hlava/krk dle stadií:
| Stadium | Pětileté přežití % |
| I | 91% |
| II | 77% |
| III | 32% |
| IVa | 25% |
| IVb | 4% |
Léčba
Jakmile byla ověřena diagnóza histologicky a určen rozsah nádoru, výběr optimální léčby odvisí od řady faktorů, včetně jeho lokalizace, tělesného stav i nemocného, zvážení možných vedlejších projevů plánované léčby a také i na přání nemocného. Léčebné možnosti jsou:
| Standardní léčebné postupy | |
| Chirurgie (+ předoperační nebo pooperační radioterapie nebo chemoradioterapie). | |
| Radioterapie (+ chemoterapie) | |
| Paliativní radioterapie nebo chemoterapie | |
| Biologická terapie | |
| Immunoterapie | |
| Další možnosti | |
| úvodní chemoterapie, podaná před chirurgickým zákrokem a radioterapií | |
| chemoprevence | |
Chirurgie
Chirurgické odstranění nádoru má u většiny nádorů v oblasti hlavy a krku prvořadý význam. Asi u 40% nemocných vystačíme se samotnou operací nebo radioterapií s léčebných záměrem. U zbylých 60% nemocných je třeba použít léčbu kombinovanou – kombinují se vzájemně chirurgie, radioterapie a chemoterapie, v některých případech lze využít i tzv biologické terapie. Podání pomocné léčby (radioterapie, chemoterapie nebo chemoradioterapie) může být ve vztahu k hlavní léčebné modalitě neoadjuvantní (tj. předcházející, konkomitantní (tj. současné), či adjuvantní (tj. následné). Oblast hlavy a krku je většinou dobře přístupná pro radioterapii, která se může pro zvýšení účinku kombinovat s chemoterapií. V některých případech, v závislosti na lokalizaci nádorů hlavy a krku, bývá nutno provést dočasnou či trvalou tracheotomii ( tj. vyústění dýchací trubice v oblasti krku), která zajistí dýchání. Tracheostomie se provádí jako součást onkologické léčby anebo u neoperabilních onemocnění, kde nádor významně zužuje dýchací cesty. Před (chemo) radioterapií se přistupuje k provedení perkutánní endoskopické gastrostomii (PEG), zajišťující výživu nemocného během léčby. Úbytek tělesné váhy u onkologických pacientů bývá způsoben nejen základním onemocněním, ale i v důsledku samotné terapie (pooperační období, chemoterapie spojená s nevolností, zvracením a průjmy, radioterapie spojená s bolestivým a ztíženým polykáním v důsledku poškození sliznic polykacích cest).
Chirurgická léčba
Chirurgická léčba je základem léčby nejméně dvou třetin případů všech nádorů oblasti hlavy a krku. Účinnost této léčby klesá s pokročilostí onemocnění. Chirurgická léčba umožňuje odstranit primární nádor, radikálně ošetřit spádový lymfatický systém a zrekonstruovat operovanou krajinu. Chirurgickou léčbu považujeme za léčbu poskytují nejvyšší procento uzdravení za předpokladu, že jsme schopni odstranit celý nádor s dostatečně širokým bezpečnostním okrajem při zachování funkčně důležitých, nádorovým procesem nepostižených tkání. Předpokladem splnění tohoto požadavku jen vysoká chirurgická zkušenost operatéra a ošetřujícího personálu. Aby byla možnost nádor bezpečně odstranit, je nutno použít takový přístup, kdy jsou dobře patné hranice nádoru, je zabezpečena kontrola krvácení a šetřeny důležité okolní struktury současně s dobrým estetickým účinkem. Kromě primárního nádorového ložiska se současně odstraňuje i spádová lymfatická oblast, pokud je u pacienta prokázáno regionální metastatické postižení, anebo pokud existuje předpoklad výskytu subklinických ( tj. klinicky nezjištěných) metastáz. Při nepříznivém kosmetickém efektu onkologických operací je třeba rekonstrukce operované krajiny pomocí plastické chirurgie.
S bouřlivým rozvojem techniky souvisí zavedení některých metod, jako jsou moderní zobrazovací metody, kvalitní mikroskopická technika nebo počítačem navigované operace. Došlo také k pokroku v jiných medicínských oborech, například v anestesiologii, což umožňuje provádět mnohahodinové operace s minimálními nežádoucími účinky. Další možnosti zlepšení chirurgické léčby jsou na rozdíl od konzervativní onkologické léčby téměř vyčerpány, chirurgická léčba se tak dostává k hranicím možností a zdá se, že již příliš nepřispěje ke zlepšení statistiky přežití nemocných.
K nejvíce diskutovaným otázkám v chirurgické léčbě solidních nádorů hlavy a krku patří radikalita chirurgických postupů versus kvalita života, otázka rekonstrukce pooperačních defektů, volba správného přístupu a otázka ošetření oblastních metastáz.
Určitým trendem je opouštění rozsáhlých výkonů ve prospěch funkčně a kosmeticky příznivějšího řešení (šetření orgánů) zajištěného radioterapií a/nebo chemoterapií.
Chirurgická léčba karcinomu nosu a vedlejších dutin nosních
Cílem chirurgické léčby vedlejších nosních dutin je odstranit nádor, zajistit drenáž postižené dutiny do dutiny nosní a při výrazném funkčním či kosmetickém defektu i zrekonstruovat operovanou krajinu. Endoskopický přístup je používán na většině pracovišť ve stále větším rozsahu. Odstranění krčních uzlin je vzhledem k poměrně malému riziku rozsevu do uzlin (přibližně 20 % všech případů karcinomů vedlejších nosních dutin) doporučováno jen u pacientů s pozitivními uzlinami. Pro nádory vyššího stadia je doporučeno následné ozáření. Pro nádory, které nejsou chirurgicky řešitelné lze použit kombinaci chemoterapie a záření.
Chirurgická léčba karcinomu dutiny ústní
Léčba je daná rozsahem nádoru, jeho lokalizací a postižením uzlin. Řešení je ve většině případů chirurgické. Chemoterapie je reservována pro místně pokročilé, neoperabilní, metastazující nebo recidivující onemocnění.
Chirurgická léčba nádorů orofaryngu
Orofarynx představuje bazi jazyka, tonzily, měkké patro a zadní část faryngální stěny. 15 až 75% nemocných má postižené regionální uzliny. Léčba je chirurgická s následným zářením.
Chirurgická léčba karcinomu hrtanu
Karcinom hrtanu patří prognosticky k příznivějším lokalizacím rakoviny hlavy a krku. Je to dáno skutečností, že většina nádorů hrtanu zůstává v časných stadiích omezena v prostorách ohraničených vazivovými membránami hrtanu a rakovina hlasivek navíc metastazuje poměrně málo často. Tato skutečnost umožňuje u méně pokročilých forem karcinomu hrtanu částečné odstranění hrtanu s dobrými funkčními výsledky – nemocní jsou většinou schopni adaptace na nové anatomické poměry a mohou dýchat, polykat a mluvit. Částečné výkony na hrtanu nejsou indikovány u celkově oslabených nemocných se špatnou plicní funkcí. Kvalita života těchto nemocných může být uspokojivější po úplném odstranění hrtanu než po funkčně neúspěšné částečné resekci hrtanu, komplikované možností vdechnutím jídla nebo slin.
Karcinom vchodové části hrtanu
Hlavním principem je radikální odstranění nádorem postižené části hrtanu, přičemž je odstraněna horní polovina štítné chrupavky spolu s přilehlými měkkými tkáněmi. Je zachována pohyblivost hlasivek (hlas) a zabezpečena možnost hlasivkového uzávěru při polykání jako ochrana proti aspiraci. V různě dlouhém pooperačním období může být přechodně snížená kvalita života právě pro zaskakování potravy do dýchacích cest. Již u malých supraglotických nádorů je vysoké riziko uzlinových metastáz, proto je i u klinicky negativního nálezu na krku indikována selektivní odstranění uzlin a/nebo pooperační radioterapie. Při zjištění postižení uzlin je indikováno chirurgické odstranění uzlin a pooperační radioterapie.
Karcinom hlasivek
Částečné odstranění hrtanu je indikováno pro T1 – T2 nádory hlasivky. Nádory větší než 2 cm jsou většinou indikovány k úplnému odstranění hrtanu. Úplné odstranění hrtanu umožňuje léčbu pokročilejších nádorů. Odstraněním celého orgánu je většinou splněna podmínka dostatečné chirurgické radikality, ovšem, za cenu obětování funkce hrtanu. Výsledkem operace je trvalé oddělení dýchacích a polykacích cest, pacient dýchá přímo průdušnicí vyústěnou v hrdelní jamce a dolní část hltanu přechází volně v místě spodního hltanového svěrače v jícen. Ochrannou funkci hrtanu lze částečně nahradit různými typy filtrů, například tzv. HME filtr částečně filtruje prachové látky a zároveň zvlhčuje vdechovaný vzduch do průdušnice. Hlas lze rehabilitovat pomocí jícnového hlasu, event. hlasové protézy, při neúspěchu lze použít elektrolarynx. Jícnový hlas spočívá v nabírání vzduchu o dostatečném objemu do jícnu a jeho zpětném vypuzování přes hltan a dutinu ústní. V místě přechodu hltanu v jícen dochází k rozkmitání sliznice a podslizniční vrstvy, při kterém vzniká vlastní jícnový hlas. Tímto způsobem komunikuje v praxi asi 20-30 % pacientů po totálním odstraněním hrtanu. Při tvorbě hlasu pomocí tzv. hlasové protézy se nasává z dýchacích cest umělým spojením průdušnice s jícnem, které je opatřeno jednocestným ventilem a hlas je opět tvořen v oblasti ezofaryngohypofaryngeálního svěrače (tzv. pseudoglottis). V tomto případě se naučí hovořit asi 80% pacientů. Elektrolarynx je elektromechanický převodník, tvořící pomocí oscilátoru vibrace, které rozechvívají prostor hltanu a dutiny ústní a umožní tak artikulaci.
Rakovina subglottis
Rakovina hrtanu v dolní části je poměrně vzácná, onemocnění bývá dlouho bez příznaků a většinou bývá diagnostikováno až v pokročilém stadiu. Základní léčebnou metodou rakoviny této lokalizace je kombinace úplného odstranění hrtanu s následnou radioterapií. Prognosticky patří subglottická lokalizace karcinomu hrtanu k nejméně příznivým.
Chirurgická léčba karcinomu slinných žláz
Léčba karcinomů slinných žláz je radikálně chirurgická. V oblasti podčelistní slinné žlázy se odstraní nádor spolu se žlázou a dolní čelistí, je-li postižena. Je indikována i odstranění lymfatických uzlin. U rakoviny příušní slinné žlázy je prováděno úplné odstranění nádoru, eventuálně s přilehlou čelistí. Vzhledem k obavě z šíření nádoru podél nervů je indikováno odstranění lícního nervu s možností jeho náhrady periferním nervem v jedné operační době. Při postižení spádových lymfatických uzlin se provádí chirurgické odstranění lymfatických uzlin. U nádorů příušní slinné žlázy s vyšším stupněm malignity je indikována chirurgická léčba lymfatických uzlin i v případě negativního klinického nálezu na uzlinách.
Chirurgická léčba karcinomu ucha
Prognóza rakoviny ucha je lepší u formy povrchní než u hluboce vrůstající formy. Chirurgická léčba spočívá v klínové excizi nebo totální amputaci boltce s odstraněním spádových lymfatických uzlin, jsou-li postiženy. Amputovaný boltec je možné nahradit plastikou nebo protézou.
„Záchovný protokol“
Současná medicína klade stále více důraz na kvalitu života nemocných, proto se zavádí tzv. záchovný protokol. Cílem tohoto léčebného postupu je ušetření orgánu a tím i jeho funkce. Uplatnění záchovného protokolu je indikováno u nemocných s místně pokročilým nádorem, který by ještě bylo možné operovat. Chirurgická léčba je zcela vynechána nebo alespoň prováděna v minimálním rozsahu. Toto šetření orgánů nesmí být na úkor délky přežití nemocných.
Záchovný protokol nelze použít u všech nemocných s karcinomem hlavy a krku, pouze ve velmi pečlivě vybraných případech. Použití záchovného protokolu je indikováno zvláště u laryngofaryngeálních nádorů (zachování hrtanu) a u karcinomu předních 2/3 i kořene jazyka (zachování jazyka). Při uplatnění záchovného protokolu u laryngeálního a hypofaryngeálního nádoru je šetřen hrtan. Nemocnému zůstává zachována funkce řeči, dýchání i polykání. Záchovný protokol je zvlášť výhodný, je-li nádor převážně v hypofaryngu – při chirurgické léčbě by bylo nutné obětovat i funkčně normální hrtan. K dalším výhodám patří i možnost použití chirurgické léčby v případě recidivy onemocnění a pozitivní vliv na psychologii nemocných.
K nevýhodám záchovného protokolu patří zvýšená toxicita, vedlejší účinky léčby se sčítají a to bez prodloužení života. Řada nemocných s karcinomy hlavy a krku také mají závažné přidružené choroby, které neumožňují podání konkomitantní chemoradioterapie. Je nutno také zvážit, že chirurgická léčba má sice jasně negativní vliv na kvalitu života, ale je schopna kontrolovat nemoc až do nadklíčku ve velké většině případů spolehlivěji.
Použití záchovného protokolu má svá omezení. Pravděpodobnost, že budeme nuceni obětovat funkci orgánu při snaze o dosažení lokální kontroly nad nádorem vzrůstá se zvětšujícím se objemem nádoru. Při nárůstu toxicity léčby u nemocných s laryngofaryngeálním karcinomem stoupá podíl nemocných vyžadujících trvale vyživovací sondu. Při rozhodování o způsobu léčby by měla být zvolena léčba, která nabízí nejlepší dobu celkového přežití a také nejlepší možnou kvalitu života (zachování orgánu a jeho funkce). Pro rozhodování o zařazení nemocných do záchovného protokolu nebyla dosud nalezena spolehlivá kriteria. Z klinického hlediska nejsou považováni za vhodné kandidáty pro záchovný protokol nemocní s příliš pokročilým nádorem|(např. průnik nádoru chrupavkou). V budoucnu budou zřejmě při indikaci záchovného protokolu hrát významnou roli biologické markery. Při rozhodování o zařazení do záchovného protokolu je třeba také respektovat přání samotného nemocného. Po léčbě v rámci záchovného protokolu je nutná kvalitní rehabilitační péče o polykání, výživu, řeč a eliminace kouření.
Radioterapie
Radioterapie patří mezi základní léčebné modality v léčbě nádorů hlavy a krku. Rozvoj radioterapie v posledních desetiletích umožnil změnit postavení radioterapie v léčebné strategii karcinomů hlavy a krku a zařadit ji po boku chirurgie ke kurativním metodám léčby. U časných stadií onemocnění je radioterapie rovnocennou alternativou chirurgického výkonu a výběr léčebné modality závisí na funkčním výsledku zvolené modality a preferencích pacienta. U lokálně pokročilého onemocnění může radioterapie následovat po chirurgickém výkonu nebo v případě inoperabilního onemocnění či orgán (larynx) zachovávajícího postupu představovat nosnou léčebnou modalitu.
Zlepšení léčebných výsledků nádorů hlavy a krku bylo dosaženo intenzifikací léčby a to jednak úpravou frakcionačních režimů radioterapie tzv. alternativní frakcionační režimy nebo kombinací radioterapie s dalšími léčebnými modalitami - konkomitantní chemoterapií či biologickou léčbou. Alternativní frakcionace má dva hlavní směry - hyperfrakcionaci a akceleraci. Při hyperfrakcionaci jsou nejčastěji aplikovány 2 frakce denně sníženou dávkou na frakci. Hyperfrakcionace umožní aplikovat celkovou dávku o 10-15% vyšší bez navýšení pozdní toxicity. Při akcelerované frakcionaci je zkrácen celý kurz radioterapie. Stejná léčebná dávka je aplikována za kratší časový úsek a tím se předchází nežádoucí repopulaci klonogenních nádorových buněk během ozařovacího cyklu. Některé studie kombinují oba postupy, důsledkem však je významné navýšení akutní toxicity ve srovnání se standardní frakcionací. Z aplikace alternativních režimů profitují především mladší pacienti, stejně tak i z kombinované léčby. Z hlediska vlastní choroby má alternativní frakcionace největší léčebný efekt na primární nádor, menší účinek na regionální uzliny a neovlivní výskyt vzdálených metastáz24.
Ke zkvalitnění radioterapie přispěl vývoj nových technologií vysokoenergetických zdrojů ionizujícího záření - lineárních urychlovačů, rozsáhlá digitalizace, vývoj počítačů, plánovacích systémů a vývoj zobrazovacích metod. Třídimenzionální zobrazovací metody jako počítačová tomografie, magnetická rezonance a pozitronová emisní tomografie umožnily zpřesnit lokalizaci a rozsah nádorového postižení, jeho vztah k rizikovým strukturám. Moderní plánovací systémy umožňují fúzi těchto zobrazovacích metod s plánovacím CT vyšetřením. Předpokladem je provedení zobrazovacího vyšetření v poloze, ve které bude pacient ozařován. Nové technologie umožňují však i fúzi diagnostického vyšetření po jeho předchozí softwarové úpravě do ozařovací polohy pacienta. Vývoj zobrazovacích metod směřuje k využití morfologického i funkčního zobrazení k plánování cílené dávkové distribuce - navýšení dávky do hypoxických, radiorezistentních oblastí.
Pokrok v radioterapii umožnil přechod od konvenční radioterapie k radioterapii konformní. Konvenční radioterapie nádorů hlavy a krku používala techniku postupně zmenšujících se polí (shrinking field technique) k dodání dávky do zvoleného objemu a současně šetření zdravých tkání. Třídimenzionální konformní radioterapie ( 3D -CRT) přizpůsobuje ozařovaný objem nepravidelnému trojrozměrnému tvaru cílového objemu a tím šetří okolní zdravé tkáně. Vyspělejší formou 3D-konformní radioterapie je radioterapie s modulovanou intenzitou IMRT (intensity-modulated radiation therapy). Tato technika dosáhla klinického využití hlavně v posledních 10 až 15 letech a stala se standardní metodou v radioterapii nádorů hlavy a krku. IMRT umožňuje konformní ozáření a navíc možnost cílené nehomogenní distribuce dávky v ozařovaném objemu. Nehomogenní distribuce dávky v cílovém objemu je dosaženo svazky záření, které nemají v celém svém objemu stejnou intenzitu záření. IMRT technika šetřením zdravých tkání umožňuje navýšení léčebné dávky a tím dosažení vyšší lokální kontroly choroby při stejné nebo nižší morbiditě. Relativní nevýhodou provedení IMRT techniky je její časová náročnost a zatížení většího objemu zdravých tkání nízkou dávkou záření, což je především významné u dětských pacientů, kdy narůstá riziko sekundárních malignit25. U nádorů hlavy a krku IMRT technika umožnuje šetřit velké slinné žlázy a snižuje tak poradiční xerostomii bez vlivu na lokální kontrolu choroby i celkové přežití ve srovnání s konvenční radioterapií, což potvrdila i studie fáze III - PARSPORT26.
Nejnovější generace lineárních urychlovačů umožňují ozařování technikou IMAT ( intensity- modulated arc therapy). Jde o kombinaci klasické IMRT techniky a pohybové terapie. Vysoce konformního ozáření je zde dosaženo kombinací užití mnoholistového kolimátoru, rychlostí rotace ozařovací hlavice a dávkovým příkonem. Tyto techniky pod komerčními názvy RapidARC ,VMAT (volumetric-modulated arc therapy) mají výhodu ve zkrácení léčebných časů, navýšení kapacity počtu ozářených pacientů a snížení radiační zátěže pacienta. Podmínkou zvyšování konformity radioterapie je však zajištění přesnosti radioterapie. K přesnosti radioterapie přispívají zobrazovací metody v průběhu ozařování ( IGRT – image - guided radiotherapy). Přídatná zobrazovací zařízení pro 2D nebo 3D zobrazení jsou umístěna přímo na ozařovači. Tyto zobrazovací systémy vyhodnocující chybu v polohování před a nebo v průběhu ozáření, umožní srovnání aktuálního zobrazení s referenčním zobrazením získaným při plánování radioterapie. Dle závažnosti je případná odchylka korigována (od posunu ozařovacího stolu až po nové plánování).
Nové technologie v radioterapii umožnily zavedení čtvrtého rozměru - času - do radioterapie. Moderní technologie umožňují synchronizovat ozáření s pohybujícím se cílovým objemem (pohyb cílového objemu během frakce, mezi jednotlivými frakcemi, fyziologické pohyby orgánů v průběhu ozáření) - tzv. 4D radioterapie.
Dávková distribuce v cílovém objemu je naplánována podle zobrazovacích vyšetření provedených před zahájením radioterapie a zpravidla je použita po celou dobu radioterapie. V průběhu radioterapie se však mohou významně měnit poměry v cílovém objemu, může dojít k regresi nádoru, stejně tak může docházet ke změnám okolní tkáně z důvodu např. reakce tkáně na ozáření (otok) nebo váhového úbytku pacienta.
Adaptivní RT - ART umožňuje vyhodnotit a upravit dávkovou distribuci v cílovém objemu dle aktuálních poměrů. Umožňuje ověřit dodanou dávku záření do cílového objemu a porovnat ji s dávkou naplánovanou a upravit aktuálně denní dávku k zajištění aplikace naplánované dávkové distribuce.
Léčba protony umožňuje vysoce konformní dávkovou distribuci s efektním šetřením okolních zdravých tkání. Dozimetrická výhoda protonů umožňuje eskalaci dávky v cílovém objemu a úpravu frakcionace ve smyslu zkrácení léčby. Z indikací pro léčbu protony jsou vhodné např. sinonasální karcinomy, nádory v oblasti baze lební z důvodu především šetření okolních zdravých tkání.
Cílem moderní radioterapie je zlepšení léčebných výsledků za přijatelné toxicity. Léčebný výsledek radioterapie je přímo závislý na kvalitě jejího provedení. Provedení kvalitní radioterapie vyžaduje odpovídající přístrojové vybavení, erudovaný personál a dostatečnou časovou kapacitu. Nezbytnou podmínkou úspěšného provedení a dokončení radioterapie je i úzká mezioborová spolupráce.
Chemoterapie
Před rokem 1980 byla chemoterapie karcinomů oblasti hlava/krk omezena na paliativní podání u nemocných v pokročilém stadiu onemocnění. Dnes je chemoterapie součást multimodální terapie jak u místně pokročilého, tak recidivujícího, metastatického onemocnění. Záměrem systémové léčby nádorů oblasti hlava/krk je maximalizovat kontrolu místně pokročilých nádorů, eradikovat okultní metastázy nebo zmenšit, byť dočasně nádorovou nálož. Léčebný plán musí být založen na znalostech možného přínosu a toxicity zvoleného postupu. Použití cytostatické léčby je dnes indikováno v následujících indikacích.
- Místně pokročilé onemocnění. Operabilní onemocnění, chirurgie následovaná pooperační radioterapií nebo chemoradioterapií pro pacienty vysokého rizika. Neresekabilní onemocnění, v kombinaci s radioterapií, s nebo bez cytostatické indukce je standardem.
- Recidivující, metastatické onemocnění se záměrem zmírnění symptomů a prodloužení života, v kombinaci s radioterapií.
- Záchovný protokol, záměr možnosti zachování orgánu, především laryngu, v kombinaci s radioterapií, s nebo bez indukční chemoterapie.
Pro léčbu cytostatiky je důležitá analýza celkového stavu nemocného, stav výživy, místo výskytu nádoru a jeho rozsah. Nejvíce používaná cytostatika jsou deriváty platiny, samotné nebo v kombinaci s 5-fluorouracilem a taxany. U pokročilých forem je někdy doporučen metotrexát, gemcitabin nebo hydroxyurea. Kombinace s radioterapií zvyšuje místní kontrolu a má přínos pro přežití proti radioterapii samotné.
Je diskutována účelnost indukční chemoterapie, tedy podání cytostatik před definitivní chirurgickou nebo radiační terapií. Je to strategie ke zmenšení lokálně pokročilých nádorů s významnou prognostickou rolí. Racionálnost tohoto postupu spočívá v lepším přísunu účinné látky do nepoškozeného terénu, lepší celkový stav pacienta, časná eradikace metastáz a především možnost zachování orgánu. Zatím co výsledky prvních studií byly nadějné, výsledky velkých randomizovaných studií pozitivní výsledky nepřinesly. Indukční chemoterapie proto zůstává postupem investigativním, pouze pro vybrané případy. Použití chemoterapie u pokročilého metastatického onemocnění je většinou neefektivná a toxické. V poslední době byl zaznamenán pokrok při použití vhodných kombinací v paliativní léčbě, i pro účinnou paliativní léčbu druhé liniue. V první linii se osvědčila kombinace platinového derivátu s fluorouracilem a nivolumabem, v druhé linii imunoterapie – nivolumab a pembrozulimab.
Biologická (cílená) terapie
Ve snaze zlepšit léčebné výsledky se v posledních letech zaměřuje pozornost na molekulární biologii nádorů hlavy a krku. Cílem specifické molekulárně cílené terapie je vytvořit látku, která selektivně postihne nádorové buňky. Záměrem je zasáhnout specifické molekulární faktory, dráhy signální soustavy, které jsou zapojeny do nádorového růstu6. Metabolická cesta receptoru pro epidermální růstový faktor je u nádorů hlava/krk abnormálně aktivovaná. Tento receptor hraje klíčovou roli v kancerogenezi, jeho signální cesta vede k aktivaci buněčného dělení, inhibici apoptózy, angiogenezi, metastázování a aktivní proliferaci nádorových buněk. Přínos se očekává ve zlepšení léčebného účinku a ve snížení toxicity, která je spojená s cytostatiky. Klinickým zkoušením prošla celá řada látek, účinnost v léčbě karcinomů hlavy/krku, jak forem místně pokročilých nebo metastatických prokázal v kombinaci s radioterapií pouze cetuximab. Cetuximab je chimérická protilátka, která se váže a inhibuje EGFR (receptor epidermálního růstového faktoru). Který byl schválen v březnu 2006 FDA pro kombinaci s radioterapií pro léčbu nádorů hlavy a krku nebo v monoterapii u nemocných již dříve léčených cisplatinou.7,8,9
Lidský papilomavirus (HPV)
Nádory oblasti hlavy a krku jsou spojovány tradičně s kouřením a alkoholem. V posledních letech přibylo údajů o vzestupu incidence nádorů, které jsou ve spojitosti s lidským papilomavirem.10, 11,12 Lidský papilomavirus se v lidské populaci vyskytuje běžně, ale pouze u malé skupiny infikovaných osob dojde k vývoji karcinomu. Je známých více jak 150 různých podtypů, představuje vysoce rizikový HPV16 90% virů izolovaných u HPV pozitivních nádorů hlavy a krku. HPV je DNA virus, který způsobuje onkogenní transformaci hostitelské buňky. HPV pozitivní nádory hlavy a krku představují novou, rozdílnou podskupinu nádorů hlavy a krku. Dle posledních údajů je prevalence nádorů orofaryngu ve spojení s HPV v Evropě asi 40%. Lassenová uvádí, že v letech 1977 až 2012 došlo 12násobnému zvýšení výskytu karcinomů orofaryngu, když podíl HPV pozitivních nádorů se zvýšil ze 17% na 74%. 13 Typický profil nemocného s orofaryngeálním karcinomem se během posledních 20 let výrazně změnil. V minulosti toto onemocnění postihovalo převážně starší osoby, kuřáky a alkoholiky. Jejich onemocnění bylo typicky HPV negativní. Dnes osoby s nádorem orofaryngu jsou mladší, vzdělaní, dobrého tělesného stavu a sociálního postavení a často bez rizikových faktorů jako kouření a alkohol. HPV pozitivní nádory jsou diagnostikovány preferenčně v orofaryngu. Překvapivou charakteristikou HPV pozitivního onemocnění jsou velké uzliny, při relativně malém nálezu primárního nádoru, tito nemocní jsou často v době stanovení diagnózy v klinicky pokročilém stavu onemocnění. HPV pozitivní nádory hlavy a krku mají lepší prognózu ve srovnání s nádory HPV negativními, lépe reagují na chemoterapii a radioterapii. HPV pozitivní nádory mají ve srovnání s nádory HPV negativními 60-80% redukci rizika úmrtí. Tato pozorování jsou důkazem pro odlišný karcinogenní proces a nádorovou biologii lokalizovaných HPV pozitivních nádorů. Pssyriová vysvětluje, HPV indukovaná karcinogeneza má výrazně méně genetických alterací/mutací než karcinogeneza nezávislá na HPV (tabák, alkohol).14 Významným faktorem je skutečnost, že se jedná většinou o mladší pacienty v dobrém stavu, bez závažných komorbidit.
Průkaz HPV má závažný dopad pro kliniku.15 Z hlediska lepších léčebných výsledků HPV pozitivních nádorů při použití standardní chemoradioterapie s cisplatinou, je účelné zvážit deintezifikaci, méně intenzivní režim, který zmenší akutní a pozdní toxicitu, při zachování současných léčebných výsledků. Uvažuje se o snížení radiační dávky, substituci cisplatiny za cetuximab, který má nejméně stejný účinek při jiné, řešitelné toxicitě. Dobrá prognóza pacientů s nádory hlava/krk, HPV pozitivních je omezená na pacienty s orofaryngem. V roce 2014 byly uvedeny překvapující výsledky několika studií (/DAHANCA, Vermorken a Pogorzelski.16,10 V těchto studiích bylo zjištěno, že pokud se zaměříme na nádory vyrůstající z orofaryngu, není rozdílů v termínech lokoregionální kontroly mezi HPV+ a HPV-. Stav HPV má sice prognostický význam, ale nepomůže v predikci odpovědi na léčbu. Podporuje tak v rámci deintenzifikace podání cetuximabu bez ohledu na stav HPV. Zjištění bude mít zřejmě dopad na další léčbu HPV pozitivních nádorů oblasti hlava/krk a mohlo by vést ke změně současné praxe. U pokročilých a metastatických karcinomů hlavy a krku nemá stav HPV jasný klinický závěr. Výsledky Vermorkenovy studie podporují klinickou aplikaci cetuximabu, nezávisle na stavu nádorového HPV.
V systémové terapii karcinomů hlavy/krku dochází tak ke zlomové situaci, odklon od tradičních postupů a hledání nových cest, především překonání resistence a markerů pro výběr pacientů s možnou sensitivitou na cetuximab. Identifikace prognostických a prediktivních markerů pro strategii individuální léčby je hlavním cílem systémové léčby
Imunoterapie
Myšlenka použít imunní systém k útoku na nádor je stará více jak století. Trvalo dlouhá léta než se imunoterapie stala účinnou léčbou pro některé lidské nádory. Byl to maligní melanom, u kterého byly dosaženy zajímavé výsledky i když nedostatečné interleukinem2, BCG a interferonem. V průběhu posledních několika let bylo imunoterapií dosaženo dříve neuvěřitelných výsledků u řady dalších solidních nádorů.
Koncepce imunoterapie je prostá: uvolnit tělesný imunní systém k útoku na karcinom. Jsou zkoumány dva přístupy. První využívá přirozené imunní odpovědi organismu na nádor a druhá pomáhá imunnímu systému nalézt a ničit nádorové buňky. Inhibitory kontrolních bodů imunitní reakce uvolňují nádorem produkované brzdy imunního systému a zastavuj růst maligních nádorů.
Před 5 pěti lety byl uveden ipilimubab jako první látka schopná prodloužit život u pacientů s pokročilým melanomem, posléze u dalších nádorů.17 Dnes jsou nové efektivnější postupy namířené proti PD-1 (programmed death-1) a PDS-L1 (programed death ligand s menším počtem vedlejších nežádoucích účinků.18
Gillisonová komentuje imunoterapii u pokročilých nádorů hlavy a krku. Od uvedení cetuximabu před 10, lety nebyla pro tyto pacienty uvedena nová účinná látka. Je to poprvé, kdy léčebný postup zlepšil přežití u refrakterního onemocnění. Problematikou imunoterapie u nádorů hlavy a krku se u nás zabývají Klozar a Vošmík.
Léčebné protokoly
Je skutečností, že léčebné postupy se často liší. Základní strategie pro definitivní léčbu však je však všeobecně akceptována.
- Stadium I – II (dutina ústní, farynx a larynx)
Primární léčba orofaryngeálního karcinomu je chirurgická resekce nebo definitivní radioterapie. Chirurgickému řešení je dávána přednost, vyjma některých pacientů s časným nádorem rtu, retromolárnáho trigona a karcinomu měkkého patra.
Radioterapii je dávána přednost pro pacienty, kteří by nebyli schopni tolerovat radioterapii.
- Stadium III-IVB (lokálně pokročilé onemocnění dutiny ústní, faryngu a laryngu).
Pro lokálně pokročilé onemocnění lze zvážit chirurgii, pro pacienty, kteří nemohou být kandidáti chirurgie, jsou kandidáti definitivní radioterapie, chemoradioterapie, nebo indukční terapie.
Konkurentní chemoradioterapie je současným standardem pro pacienty s lokálně pokročilým karcinomem oblasti hlava/krk.
Rozhodnutí, zda léčit pacienta konkurentní chemoradioterpií, nebo pouze chirurgií nebo chemoterapií musí rozhodnout odpovědná komise.
- Stadium IVC
Metastatické nebo recidivujícící onemocnění dutiny ústní, faryngu a laryngu. Léčebná doporučení obsahují chemoterapii v monoterapii nebo kombinacích. Vhodné jsou kombinace s cisplatinou, pokud mohou být pacientem tolerovány, pokud ne, pak pouze monoterapie. Standardním nejúčinnějším režimem pro léčbu první linie je kombinace platinového derivátu s cetuximabem, a 5-fluorouracilem, s udržovací léčbou cetuximabem až do progrese, dle Vermorkenovy studie EXTREME.19. Chemoterapii druhé řady lze použít po progresi nebo recidivě pro terapii první řady. U pacientů v dobrém klinickém stavu bez autoimunních interkurencí lze zvážit použití nivolumabu. Další možností jsou taxany nebo metotrexat.
Prognóza nádorů oblasti hlava krk
Lokalizace primárního nádoru ovlivňuje časný vznik příznaků a tím včasnou diagnózu, což ovlivňuje prognózu a tedy i možnost radikálního chirurgického řešení. Prognóza je horší vzestupným gradientem směrem od rtů přes dutinu ústní do hltanu. Významnější pro prognózu je však rozsah primárního nádoru v době stanovení diagnózy. Např. malý nádor v oblasti, hlasivek a rtů má 5-leté přežití až u 80% nemocných. Pokročilé nádory však mají prognózu velmi špatnou, 5-leté přežití u nich nepřesahuje 10 – 15%. Druhotné nádory jsou popisovány v oblasti hlavy a krku asi v 40% u nemocných léčených pro první karcinom, kteří nepřestali kouřit. K místním recidivám dochází až v 66% a většina recidiv se objevuje do 2 let od začátku léčby. Vzdálené metastázy nejsou časté a vznikají většinou pozdě. Prognóza je ještě zhoršována častými přidruženými chorobami.
Prevence
Nejdůležitějším doporučením pro prevenci nádorů oblasti hlavy a krku je především vyhnout se kouření a nestřídmé konzumace alkoholu. U nemocných s premaligními lézemi a u nemocných již dříve léčených pro nádory oblasti hlavy a krku, byla intenzivně studována chemoprevence. Nejnadějnější v prevenci orálních malignit se ukázaly být retinoidy. Isotretinoin je účinný v léčbě přednádorových stavů, je ale značně toxický a účinek velmi rychle mizí po vysazení přípravku.
Nádory nosohltanu
Ve srovnání s ostatními nádory hlavy a krku mají nádory nosohltanu řadu odlišných vlastností. Vyskytuje se především v oblasti jižní Číny a jihovýchodní Asie. V Evropě se jedná o nádor relativně řídkého výskytu. Vyskytuje se spíše v mladších věkových skupinách. Byla prokázána přímá souvislost s infekcí virem Epstein-Barrové. Mezi faktory prostředí byl prokázán vliv nitrosaminů při konzumaci sušených solených ryb v jihovýchodní Asii a severní Africe.
Časná stadia nádorů nosohltanu bývají bez příznaků, nebo zůstávají skryta pod příznaky zaměnitelnými s infekcí horních cest dýchacích. Často se diagnóza nádorů nosohltanu stanoví až v pokročilém stadiu choroby při metastatickém postižení krčních lymfatických uzlin. Jiným prvním příznakem může být i chronický zánět středouší s pocitem zalehnutí ucha, způsobený růstem nádorů v nosohltanu.
Diagnosticky se nádor nosohltanu ověřuje nepřímou epifaryngoskopií (vyšetřením nosohltanu pomocí zvětšovací optiky) s odběrem tkáně k mikroskopickému vyšetření. Počítačová tomografie zjistí rozsah kostního postižení, zatím co magnetická rezonance zobrazí spíše měkké části nádoru, uzlin a cév. Nejčastěji je nádor nosohltanu diagnostikován v postranní části nosohltanu. Další vyšetření: otoskopie, audiogram, vyšetření hlavových nervů. Pro ověření vzdálených metastáz jsou vhodné: snímek plic, monografie břicha, scintigrafie kostí.
Léčba spočívá v radioterapii a chirurgickém odstranění krčních uzlin. Chemoterapie je indikována v kombinaci s radioterapií u pokročilých nádorových stadií.
Nádory slinných žláz
Zaujímají jen 6% nádorů hlavy a krku, maligní jsou asi v 35ti procentech. Revidivují až v 85ti procentech a 90% pacientů s maligními tumory slinných žláz zemře do 15ti let od diagnosy. Histologie jsou různé, od adenokarcinomu přes adenoidně cystický, mucoepidermoidní a další méně časté. Nejčastějším etiologickým faktorem je práce s těžkými kovy, kouření, častěji se vyskytují u mužů vyššího věku a dle studie INTERphone na 1266 ti pacientech je prokázána přímá souvislost i s užíváním mobilních telefonů (více než 10 let a více než 1035 hodin bez hands free).21 Základní léčba nepokročilého onemocnění je chirurgická, možná je i radioterapie u pozitivních okrajů a recidiv, případně paliativně u oligometastatického onemocnění. Systémová léčba u metastatického onemocnění je jednak chemoterapie založená na platině a taxanech, eventuálně antracyklinech, z kterých se nejúčinnější jeví mitoxantron.22 Další možností je léčba dle prediktivních markerů: v případě pozitivity androgenního receptoru jsou zkušenosti s Bicalutamidem, goserelinem, u HER 2 neu amplifikace s herceptinem, u k ckit a PDGFR wt i imatinib mesylatem a sunutinibem.23
ZÁVĚR
Stále významnější v léčbě nádorů HNC je kvalita života. Cílem je, aby více pacientů nejen žilo, ale bylo schopno plnohodnotného života. Dokážeme zvládnout vedlejší výsledky léčby tak, že pacient může během léčby pokračovat v běžné denní aktivitě. Je to závažné hlavně z toho důvodu, že karcinom zůstává hlavní příčinou úmrtí. Očekává se, že v roce 2030 bude úmrtí na karcinom stoupat globálně až o 80 %. Proto je třeba, aby nové objevy přicházely z laboratoře k pacientovi rychleji. Díky menší toxicitě je důležitá možnost expanze léčby i pro starší pacienty, více jak 60% karcinomů se vyskytuje u pacientů nad 65 let a starších, při tom v klinických studiích jsou obyčejně zastoupení většinou mladší pacienti. A populace bude stárnout. První úspěchy imunoterapie jsou oprávněně považovány za „pokrok roku“, vedle chemoterapie, radioterapie a chirurgie se staly novým pilířem protinádorové léčby. Co asi bude následovat? Existuje celá řada nových možností, kombinace více inhibitorů, nebo kombinace s tradiční terapií – chemoterapií, cílenou terapií a radioterapií.
Literatura
- Mechl Z, Brančíková D.- Nádory hlavy a krku – pohled onkologa. Postgraduální medicína 2012, (14), 777 -786
- La Vecchia C, Bosetti C, Lucchini F, et al. Cancer mortality in Europe. 200-2004 and an overview of trends since 1975. Ann Oncology 201021: 6;1323-61
- Dušek L et al. Czech Cancer Care in Numbers. 2008 - 2009. Grada Publ. 2009
- Smilek P, Plzák J, Klozar J et al Karcinomy dutiny ústní a hltanu.MSD 2015
- Sadetzki S, Chetrit A, Jarus-Hakak A, Cardis E, Deutch Y, Duvdevani S, Zultan A, Novikov I, Freedman L, Wolf M. Cellular phone use and risk of benign and malignant parotid gland tumors--a nationwide case-control study. Am J Epidemiol. 2008 Feb 15;167(4):457-67. doi: 10.1093/aje/kwm325. Epub 2007 Dec 6. PMID: 18063591.
- Dubner S, Narayan D. et al Head and Neck Cancer, Medscape updating 2017.
- Stevenson AM, Petruzzeli GJ et al. Head and Neck Cancer Treatment, Protocols. Medscape, 2016
- Chaturvedi P.A. Techniques for targeted molecular therapy. Medscape Nov 20, 2016
- Vermorken JB, Mesia R, Rivera F, et al. Platinum-based chemotherapy plus cetuximab in head and neck cancer..N Engl J Med 2008; 359: 1116-27
- Pogorzelski M, Ting S, Gauler TC et al. Impact of human papilloma virus infection on the response of head and neck cancers to anti-epidermal growth factor receptor antibody therapy.Cell Death and Disease. 2014; 5, e 1091
- Verrmorken JB, Psyrri A, Mesia R. et al. Impact of tumor HPV status on outcome in patients with recurrent and/or metastatic squamous cell carcinoma of the HNSCC with or without cetuximab. Ann Oncol 2014; 25 (4): 801-809
- Ang KK, Harris J, Wheeler MS et al. Human Papillomavirus and Survival of Patients with Oropharyngeal Cancer. N Engl J Med 2010, 363, July 1. 24-35
- Gillison MI. HPV and prognosis for patiens with oropharynx cancer. Eur J Cancer 2009; 45 (Suppl 1): 38-385
- Pssyri A, Gouveris P, Vermorken JB. Human papillomavirus-related head and neck tumors: clinical and research implications. Curr Opinion Oncol 2009; 344: 1125-31.
- Klozar J,,Zábrodský M, Kodet R. et el.. Humánní papilomy v etiologii karcinomu ústní dutiny a orofarynx. Orolaryng. Foniatr 2007; 56: 73-81
- Vermorken JB, Pssyri A, Mesia R et al. Impact of tumor HPV status on outcomes in patients with recurrent and/or metastatic squamous cell carcinoma of the HNSCC with
or without cetuximab. Ann Oncol 2014; 25, 801-807 - Ferris RL, Blumenschein G Jr, Fayette J, Guigay J, Colevas AD, Licitra L, Harrington KJ, Kasper S, Vokes EE, Even C, Worden F, Saba NF, Docampo LCI, Haddad R, Rordorf T, Kiyota N, Tahara M, Lynch M, Jayaprakash V, Li L, Gillison ML. Nivolumab vs investigator's choice in recurrent or metastatic squamous cell carcinoma of the head and neck: 2-year long-term survival update of CheckMate 141 with analyses by tumor PD-L1 expression. Oral Oncol. 2018 Jun;81:45-51. doi: 10.1016/j.oraloncology.2018.04.008. Epub 2018 Apr 17. PMID: 29884413; PMCID: PMC6563923.
- Seiwert TY, Haddad R, Gupta S. et al Antitumor actvity of the anti-PD-1 antibody pembrozulimab in biomarker – unselected patients with R/M head and neck cancer „
preliminary results from the KEYNOTE-P12 expansion cohort. J Clin Oncol 2015 (suppl) abst LBA 6008). - Vermorken JB, Mesia R, Rivera F, et al. Platinum-based chemotherapy plus cetuximab in head and neck cancer. N Engl J Med 2008; 359: 1116-1127.
- Guardiola E, Peyrade F, Chaigneau L, et al. Results of a randomised phase II study comparing docetaxel with methotrexate in patients with recurrent head and neck cancer. Eur J Cancer 2004; 40: 2071-2076.
- Siegal Sadetzki, Angela Chetrit, Avital Jarus-Hakak, et all Cellular Phone Use and Risk of Benign and Malignant Parotid Gland Tumors, a Nationwide Case-Control Study. Am. J. Epidemiol. (2008) 167 (4): 457-467.
- Aymen Langha et all.Systemic therapy in the management of metastatic or advanced salivary gland cancers Head Neck Oncol. 2012; 4: 19.
- Scott A. Laurie , Lisa Licitra. Systemic Therapy in the Palliative Management of Advanced Salivary Gland Cancers JCO June 10, 2006 vol. 24 no. 17 2673-2678
- Bourhis J, Overgaard J, Audry H. et al. Hyperfractionated or accelerated radiotherapy in head and neck cancer: a meta-analysis. Lancet 2006; 368: 843-854.
- Hall EJ,Wuu CS. Radiation-induced second cancers: the impact of 3D-CRT and IMRT. Int J Radiat Oncol Biol Phys 2003; 56: 83.
- Nutting CM, Morden JP, Harrington KJ, et al. Parotis sparing intensity modulated versus conventional radiotherapy in head and neck cancer (PARSPORT): a phase 3, multicentre randomised controlled trial, Lancet Oncol 2011; 12: 127-136
