Před zahájením onkologické léčby musí být proveden staging onemocnění. U každého pacienta bychom měli zvážit možnosti multioborového přístupu. Níže jsou uvedena indikační kritéria pro prezentaci pacienta na multioborovém týmu:
a) pacienti s pT2G4 /sarkomatoidní složkou a pT3 a více onemocněním
b) pacienti s pozitivními uzlinami N1
c) pacienti s M1 postižením, u kterých se předpokládá multioborový přístup (metastazektomie, cytoreduktivní nefrektomie)
d) všichni pacienti k operační léčbě (zvážení robotické chirurgie)
e) jiné histologické podtypy RCC než světlobuněčný karcinom
f) všichni pacienti s klinicky lokalizovaným tumorem, u kterých se nezvažuje radikální operace (zvažuje se použití lokálních metod, např. SBRT, RFA, MWA atd.)
Doporučené prediktivní vyšetření u kandidátů na systémovou léčbu
1/ světlobuněčný mRCC: fakultativně PD-L1 a další cílitelné aberace (multigenový NGS onkopanel)
2/ nesvětlobuněčný mRCC: vzhledem k nedostatku uspokojivých možností systémové léčby lze zvážit vyšetření na cílitelné aberace (multigenový NGS onkopanel) již iniciálně v době zjištění metastatického onemocnění
3/ genetické vyšetření při podezření na hereditární syndromy (např. syndrom Von Hippel Lindau, Birt-Hogg-Dubé, atd.)
21.1 Léčba lokalizovaného onemocnění (stádium I, II a operabilní III. stádium)
Základem je léčba chirurgická. Pokud je to možné, pak by u všech T1 tumorů měl být proveden ledvinu šetřící výkon, ve všech ostatních případech je provedena radikální nefrektomie. Ledvinu šetřící výkon by měl být zvážen i u T2 tumorů, pokud je technicky možný. Regionální lymfadenektomie je možná u vysoce rizikových tumorů nebo v případě radiograficky patrné lymfadenopatie z důvodů zpřesnění stagingu a prognózy, i když její onkologický benefit nebyl jednoznačně prokázaný.
Miniinvazivní přístupy (laparoskopický nebo robotický) mají nižší morbiditu oproti otevřenému přístupu. Onkologické výsledky jsou srovnatelné. Miniinvazivní přístup by měl být preferován vždy, pokud nejsou ohroženy onkologické, funkční nebo perioperační výsledky.
U nádorů malého objemu (small renal mass, tj. ≤ cca 3 cm) u pacientů s kratší předpokládanou dobou života je možné sledování nebo miniinvazivní postupy, např. RFA. U těchto nemocných je indikována biopsie nádoru s výjimkou pacientů se závažnými komorbiditami, které znemožňují aktivní léčebný přístup ve smyslu operace nebo lokálně ablativních metod.
Adjuvantní léčba pembrolizumabem může být zvažovaná u pacientů s operabilním světlobuněčným RCC se středním nebo vysokým rizikem (střední riziko: pT2, grade 4 nebo sarkomatoidní složka, N0M0 nebo pT3, jakýkoliv grade, N0M0; vysoké riziko: pT4, jakýkoliv grade, N0M0 nebo jakékoliv pT jakýkoliv grade, N1M0) po konzultaci s pacientem s ohledem na potenciální dlouhodobé nežádoucí účinky (úroveň důkazů 1).
K odhadu rizika relapsu lze využít různé prognostické modely (např. Leibovich skóre, UISS). Možnosti systémové léčby po relapsu jsou uvedené ve schématu níže. U pacientů po metastasektomii (dle registrační studie optimálně do jednoho roku od nefrektomie) pro oligometastatické onemocnění lze nabídnout adjuvantní pembrolizumab po kompletní resekci (stupeň doporučení 1)..
21.2 Léčba pokročilého onemocnění (neoperabilní lokálně pokročilé onemocnění a metastatické stádium)
21.2.1 Chirurgická léčba metastatického karcinomu ledviny
- Paliativní nefrektomie je indikována v případě výskytu konzervativně neřešitelných lokálních příznaků, jako je například neztišitelné krvácení.
- Cytoredukční nefrektomii jako zahájení léčby indikujeme individuálně v závislosti na celkovém stavu pacienta a rozsahu onemocnění. Výsledky studie CARMENA by neměly vést ke kontraindikaci cytoredukční nefrektomie, kterou je vhodné zvážit zejména u pacientů s nízkým objemem metastatického onemocnění, ECOG stavem 0–1 a v příznivém či středním riziku (především pak v přítomnosti jednoho rizikového faktoru). Navíc ve studii CARMENA byl hodnocen sunitinib, který dnes již nepředstavuje preferovanou možnost léčby první paliativní linie. Recentně publikovaná data ukazují, že klinické výsledky jednotlivých podskupin pacientů podstupující léčbu moderní imunoterapií byly lepší, pokud podstoupili primární nebo odloženou (při efektu systémové terapie) cytoredukční nefrektomii. U pacientů v nepříznivé rizikové skupině je primárně indikovaná systémová léčba. U všech nemocných podstupujících primárně systémovou terapii (zejména imunoterapii) je možné zvážit, dle odpovědi na léčbu, odloženou nefrektomii, buď jako cytoredukci, nebo jako pokus o kurativní léčbu po vymizení, dlouhodobé stabilizaci nebo adekvátním ošetření všech metastáz (úroveň důkazů 2A).
- Chirurgická léčba metastáz je doporučena v případě možnosti jejich kompletního odstranění a zvážení přínosu vs. operační zátěže (úroveň důkazů 2A), alternativou může být využití lokálně ablativních metod (např. SBRT).
21.2.2 Systémová léčba metastatického karcinomu ledviny
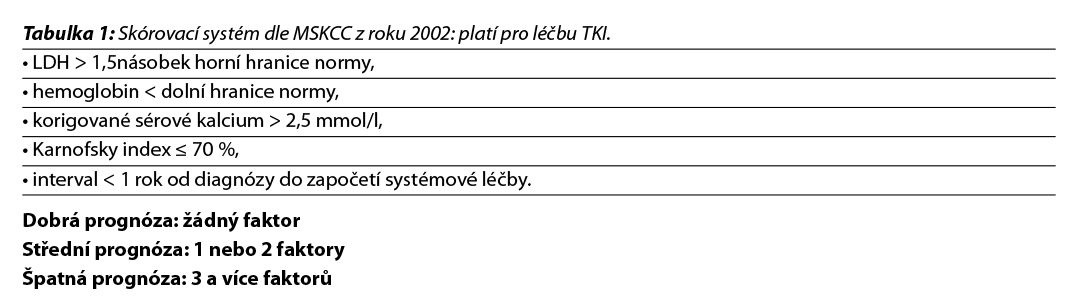
Pro léčbu v první linii cílené terapie multikinázovými inhibitory se používá skórovací systém dle MSKCC z roku 2002 (Motzer a kol. 2002) – tabulka 1 nebo dle IMDC (Heng a kol. 2009) – tabulka 2. Při použití kombinované terapie (TKI a checkpoint inhibitory, či nivolumabu a ipilimumabu) se používá skórování dle IMDC. Při stanovení prognostické kategorie je nutno dodržovat aktuální indikační omezení a způsob úhrady stanované SÚKL – úhrada může být vázána jen na MSKCC nebo jen na IMDC kritéria.

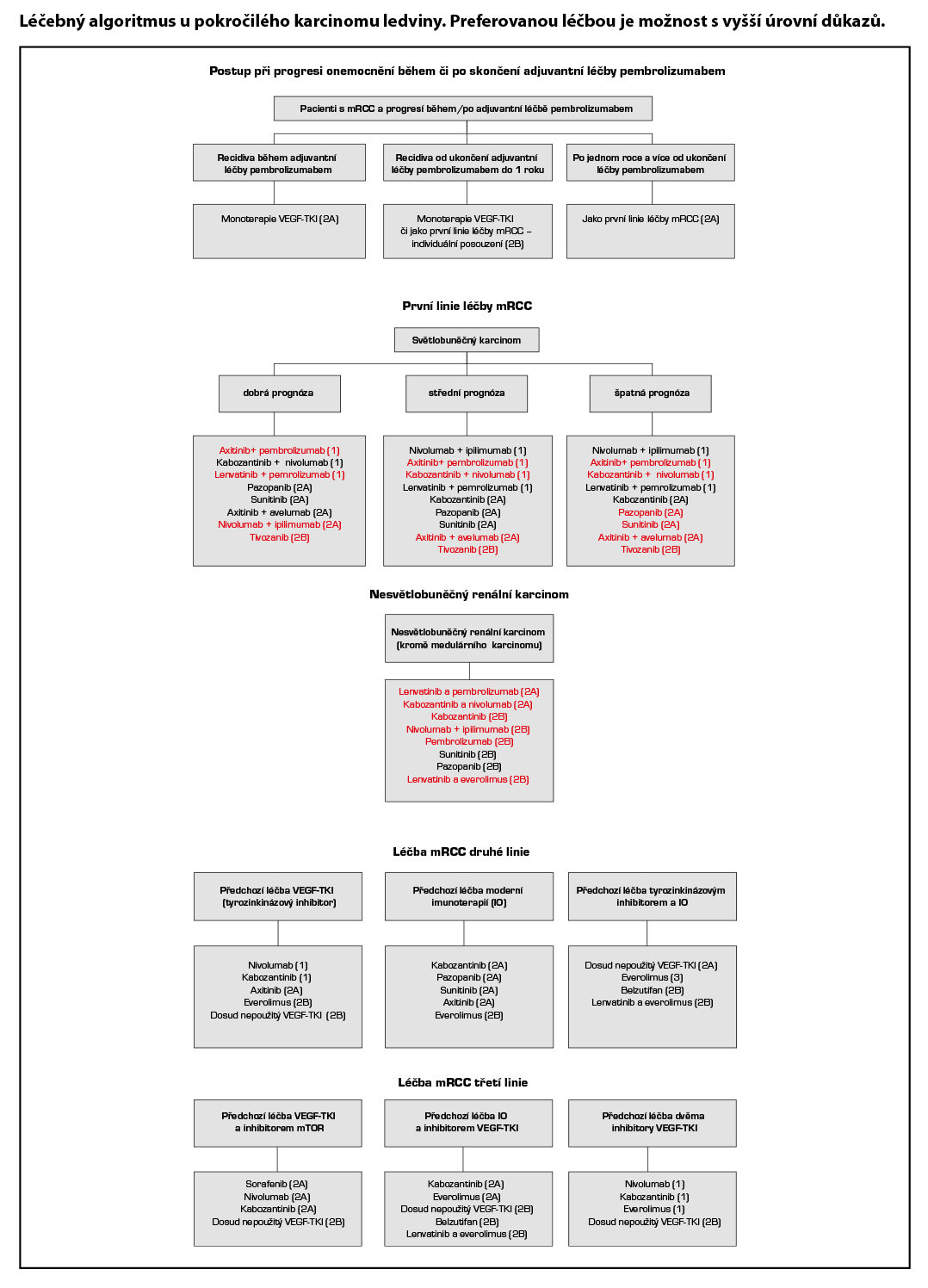
Poznámka:
Červeně jsou označeny moderní léky, které nemají k 1. 3. 2026 stanovenu úhradu ze zdravotního pojištění. Ve vyšších liniích léčby nelze barevně odlišit hrazenou a nehrazenou léčbu pro různé znění úhrad u daných preparátů. Indikace moderních preparátů je podmíněna splněním pravidel úhrady dle SÚKL (www.sukl.cz).
Komentář k léčebným schématům
- Uvedená doporučení jsou založená na nejnovějších medicínských poznatcích a nemusí se vždy shodovat s pravidly úhrady léku od plátce péče.
- Pokud se týká kombinačních režimů, jsou v první linii léčby pacientů s mRCC v dobré prognostické skupině ze zdravotního pojištění hrazena kombinace axitinibu a avelumabu, kabozantinibu a nivolumabu nebo lze podat sunitinib nebo pazopanib v monoterapii (je možno zvolit i strategii sledování – watch and wait). U pacientů se střední a špatnou prognózou jsou v první linii léčby pacientů s mRCC doporučeny kombinované režimy s moderní imunoterapií (IO) (viz Léčebný algoritmus paliativní léčby I. linie). V případě kontraindikace či nevhodnosti imunoterapeutických kombinací lze podat u pacientů se střední prognózou kabozantinib, sunitinib nebo pazopanib v monoterapii, u pacientů se špatnou prognózou kabozantinib v monoterapii.
- U nemocných s mRCC by mělo být zvažováno zařazení do klinické studie.
- Doporučuje se zahajovat terapii plnou dávkou cíleného léku s redukcí dávky při limitující toxicitě (2A).
- Několik studií ukázalo, že na základě PFS v první linii léčby nelze předpovídat PFS na 2. linii terapie.
- U RCC se sarkomatoidní složkou je nutné preferovat především kombinovanou imunoterapii checkpoint inhibitory nebo kombinaci checkpoint inhibitorů s TKI, které výrazně zlepšují výsledky ve srovnání s monoterapií tyrozinkinázovými inhibitory (1; nutno dodržovat úhradové omezení).
- U nemocných s indolentním průběhem onemocnění (především v dobré prognostické skupině) je možné sledování bez systémové protinádorové léčby (2A).
- U pacientů s nesvětlobuněčným pokročilým renálním karcinomem by měla být léčba individualizována dle podtypu, doporučené schéma v léčebném algoritmu je orientační a nelze aplikovat na všechny podtypy RCC. Pro vedení léčby doporučujeme sledovat např. NCCN či ESMO guidelines. Naprosto výjimečný přístup vyžadují především medulární renální karcinom a karcinom ze sběrných kanálků (léčba u karcinomu ze sběrných kanálků je založena především na chemoterapii).
- Počet linií léčby mRCC by neměl být limitován jinak než stavem nemocného a dostupností léků (2A). Vyšší počet použitých linií pozitivně koreloval v retrospektivních studiích s celkovým přežitím pacientů.
- Belzutifan je indikován v monoterapii k léčbě dospělých pacientů s von Hippelovou-Lindauovou chorobou (VHL), u nichž nejsou lokalizované procedury vhodné, a kteří vyžadují léčbu klinických projevů VHL:
- lokalizovaného karcinomu ledvin (RCC),
- hemangioblastomů nebo jiných lézí centrálního nervového systému (CNS) nebo oka,
- neuroendokrinních nádorů pankreatu (pNET).
Doporučení uvedená v Modré knize vychází z medicíny založené na důkazech. Postupně se budeme snažit k jednotlivým doporučením přičlenit také určitý stupeň, který vyjadřuje míru důkazů a míru doporučení ČOS. Vycházíme z modifikovaného systému, který používá NCCN a ESMO.
ČOS: Stupně evidence a doporučení
Stupeň 1 Založeno na vysokém stupni důkazů, jednotné doporučení ČOS, že léčba je vhodná.
Stupeň 2A Založeno na nižším stupni důkazů, jednotné doporučení ČOS, že léčba je vhodná.
Stupeň 2B Založeno na nižším stupni důkazů, doporučení ČOS, že léčba je vhodná.
Stupeň 3 Založeno na jakémkoliv stupni důkazů, v rámci ČOS není shoda o vhodnosti léčby.
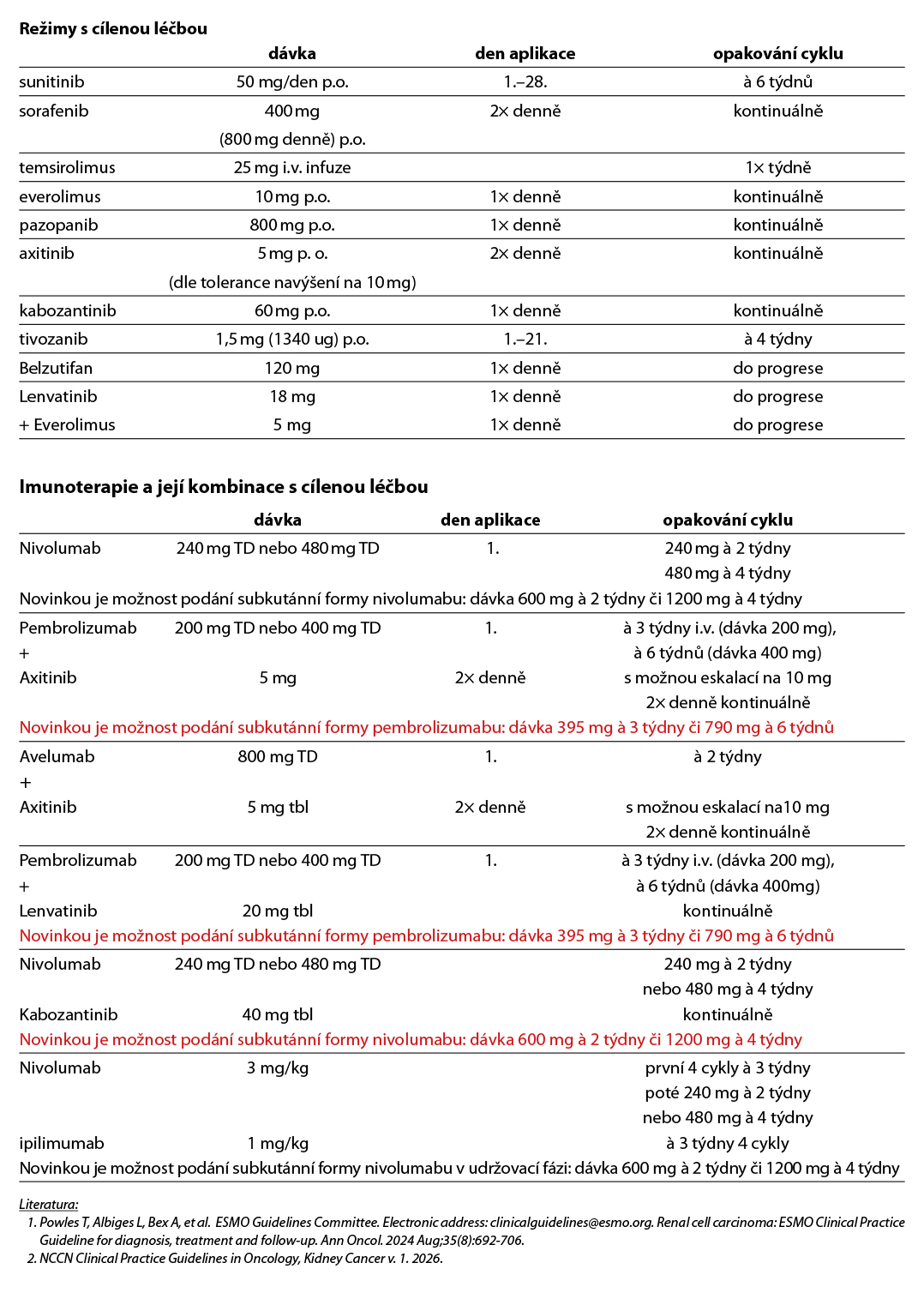
Literatura:
- Powles T, Albiges L, Bex A, et al. ESMO Guidelines Committee. Electronic address: clinicalguidelines@esmo.org. Renal cell carcinoma: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2024 Aug;35(8):692-706.
- NCCN Clinical Practice Guidelines in Oncology, Kidney Cancer v. 1. 2026.
21.3 Renální karcinom-follow-up
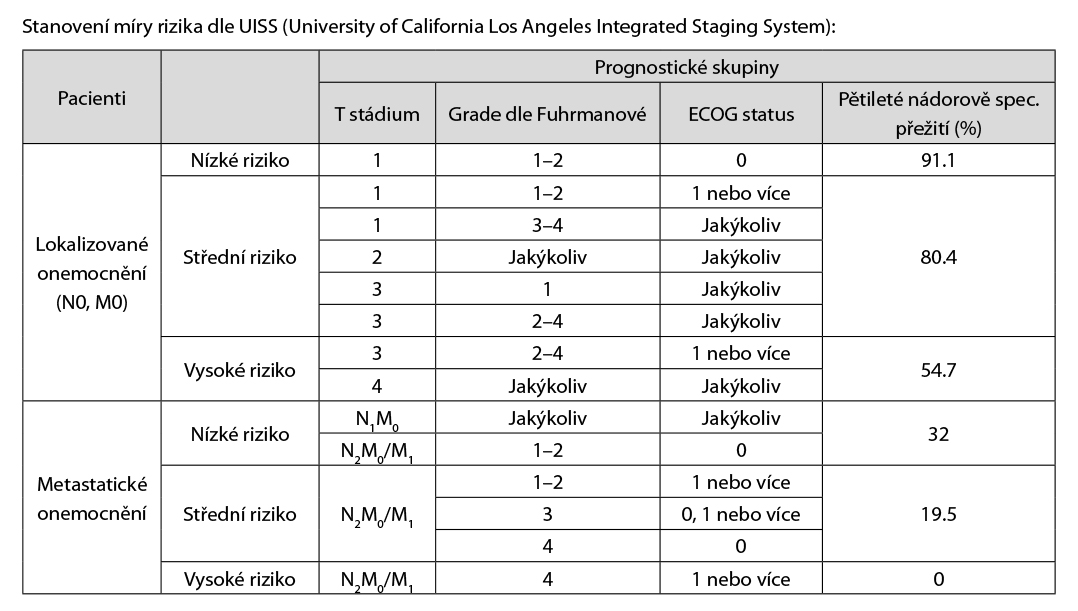
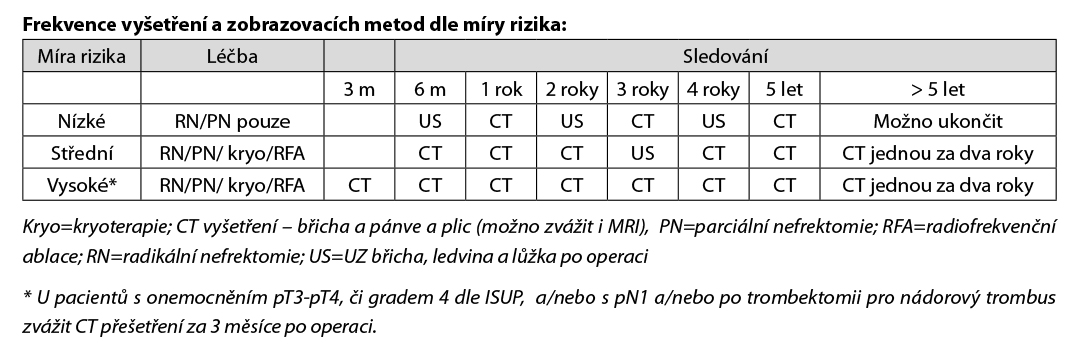
Zobrazovací vyšetření a laboratorní vyšetření jsou indikovány dle úvahy lékaře na základě klinického vyšetření. Kontroly a vyšetření se pak u pacientů s RCC zaměřují na pooperační komplikace, renální funkce (kontroly GFR, biochemie, krevní obraz, moč+sed), lokální a kontralaterální rekurence a vzdálené metastázy. Doba sledování není jasná, všeobecné doporučení je minimálně 5 let po operaci (pozdní relapsy u low-risk tumorů nejsou vyloučené). Základním vyšetřením je CT vyšetření břicha a pánve (možno též zvážit i MRI pro snížení radiační zátěže), CT hrudníku. CT hrudníku může být později nahrazeno RTG plic. UZ břicha a pánve se doporučuje u pacientů s nízkým rizikem – viz níže uvedená tabulka. Kostní scan a CT/PET vyšetření se provádí jen v indikovaných případech.
U pacientů s RCC provádíme skórování rizika rekurence dle nomogramů, následně dle stupně rizika se stanovuje frekvence kontrol a vyšetření, nejčastěji užíváme nomogramy: UISS či SSIGN. Níže je uvedená tabulka UISS, lze použít i on-line kalkulátory: www.mdcalc.com/ucla-integrated-staging-system-uiss-renal-cell-carcinoma-rcc
www.mdcalc.com/ssign-score-renal-cell-carcinoma-rcc