8. ZHOUBNÝ NOVOTVAR BRONCHU, PLÍCE, PLEURY A THYMU (C34, C33, C37)
8.1 Nemalobuněčný karcinom
Rozhodnutí o indikaci cílené léčby nebo imuno(chemo)terapie je bezpodmínečně závislé na histologické typizaci nádoru a následném stanovení prediktivních markerů na molekulární úrovni. Prediktivní testování v současné době zahrnuje reflexní testování dle platných algoritmů pro hodnocení mutačního stavu genu EGFR, chromozomálních translokací zasahujících gen ALK, ROS1 a imunohistochemické vyšetření exprese PD-L1. Testování probíhá již v době stanovení diagnózy, bez ohledu na typ bioptického materiálu (u resekátu i malého bioptického vzorku probíhá automatické vyšetření prediktorů EGFR, ALK, ROS1, PD-L1 indikované patologem dle stejného algoritmu). Další metodou je komplexní molekulární testování pomocí NGS. Jedná se o komplexní vyšetření somatických aberací na úrovni DNA a RNA, které je prováděno na základě indikce multidisciplinárního indikačního semináře KOC (MDT). Testování metodou NGS je prováděno na žádost onkologa buď v průběhu onemocnění, nebo hned v rámci primodiagnózy (Podrobněji viz www.patologie.info/soubory/all/NGS.pdf) Pacienti klinického stádia I-III, kteří jsou schopni podstoupit protinádorovou léčbu, by vždy měli být prezentováni v rámci MDT KOC.
8.1.1 Stadium I (IA1 = T1a, IA2 = T1b, IA3 = T1c nebo IB = T2a, vše N0 M0)
U operabilních pacientů je indikována chirurgická léčba. Standardem je lobektomie se systematickou mediastinální lymfadenektomií, preferenčně videoasistovaná torakotomie (VATS) nebo roboticky asistovaná torakotomie (RATS). U malých periferních tumorů lze akceptovat systematický sampling nejméně 3 uzlinových stanic dle ESTS (European Society of Thoracic Surgery). Torakotomický přístup je možný v případě nepříznivé anatomické lokalizace tumoru, při adhesích apod. U malých periferních nádorů ≤ 2 cm je doporučována segmentární resekce ev. multisegmentární resekce (dle lokalizace a charakteru tumoru) s lymfadenektomií. U vysoce rizikových pacientů lze provést klínovitou (neanatomickou) resekci, radikalita uvedeného výkonu je však zřejmě obdobná, jako je tomu v případě stereotaktické radioterapie. V případě R1 nebo R2 resekce je preferována reresekce. Pokud není reresekce indikována, pak je indikována radioterapie. U inoperabilních pacientů (ve stadiu I a z indikace interních komorbidit, případně při odmítnutí chirurgické léčby) je indikována radioterapie, přednostně stereotaktická radioterapie (stereotactic body radiation therapy, SBRT). Adjuvantní chemoterapie není ve stadiu IA indikována. Ve stadiu IB je možné zvážit podání adjuvantní chemoterapie v případě rizikových faktorů jako je angioinvaze, grade 3, invaze pleury, klínovitá resekce a pNX. Po úplné resekci nádoru ve stadiu IB s průkazem delece exonu 19 nebo substituční mutaci exonu 21 (L858R) receptoru epidermálního růstového faktoru (EGFR) je indikován adjuvantní osimertinib.
8.1.2 Stadium II
(UICC 8: IIA = T2bN0, IIB = T1a-cN1, T2a,b N1, T3N0, vše M0)
(UICC9: IIA = T2bN0 nebo T1a-cN1, IIB = T2a,bN1 nebo T3N0 nebo T1a-CN2a, vše M0)
Operabilní: Ve stadiu IIA je podobně jako ve stadiu I indikována anatomické resekce, nejčastěji lobektomie se systematickou mediastinální lymfadenektomií nebo mediastinální lymfadenektomií. V případě nutnosti resekce většího rozsahu je preferován parenchym šetřící výkon (sleeve lobektomie) před pneumonektomií. I v tomto případě je možné preferovat miniinvazivní přístupy. Stadium IIB T3N0M0 může zahrnovat resekci hrudní stěny s její náhradou (včetně Pancoastova tumoru v plicním hrotu), ale může zahrnovat i VATS či RATS lobektomii v případě malého satelitního tumoru ve stejném laloku, jako je primární nádor.
V případě R1 nebo R2 resekce je indikována reresekce, pokud je kontraindikace reresekce, pak je indikována radioterapie (u malých N0 nádorů, přednostně SABR), u větších nádorů nebo N1-2a chemoradioterapie podle standardu inoperabilního stadia III.
Ve stadiu II je indikována kromě lokální léčby léčba systémová, a to neoadjuvantní imunochemoterapie nebo perioperační imunochemoterapie nebo adjuvantní léčba chemoterapií, imunoterapií nebo cílená léčba osimertinibem nebo alektinibem, výjimečně neoadjuvantní chemoterapie samotná.
Předoperační (neoadjuvantní) imunochemoterapie v kombinaci 3 cyklů checkpoint inhibitoru a chemoterapie na bázi platiny.
Nivolumab v kombinaci s chemoterapií na bázi platiny.
je indikován k neoadjuvantní léčbě dospělých pacientů s resekovatelným NSCLC stádia IB-IIIA (dle 7. TNM klasifikace), který má expresi PD-L1 ≥ 1 % (CheckMate 816). Neoadjuvantní nivolumab s chemoterapií vedl k významně delšímu celkovému přežití, přežití bez progrese nádoru a vyššímu procentu pacientů s patologickou kompletní odpovědí než samotná chemoterapie. Přidání nivolumabu k neoadjuvantní chemoterapii nezvýšilo incidenci nežádoucích účinků ani neztížilo proveditelnost operace.
Perioperační imunochemoterapie v kombinaci 4 cyklů checkpoint inhibitoru a chemoterapie na bázi platiny předoperačně a následná pooperační imunoterapie.
Pembrolizumab* je v kombinaci s chemoterapií obsahující platinu v neoadjuvantní léčbě a následně v monoterapii po dobu 13 cyklů v adjuvantní léčbě indikován k léčbě resekovatelného nemalobuněčného karcinomu plic s vysokým rizikem recidivy (klinického stádia II-IIIB dle 8. klasifikace) u dospělých bez ohledu na přítomnost nebo výši exprese PD-L1 na základě studie Keynote-671. Studie prokázala statisticky významná zlepšení OS, EFS, pCR a mPR u pacientů randomizovaných do ramene s pembrolizumabem.
Nivolumab* je indikován v kombinaci s chemoterapií na bázi platiny k neoadjuvantní léčbě následované adjuvantní léčbou nivolumabem v monoterapii po dobu 13 cyklů u dospělých pacientů s resekovatelným nemalobuněčným karcinomem plic s vysokým rizikem recidivy, jejichž nádory mají expresi PD-L1 ≥ 1 % na základě studie CA209-77T. Studie prokázala statisticky významné zlepšení EFS a v průběžné analýze zlepšení OS u pacientů randomizovaných do ramene s nivolumabem.
Durvalumab* je v kombinaci s chemoterapií na bázi platiny jako neoadjuvantní léčba (maximálně 4 cykly) a následně po operaci v monoterapii jako adjuvantní léčba (maximálně 12 cyklů) indikován k léčbě dospělých pacientů s nemalobuněčným karcinomem plic s vysokým rizikem recidivy a bez mutací EGFR nebo přestavby ALK. Studie AEGEAN prokázala významné zlepšení EFS a pCR u pacientů randomizovaných k léčbě durvalumabem ve srovnání s léčbou placebem.
Tislelizumab* je v kombinaci s chemoterapií obsahující platinu v neoadjuvantní léčbě (3–4 cykly) a následně v monoterapii v adjuvantní léčbě (až 8 cyklů) indikován k terapii resekovatelného nemalobuněčného karcinomu plic s vysokým rizikem recidivy u dospělých. Studie BGB-A317-315 prokázala statisticky významné zlepšení MPR, EFS, pCR a OS u pacientů randomizovaných do ramene s tislelizumabem ve srovnání s ramenem s placebem.
Imunoterapie v adjuvantní léčbě:
Atezolizumab je na podkladě výsledků studie IMpower010 indikován po dobu 1 roku po úplné resekci a chemoterapii na bázi platiny k adjuvantní léčbě dospělých pacientů, kteří mají nádory s expresí PD-L1 na ≥ 50 % nádorových buněk (TC) a kteří nemají NSCLC s aktivačními mutacemi EGFR nebo přestavbami ALK.
Pembrolizumab* je v monoterapii indikován po dobu 1 roku k adjuvantní léčbě dospělých s NSCLC, kteří mají vysoké riziko recidivy po kompletní resekci a léčbě chemoterapií na bázi platiny na základě studie PEARLS/Keynote-091 bez ohledu na hodnotu exprese PD-L1.
Terčová léčba u EGFR mutovaných NSCLC:
Osimertinib je indikován po úplné resekci nádoru s průkazem delece exonu 19 nebo substituční mutace exonu 21 (L858R) (studie ADAURA), po ukončení adjuvantní chemoterapie nebo bez ní, po dobu až 3 let.
Terčová léčba u NSCLC s translokací genu ALK:
Alectinib je indikován v monoterapii jako adjuvantní léčba po úplné resekci nádoru u dospělých pacientů s ALK pozitivním NSCLC s vysokým rizikem rekurence po dobu až dvou let.
Adjuvantní chemoterapie je indikována v případě kontraindikace imunoterapie v dávce 4 cykly kombinace založené na cisplatině nebo karboplatině (podle klinického stavu).
Výjimečně může být indikována předoperační (neoadjuvantní) chemoterapie 3–4 cykly kombinace založené na cisplatině nebo karboplatině, opět jen u případů, kde je nevhodná kombinace s imunoterapií.
Inoperabilní: konkomitantní chemoradioterapie nebo sekvenční chemoradioterapie nebo radioterapie samostatná při kontraindikaci chemoterapie. U stadia T2bN0M0 lze také uvažovat o stereotaktické radioterapii. Zásady chemoradioterapie jsou stejné jako u inoperabilního stadia III. *K 1. 3. 2026 nebyla v ČR pro pembrolizumab, nivolumab, durvalumab a tislelizumab v perioperační ani v adjuvantní léčbě stanovena úhrada.
*K 1. 3. 2026 nebyla v ČR pro pembrolizumab, nivolumab, durvalumab a tislelizumab v perioperační ani v adjuvantní léčbě stanovena úhrada.
8.1.3 Stadium III
(UICC8: IIIA = T1-2N2, T3N1, T4N0-1; IIIB = T3-4N2, T1-2N3; IIIC = T3-4N3, vše M0)
(UICC9: IIIA = T1N2b, T2N2a, T3N1-2a, T4N0-1; IIIB = T1N3, T2N2b-3, T3N2b, T4N2a-b; IIIC = T3-4N3
8.1.3.1 Stadium III operabilní dle multidisciplinárního týmu
Ve stadiu IIIA, eventuálně ve stadiu IIIB, je opět dle individuálního posouzení multidisciplinárním týmem možná chirurgická léčba v podobě anatomické resekce, nejčastěji lobektomie se systematickou mediastinální lymfadenektomií. V případě nutnosti většího rozsahu resekce je preferován parenchym šetřící výkon (sleeve lobektomie, případně „double sleeve“ , tj. resekce bronchu i plicní tepny) před pneumonektomií, která je ovšem u lokálně pokročilého nádoru někdy nezbytná. Standardní přístup torakotomický je v expertních rukách stále častěji nahrazován výkony miniinvazivními (VATS či RATS). Operabilní stadium T4N0-2 patří do rukou velmi zkušeného týmu hrudních chirurgů s kompletním zázemím (ECMO, trysková ventilace, špičková intenzivní péče). V případě stadia T4 s invazí se jedná o plicní resekce kombinované s resekcemi velkých cév s jejich náhradou, srdeční síně, resekce průdušnice, kariny (sleeve pneumonektomie), obratlových těl atd. Ve stadiu III je vždy indikována kromě lokální léčby léčba systémová, stejně jako ve stadiu II. Navíc jsou možné kombinace s radioterapií, jako:
Předoperační konkomitantní chemoradioterapie – zejména u nádorů horního sulku (Pancoast). Aplikuje se dávka 40–50 Gy/ 20–25 frakcí.
Pooperační radioterapie je indikována v případě R1(R2) resekce. Dle radikality operace se aplikují dávky 50–66 Gy/ 25–33 frakcí. Při postižení mediastinálních uzlin (N2+) není pooperační radioterapie mediastina paušálně indikována na podkladě negativního výsledku studie LungART, kde nebylo prokázáno prodloužení celkového přežití ani doby do progrese. Adjuvantní radioterapie může být individuálně zvažována při rizikových faktorech u pN2+ jako jsou extrakapsulární extenze, víceetážové postižení, neadekvátní mediastinální lymfadenektomie, kontraindikace nebo intolerance adjuvantní systémové terapie.
Předoperační (neoadjuvantní) imunochemoterapie, perioperační imunochemoterapie, adjuvantní imunoterapie, adjuvantní nebo neoadjuvantní chemoterapie a adjuvantní terčová léčba má stejná pravidla jako u stadia II.
8.1.3.2 Stadium III inoperabilní dle multidisciplinárního týmu
Standardem je konkomitantní chemoradioterapie (přednostně u nemocných s PS 0-1) nebo sekvenční chemoradioterapie (komorbidity) nebo paliativní radioterapie (pravděpodobnost radikality samostatné radioterapie u inoperabilního stadia III je minimální, ale taktika léčby je věcí radioterapeuta) nebo paliativní chemoterapie.
V případě konkomitantní chemoradioterapie se standardně aplikuje dávka 60–66 Gy/30–33 frakcí. Ozařování by mělo být zahájeno ideálně s 1. až 2. cyklem CHT.
V případě indikace sekvenční chemoradioterapie se doporučují před ozářením 2 cykly chemoterapie s bezprostřední časovou návazností radioterapie, při podávání 3 a více cyklů hrozí u chemorezistentních případů progrese bez možnosti následné radikální RT (Curran, Fournel, Zatloukal) (IIA). Konkomitantní chemoradioterapie by měla být podávána ve spolupráci radioterapeutického centra a pneumoonkologického pracoviště. V případě samostatné (paliativní) nebo sekvenční radioterapie lze zvážit akcelerované režimy (např. 18–20× 2,75 Gy, 20–22× 2,5 Gy).
Konsolidační (adjuvantní) imunoterapie:
Durvalumab v monoterapii je indikován k léčbě dospělých pacientů s lokálně pokročilým, neoperovatelným nemalobuněčným karcinomem plic (NSCLC) s expresí PD-L1 ≥1 % nádorových buněk, u kterých nedošlo k progresi onemocnění po konkomitantní radiochemoterapii s CHT na bázi platiny. Léčba se doporučuje do progrese onemocnění nebo nepřijatelné toxicity nebo maximálně 12 měsíců.
Sugemalimab* je v monoterapii indikován k léčbě neresekabilního NSCLC stadia III bez senzibilizujících mutací EGFR nebo genomových aberací ALK, ROS1 u dospělých, jejichž nádory exprimují PD-L1 na ≥ 1 % nádorových buněk a u jejichž onemocnění nedošlo k progresi po chemoradioterapii s CHT na bázi platiny (GEMSTONE-301). Maximální doba léčby v rámci studie byla dva roky nebo do progrese onemocnění nebo nepřijatelné toxicity.
Imunoterapie u pacientů s NSCLC stádia III nevhodných k definitivní chemoradiační léčbě:
Cemiplimab* je indikován k léčbě lokálně pokročilého NSCLC nevhodného k definitivní chemoradiační léčbě v monoterapii v případě exprese PD-L1 ≥ 50 % nebo v kombinaci s chemoterapií na bázi platiny v případě exprese PD-L1 ≥ 1 %.
Anti-EGFR léčba po chemoradiační léčbě:
Osimertinib* je indikován k léčbě neoperabilního lokálně pokročilého NSCLC s mutací EGFR del19 nebo L858R po definitivní chemoradiační léčbě (studie LAURA) * K 1. 3. 2026 nebyla v ČR pro osimertinib po definitivní chemoradiační léčbě, sugemalimab a cemiplimab stanovena úhrada
* K 1. 3. 2026 nebyla v ČR pro osimertinib po definitivní chemoradiační léčbě, sugemalimab a cemiplimab stanovena úhrada
8.1.4 Stadium IV (IVA =T jakékoli, N jakékoli, M1a,b, IVB = M1c) a stadium IIIB nebo IIIC (pokud není možná souběžná chemoradioterapie nebo je radioterapie kontraindikována)
8.1.4.1 Léčba pacientů s průkazem řídících mutací


8.1.4.1.1 Léčba pacientů s prokázanou aktivační mutací EGFR
První linie léčby u pacientů s prokázanou aktivační mutací EGFR
U nemocných s prokázanou aktivační mutací EGFR jsou v první linii léčby indikovány inhibitory tyrozinkinázy EGFR.
- Afatinib je indikován v monoterapii k léčbě dospělých pacientů s lokálně pokročilým nebo metastazujícím NSCLC s aktivačními mutacemi EGFR dosud neléčených EGFR-TKI.
- Dakomitinib* je v monoterapii indikován k léčbě dospělých pacientů s lokálně pokročilým nebo metastazujícím NSCLC s aktivačními mutacemi EGFR.
- Erlotinib je indikován v první linii léčby pacientů s lokálně pokročilým nebo metastazujícím NSCLC s aktivačními mutacemi EGFR, anebo k převedení na udržovací léčbu pacientů s lokálně pokročilým nebo metastazujícím NSCLC s aktivačními mutacemi EGFR a stabilizací nemoci po standardní chemoterapii první linie*.
- Erlotinib v kombinaci s bevacizumabem* je indikován k první linii léčby pacientů s pokročilým, metastatickým nebo rekurentním neskvamózním NSCLC s aktivačními mutacemi EGFR.
- Gefitinib v monoterapii je indikován k léčbě dospělých pacientů s lokálně pokročilým nebo metastazujícím NSCLC s aktivačními mutacemi EGFR.
- Lazertinib v kombinaci s amivantamabem je indikován v první linii léčby dospělých pacientů s pokročilým NSCLC s aktivační mutací EGFR del19 nebo L858R v exonu 21.
- Osimertinib je indikován v monoterapii k léčbě dospělých pacientů s lokálně pokročilým nebo metastazujícím NSCLC s aktivační mutací EGFR a/nebo k léčbě pacientů s lokálně pokročilým nebo metastazujícím NSCLC s přítomnou mutací EGFR T790M.
- Osimertinib v kombinaci s platinovou chemoterapií a pemetrexedem je indikován v první linii léčby dospělých pacientů s lokálně pokročilým nebo metastatickým NSCLC s aktivačními mutacemi EGFR del19 nebo L858R v exonu 21.
* K 1. 3. 2026 nebylo v České republice rozhodnuto o úhradě erlotinibu v udržovací léčbě, kombinace erlotinibu + bevacizumabu a dakomitinibu.
Druhá a další linie léčby u EGFR mutovaných NSCLC po léčbě TKI I., II. nebo III. generace
- T790M pozitivita po léčbě EGFR TKI I. nebo II. generace:
Osimertinib je indikován k léčbě dospělých pacientů s lokálně pokročilým nebo metastazujícím NSCLC, u kterých došlo k progresi při léčbě EGFR TKI I. nebo II. generace, u kterých byla prokázána mutace T790M.
- T790M negativita po léčbě EGFR TKI I. nebo II. generace:
V případě T790M negativity je indikována chemoterapie na bázi platiny nebo amivantamab s chemoterapií na bázi platiny, nebo imuno(chemo) terapie viz. níže.
- Po selhání EGFR TKI:
Amivantamab v kombinaci s chemoterapií karboplatinou a pemetrexedem je indikován k léčbě pokročilého NSCLC s mutací EGFR delece v exonu 19 nebo L858R v exonu 21 po selhání předchozí terapie, včetně EGFR TKI.
Atezolizumab** (bez ohledu na míru exprese PD-L1) v monoterapii nebo v kombinaci s bevacizumabem, paklitaxelem a karboplatinou, může být u pacientů s aktivačními mutacemi EGFR nebo ALK pozitivním NSCLC indikován po selhání vhodných možností cílené léčby.
Pembrolizumab** v monoterapii je indikován u pacientů s expresí PD-L1 ≥ 1 % a pozitivními nádorovými mutacemi EGFR nebo ALK, kteří musí být předtím léčení cílenou terapii.
EGFR inzerce v exonu 20 (Ex20Ins):
- Amivantamab v kombinaci s chemoterapií karboplatinou a pemetrexedem je indikován k první linii léčby pacientů s pokročilým nemalobuněčným karcinomem plic s aktivační mutací EGFR Ex20Ins.
- Amivantamab v monoterapii* je indikován k léčbě dospělých pacientů s pokročilým nemalobuněčným karcinomem plic s aktivační mutací EGFR Ex20Ins po selhání léčby na bázi platiny.
* K 1. 3. 2026 nebyla v ČR pro amivantamab v monoterapii v léčbě NSCLC s Ex20Ins po selhání systémové léčby stanovena úhrada.
** K 1. 3. 2026 nebyla v ČR pro atezolizumab v kombinaci s bevacizumabem, paklitaxelem a karboplatinou ani pro atezolizumab nebo pembrolizumab v monoterapii po selhání cílené léčby stanovena úhrada.
8.1.4.1.2 Léčba pacientů s prokázanou translokaci genu ALK
- Alektinib je indikován v monoterapii k léčbě dospělých pacientů s pokročilým ALK pozitivním NSCLC v první linii léčby; nebo po předchozí léčbě krizotinibem.
- Brigatinib je indikován v monoterapii k léčbě dospělých pacientů s pokročilým ALK pozitivním NSCLC v první linii léčby; nebo po předchozí léčbě krizotinibem.
- Ceritinib* je indikován v monoterapii k léčbě dospělých pacientů s pokročilým ALK pozitivním NSCLC v první linii léčby; nebo po předchozí léčbě krizotinibem.
- Krizotinib je indikován v monoterapii k léčbě dospělých pacientů s pokročilým ALK pozitivním NSCLC v první linii nebo pacientů již dříve léčených.
- Lorlatinib je indikován v monoterapii k léčbě dospělých pacientů s pokročilým ALK pozitivním NSCLC v první linii léčby; nebo po progresi onemocnění po léčbě alektinibem nebo ceritinibem; nebo po léčbě krizotinibem a nejméně jedním dalším ALK TKI.

Po selhání ALK TKI:
- Standardní volbou po selhání ALK TKI je léčba chemoterapií na bázi platiny.
- Atezolizumab* (bez ohledu na míru exprese PD-L1) v monoterapii nebo v kombinaci s bevacizumabem, paklitaxelem a karboplatinou, může být u pacientů s aktivačními mutacemi EGFR nebo ALK pozitivním NSCLC indikován po selhání vhodných možností cílené léčby.
- Pembrolizumab* v monoterapii je indikován u pacientů s expresí PD-L1 ≥ 1 % a pozitivními nádorovými mutacemi EGFR nebo ALK, kteří musí být předtím léčení cílenou terapii.
* K 1. 3. 2026 nebyla v ČR pro atezolizumab v kombinaci s bevacizumabem, paklitaxelem a karboplatinou ani pro atezolizumab nebo pembrolizumab v monoterapii po selhání cílené léčby stanovena úhrada.
8.1.4.1.3 Léčba pacientů s prokázanou translokací genu ROS1
- Entrektinib je v monoterapii indikován k léčbě dospělých pacientů s ROS1 pozitivním pokročilým NSCLC bez předchozí léčby inhibitory ROS1.
- Krizotinib* v monoterapii je indikován jako léčba dospělých pacientů s ROS1-pozitivním pokročilým NSCLC.
- Repotrektinib* je indikován k léčbě dospělých pacientů s lokálně pokročilým ROS1 pozitivním NSCLC.
*K 1. 3. 2026 nebyla v ČR pro krizotinib a repotrektinib v léčbě ROS1 pozitivních nádorů stanovena úhrada.
8.1.4.1.4 Léčba pacientů s prokázanou alterací genu BRAF
- Enkorafenib* v kombinaci s binimetinibem je indikován k léčbě dospělých pacientů s pokročilým NSCLC s mutací V600E genu BRAF.
- Dabrafenib* v kombinaci s trametinibem je indikován k léčbě dospělých pacientů s pokročilým NSCLC s mutací V600 genu BRAF.
* K 1. 3. 2026 nebyla v ČR pro dabrafenib v kombinaci s trametinibem a enkorafenib v kombinaci s binimetinibem k léčbě BRAFV600E pozitivních NSCLC stanovena úhrada.
8.1.4.1.5 Léčba pacientů s prokázaným fúzním genem NTRK1,2,3
- Entrektinib* je v monoterapii indikován k léčbě dospělých a pediatrických pacientů od 12 let se solidními nádory s fúzí genu neurotrofního tyrosinkinázového receptoru (NTRK), kteří mají lokálně pokročilé, metastazující onemocnění nebo kde chirurgická resekce může vyústit v závažnou morbiditu, nebo kteří neobdrželi předchozí léčbu inhibitorem NTRK, a nebo kteří nemají jiné vhodné možnosti léčby.
- Larotrektinib* je indikován k léčbě dospělých a pediatrických pacientů se solidními nádory, které s fúzní genu NTRK, kteří mají lokálně pokročilé, metastatické onemocnění nebo u nichž by chirurgická resekce pravděpodobně vedla k závažné morbiditě a pro které neexistují uspokojivé možnosti léčby.
- Repotrektinib* je indikován k léčbě dospělých a pediatrických pacientů od 12 let se solidními nádory s fúzí genu NTRK ve stádiu metastatickém nebo lokálně pokročilém u nichž by chirurgická resekce vedla k závažné morbiditě, u kterých došlo k progresi onemocnění po přechozí onkologické léčbě nebo pro ně neexistuje uspokojivá léčebná alternativa.
* K 1. 3. 2026 nebyla v ČR pro larotrektinib, entrektinib a repotrektinib u pacientů s nádory s prokázaným fúzním genem NTRK stanovena úhrada.
8.1.4.1.6 Léčba pacientů s prokázanou fúzí genu RET
- Selperkatinib je indikován k léčbě dospělých pacientů s pokročilým NSCLC s pozitivitou RET fúze v první linii léčby nebo po předchozí léčbě imunoterapií a/ nebo chemoterapií založenou na platině.
8.1.4.1.7 Léčba u pacientů s prokázanou mutací genu KRAS p.G12C
- Adagrasib* je indikován k léčbě dospělých pacientů s pokročilým NSCLC s prokázanou mutací KRAS p.G12C po alespoň jedné předchozí linii systémové léčby.
- Sotorasib je indikován k léčbě dospělých pacientů s pokročilým NSCLC s prokázanou mutací KRAS p.G12C po alespoň jedné předchozí linii systémové léčby.
* K 1. 3. 2026 nebyla v ČR pro adagrasib u pacientů s prokázanou mutací KRAS p.G12C stanovena úhrada.
8.1.4.1.8 Léčba u pacientů s prokázanou skipping mutací exonu 14 v genu MET
- Kapmatinib* je indikován v monoterapii k léčbě dospělých pacientů s pokročilým NSCLC s prokázanou mutací METex14 po předchozí léčbě imunoterapií a/nebo chemoterapií založené na platině.
- Tepotinib je indikován v monoterapii k léčbě dospělých pacientů s pokročilým NSCLC s prokázanou mutací METex14 v první linii léčby nebo po předchozí léčbě imunoterapií a/nebo chemoterapií založené na platině.
* K 1. 3. 2026 nebyla v ČR pro léčbu kapmatinibem stanovena úhrada.
8.1.4.1.9 Léčba pacientů s prokázanou aktivační mutací HER2
- Trastuzumab deruxtekan* je indikován k léčbě dospělých pacientů s pokročilým NSCLC s prokázanou aktivační mutací HER2 po předchozí léčbě imunoterapií a/nebo chemoterapií založené na platině.
* K 1. 3. 2026 nebyla v ČR pro léčbu trastuzumabem deruxtecanem stanovena úhrada.
8.1.4.2 Léčba pacientů bez průkazu řídících mutací
Vzhledem k registraci a úhradě imunoterapie inhibitory kontrolních bodů (check-point inhibitorů), kdy některé indikace vyžadují potvrzení přítomnosti nebo určité výše exprese ligandu PD-L1, je doporučeno provádět reflexní testování této exprese u skvamózních i neskvamózních NSCLC.
U oligometastatických pacientů je na zvážení MDT doplnění systémové léčby o lokoregionální terapii.
V případě užití platinového doubletu u pacientů nad 75 let je preferováno využití carboplatiny.
U všech pacientů by k celkové léčbě měla být časně zařazena léčba podpůrná. Pro pacienty s ECOG PS 0-2 platí doporučení viz níže (s tím, že dostupnost imunoterapie je obvykle omezena na ECOG PS 0-1), pro pacienty s ECOG PS 3-4 volíme obvykle symptomatický postup.
8.1.4.2.1 První linie léčby u pacientů s neskvamózním NSCLC
Imunomonoterapie u PD-L1 exprese ≥ 50 %:
- Atezolizumab v monoterapii je indikován k první linii léčby dospělých pacientů s metastazujícím NSCLC, kteří mají nádory s expresí PD-L1 na ≥ 50 % nádorových buňkách (TC) nebo ≥ 10 % na tumor infiltrujících imunitních buňkách (IC) a kteří nemají NSCLC s mutacemi EGFR nebo přestavbami ALK.
- Cemiplimab* v monoterapii je indikován v první linii léčby dospělých pacientů s nemalobuněčným karcinomem plic (NSCLC) exprimujícím PD-L1 (na ≥ 50 % nádorových buňkách), bez aberací EGFR, ALK nebo ROS1, kteří mají lokálně pokročilý NSCLC a nejsou vhodní k definitivní chemoradiaci, nebo metastazující NSCLC
- Pembrolizumab je v monoterapii indikován v první linii k léčbě metastazujícího neskvamózního NSCLC u dospělých, jejichž nádory exprimují PD-L1, se skóre nádorového podílu (tumour proportion score – TPS) ≥ 50 % bez pozitivních nádorových mutací EGFR nebo ALK.
- Tislelizumab* je indikován, v kombinaci s chemoterapií obsahující pemetrexed a platinu, jako první linie léčby dospělých pacientů s nespinocelulárním NSCLC, jejichž nádory mají expresi PD-L1 na ≥ 50 % nádorových buněk bez pozitivních mutací EGFR nebo ALK a kteří mají lokálně pokročilý NSCLC a nejsou vhodní pro chirurgickou resekci nebo chemoradiaci s platinou nebo mají metastazující NSCLC.
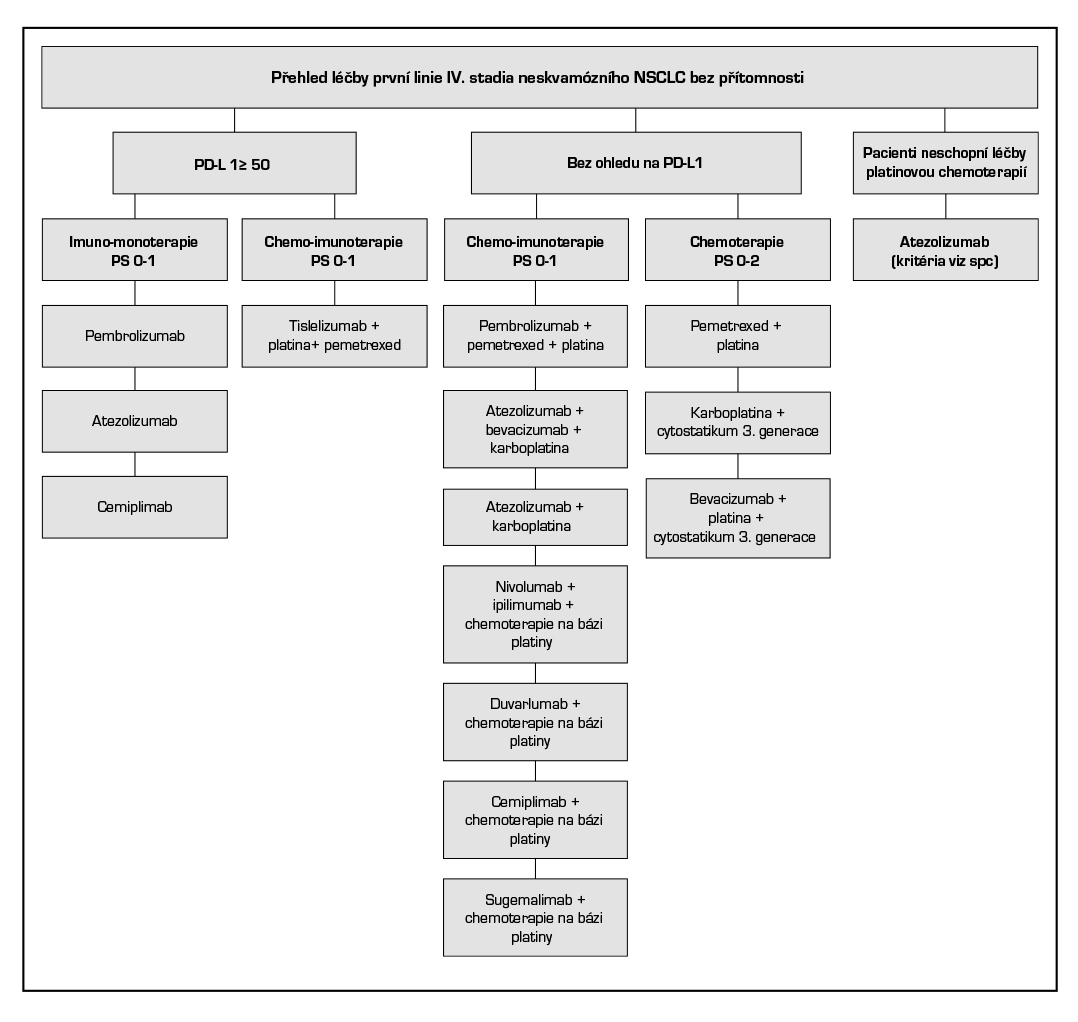
Imunochemoterapie bez ohledu na expresi PD-L1:
- Atezolizumab* v kombinaci s bevacizumabem, paklitaxelem a karboplatinou je indikován k první linii léčby dospělých pacientů s metastazujícím neskvamózním NSCLC. U pacientů s aktivačními mutacemi EGFR nebo ALK pozitivním NSCLC je v této kombinaci indikován až po selhání vhodných možností cílené léčby.
- Atezolizumab* v kombinaci s nab-paklitaxelem a karboplatinou je indikován k první linii léčby dospělých pacientů s metastazujícím neskvamózním NSCLC bez aktivačních mutací EGFR nebo bez přestavby ALK.
- Cemiplimab* je v kombinaci s chemoterapií na bázi platiny indikován v první linii léčby dospělých pacientů s NSCLC exprimujícím PD-L1 (u ≥1 % nádorových buněk) bez aberací EGFR, ALK nebo ROS1, kteří mají lokálně pokročilý NSCLC a nejsou vhodní k definitivní chemoradiaci, nebo mají metastazující NSCLC.
- Durvalumab je v kombinaci s tremelimumabem* a chemoterapií na bázi platiny indikován k první linii léčby dospělých pacientů s metastatickým NSCLC bez senzitizujících mutací EGFR nebo přítomnosti mutací ALK.
- Nivolumab** je v kombinaci s ipilimumabem a dvěma cykly chemoterapie na bázi platiny indikován k léčbě metastazujícího nemalobuněčného karcinomu plic v první linii u dospělých s nádory bez senzitizující mutace EGFR nebo translokace ALK.
- Pembrolizumab je v kombinaci s chemoterapií pemetrexedem a platinou indikován v první linii k léčbě metastazujícího neskvamózního NSCLC u dospělých, jejichž nádory nevykazují pozitivní mutace EGFR nebo ALK.
- Sugemalimab* je v kombinaci s chemoterapií na bázi platiny indikován v první linii léčby dospělých s metastazujícím nemalobuněčným karcinomem plic (NSCLC) bez senzibilizujících mutací EGFR a bez aberací genomu ALK, ROS1 nebo RET.
- Atezolizumab* je indikován v monoterapii v první linii léčby pacientů, kteří nejsou způsobilí k léčbě chemoterapií na bázi platiny, kritéria na základě ECOG, věku či komorbidit viz. spc (studie IPSOS, median OS 10,3 vs. 9,2 měsíců; HR: 0,78 [0·63–0·97]).
* K 1. 1. 2026 v České republice nebylo o úhradě rozhodnuto.
** Kombinace ipilimumab, nivolumab a 2 cykly chemoterapie jsou hrazeny u pacientů s expresi PD-L1 0–49 %.
Chemoterapie při kontraindikaci imunoterapie
U nemocných s neskvamózním NSCLC bez aktivační mutace je pak dalším rozhodovacím kritériem nepřítomnost kontraindikace podávání bevacizumabu, který je možno podat s chemoterapeutickým režimem založeným na platinovém derivátu.
Základem chemoterapie u nemocných s neskvamózním NSCLC bez aktivační mutace je obvykle platinový derivát (cisplatina, karboplatina) + lék s prokázanou účinností u NSCLC (vinorelbin, gemcitabin, paklitaxel, docetaxel, pemetrexed). Cisplatinu není vhodné podávat u těchto pacientů: kreatininová clearance <60 ml/min., srdeční selhávání NYHA class II-III, ztráta sluchu> G2.
U pacientů kontraindikovaných k léčbě platinovým doubletem (zejména z důvodu horšího výkonnostního stavu pacienta) je indikována monochemoterapie. Ev. je možné použít metronomickou terapii vinorelbinem (50 mg 3× týdně, jeden cyklus léčby jsou 3 týdny, do progrese onemocnění, nebo do neakceptovatelné toxicity).
8.1.4.2.2 První linie léčby u pacientů se skvamózním NSCLC
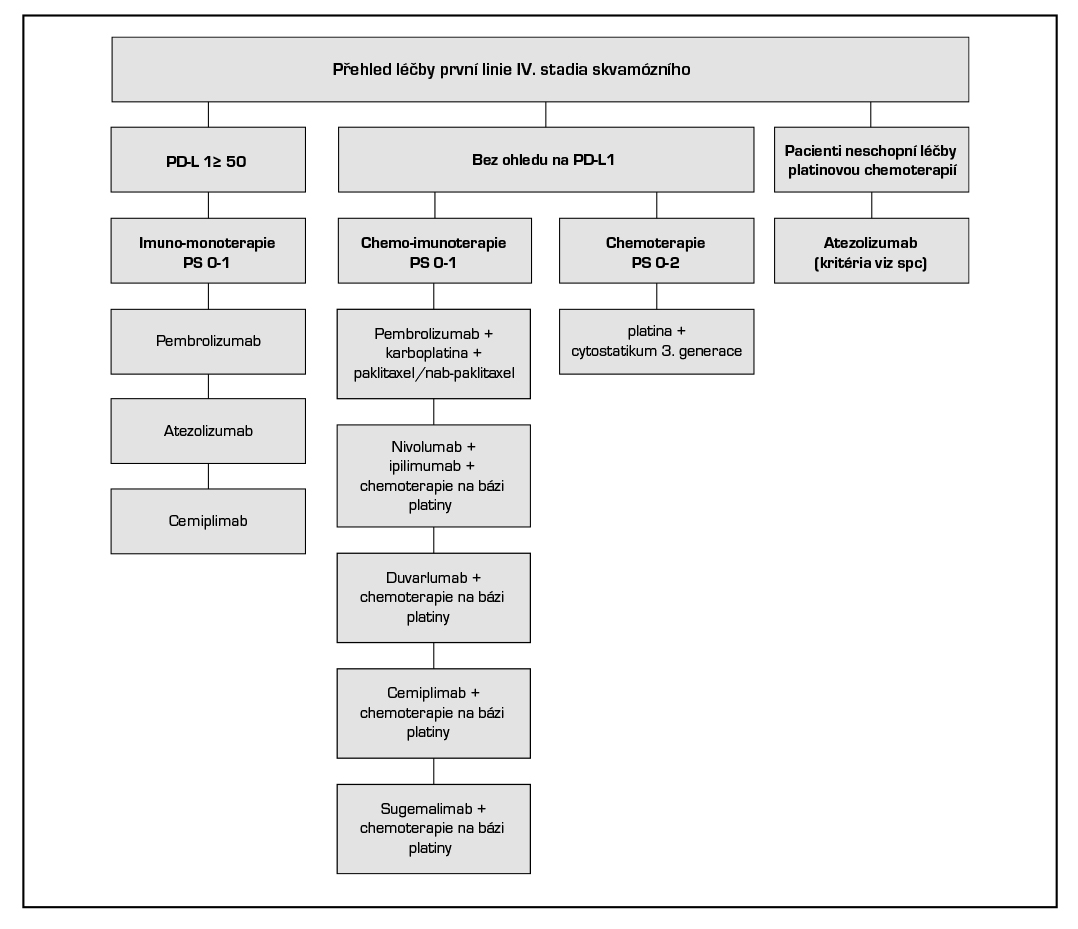
Imunomonoterapie u PD-L1 exprese ≥ 50 %:
- Atezolizumab v monoterapii je indikován k první linii léčby dospělých pacientů s metastazujícím NSCLC, kteří mají nádory s expresí PD-L1 na ≥ 50 % nádorových buňkách (TC) nebo ≥ 10 % na tumor infiltrujících imunitních buňkách (IC) a kteří nemají NSCLC s mutacemi EGFR nebo přestavbami ALK.
- Cemiplimab* v monoterapii je indikován v první linii léčby dospělých pacientů s nemalobuněčným karcinomem plic (NSCLC) exprimujícím PD-L1 (u ≥ 50 % nádorových buněk), bez aberací EGFR, ALK nebo ROS1, kteří mají lokálně pokročilý NSCLC a nejsou vhodní k definitivní chemoradiaci, nebo metastazující NSCLC.
- Pembrolizumab v monoterapii je indikován v první linii k léčbě metastazujícího skvamózního NSCLC u dospělých, jejichž nádory exprimují PD-L1, se skóre nádorového podílu (tumour proportion score – TPS) ≥ 50 % bez pozitivních nádorových mutací EGFR nebo ALK.
Imunochemoterapie bez ohledu na expresi PD-L1:
- Cemiplimab* je v kombinaci s chemoterapií na bázi platiny indikován v první linii léčby dospělých pacientů s NSCLC exprimujícím PD-L1 (u ≥1 % nádorových buněk) bez aberací EGFR, ALK nebo ROS1, kteří mají lokálně pokročilý NSCLC a nejsou vhodní k definitivní chemoradiaci, nebo mají metastazující NSCLC.
- Durvalumab v kombinaci s tremelimumabem*** a chemoterapií na bázi platiny je indikován k první linii léčby dospělých pacientů s metastatickým NSCLC bez senzibilizujících mutací EGFR nebo přítomnosti mutací ALK.
- Nivolumab** je indikován v kombinaci s ipilimumabem a dvěma cykly chemoterapie na bázi platiny k léčbě metastazujícího nemalobuněčného karcinomu plic v první linii u dospělých s nádory bez senzitizující mutace EGFR nebo translokace ALK.
- Pembrolizumab** je v kombinaci s karboplatinou a paklitaxelem nebo nab-paklitaxelem indikován v první linii k léčbě metastazujícího skvamózního NSCLC u dospělých.
- Sugemalimab* je v kombinaci s chemoterapií na bázi platiny indikován v první linii léčby dospělých s metastazujícím nemalobuněčným karcinomem plic (NSCLC) bez senzibilizujících mutací EGFR a bez aberací genomu ALK, ROS1 nebo RET.
- Tislelizumab* je indikován, v kombinaci s karboplatinou a paklitaxelem nebo nab-paklitaxelem, jako první linie léčby dospělých pacientů se spinocelulárním NSCLC, kteří mají: lokálně pokročilý NSCLC a nejsou vhodní pro chirurgickou resekci nebo chemoradiaci s platinou nebo mají metastazující NSCLC.
- Atezolizumab* je indikován v monoterapii v první linii léčby pacientů, kteří nejsou způsobilí k léčbě chemoterapií na bázi platiny, kritéria na základě ECOG, věku či komorbidit viz. spc (studie IPSOS, median OS 10,3 vs. 9,2 měsíců; HR: 0,78 [0·63–0·97]).
* K 1. 1. 2026 v České republice nebylo o úhradě rozhodnuto.
** Pembrolizumab v kombinaci s chemoterapií a nivolumab v kombinaci s ipilimumabem a 2 cykly chemoterapie jsou hrazeny jen u pacientů s expresí PD-L1 TPS 0–49 %.
Chemoterapie při kontraindikaci imunoterapie
U nemocných se skvamózním typem NSCLC, u kterých není indikována cílená léčba ani imunoterapie je základem chemoterapie. Obvykle platinový derivát (cisplatina, karboplatina) + lék s prokázanou účinností u NSCLC (vinorelbin, gemcitabin, paklitaxel, docetaxel). Doporučuje se podat 4–6 cyklů, po 2. cyklu je nutné přešetření k posouzení efektu léčby. Cisplatinu není vhodné podávat u těchto pacientů: kreatininová clearance <60 ml/min., srdeční selhávání NYHA class II-III, ztráta sluchu> G2.
U pacientů kontraindikovaných k léčbě platinovým doubletem (zejména z důvodu horšího výkonnostního stavu pacienta) je indikována monochemoterapie. Ev. je možné použít metronomickou terapii vinorelbinem (50 mg 3× týdně, jeden cyklus léčby jsou 3 týdny, do progrese onemocnění, nebo do neakceptovatelné toxicity).
8.1.4.2.3 Udržovací léčba
V České republice mají stanovenou úhradu v této indikaci pemetrexed a bevacizumab. Pemetrexed je hrazen v monoterapii v rámci udržovací fáze léčby lokálně pokročilého nebo metastazujícího karcinomu plic histologického typu adenokarcinomu nebo velkobuněčného karcinomu do progrese onemocnění u pacientů o výkonnostním stavu ECOG 0-1, kteří po 4 cyklech léčby 1. linie kombinací pemetrexedu a cisplatiny dosáhli objektivní odpovědi nebo stabilizace onemocnění. Léčba je hrazena do progrese onemocnění. Po skončení chemoterapie s bevacizumabem se pokračuje v monoterapii bevacizumabem do progrese nemoci, pokud při ukončení chemoterapie byla prokázána parciální remise nebo stabilizace onemocnění. Tato udržovací léčba je indikována i při kombinaci s imunoterapií.
8.1.4.2.4 Druhá a další linie léčby u pacientů bez řídících mutací
Standardem léčby pacientů (mužů a žen) starších 18 let se skvamózním i neskvamózním nemalobuněčným karcinomem plic progredujícím po předchozí systémové terapii na bázi platiny je terapie checkpoint inhibitory, pokud nebyly podány v první linii. U pacientů bez ohledu na výši exprese PD-L1 je indikován nivolumab nebo atezolizumab v monoterapii. U pacientů s expresi PD-L1 ≥1 % pembrolizumab* v monoterapii. U vhodně indikovaných nemocných je prokázáno prodloužení celkového přežití další linií systémové terapie. Doporučena je monoterapie. Srovnatelnou účinnost prokázal v této indikaci docetaxel (u všech histologických typů) a pemetrexed (pouze u pacientů s nedlaždicobuněčnou histologií), pokud nebyly podány v první linii.
Pokud je zvažován docetaxel u adenokarcinomu, je indikováno podání společně s nintedanibem*, což je perorálním inhibitorem angiogeneze. Dále je v kombinaci s docetaxelem indikován ramucirumab* k léčbě dospělých pacientů s lokálně pokročilým nebo metastazujícím nemalobuněčným karcinomem plic, u kterých po chemoterapii založené na platině došlo k progresi onemocnění.
* K 1. 1. 2026 nebyla v ČR pro pembrolizumab ve 2.a 3. linii stanovena úhrada. Dále není hrazena terapie nintedanibem a ramucirumabem.
8.2 Malobuněčný karcinom
8.2.1 Limitované i extenzivní onemocnění
Ve stadiu limitovaném prodlužuje přežití přidání radioterapie, ideálně co nejdříve po zahájení chemoterapie. Pro konkomitantní chemoradioterapii nelze použít režimy s antracykliny. U nemocných neprogredujících na I. linii terapie je ve stadiu limitovaném i extensivním indikováno preventivní ozáření neurokrania, případně lze při použití imunoterapie zvážit sledování pomocí MRI, což se týká především extensivního stadia. Ve stadiu extensivním je rovněž možné zvolit ozáření nitrohrudního residua, pokud došlo ke kompletní remisi nebo velmi dobré parciální remisi mimohrudních metastáz.
Chirurgie: Za předpokladu vyloučení vzdálených metastáz (MR mozku, PET/CT) a vyloučení postižení N+ uzlin extenzivním stagingovým bioptickým vyšetřením (EBUS, EUS ev. videomediastinoskopie) jsou k chirurgické resekci, tj. lobektomii se systematickou lymfadenektomií indikováni vybraní pacienti ve stadiu I–IIA (T1–2N0M0). Vždy následuje adjuvantní chemoterapie, při patologickém nálezu N2 nebo R1, R2 v kombinaci s radioterapií. Pacienti klinického stádia I-III, kteří jsou schopni podstoupit protinádorovou léčbu, by jednoznačně měli být prezentováni v rámci MDT KOC.
8.2.2 Použitá systémová léčba a délka léčby
Jsou indikovány přípravky s prokázanou účinností u malobuněčného karcinomu plic. Počet cyklů chemoterapie je zpravidla 4–6. Do léčebného schématu neodmyslitelně patří imunoterapie. Imunoterapie je v extenzivním stadiu podávána do progrese onemocnění nebo do vzniku nepřijatelné toxicity. Příklady doporučených kombinací viz tabulka 8.6.6.
- Atezolizumab v kombinaci s karboplatinou a etoposidem, následně podávaný jako udržovací monoterapie, je indikován k první linii léčby dospělých pacientů s extenzivním stadiem malobuněčného karcinomu plic (extensi- ve-stage small cell lung cancer, ES-SCLC) na základě výsledků studie IMpower133.
- Durvalumab má indikaci u extenzivního i limitovaného klinického stádia:
- Durvalumab v kombinaci s etoposidem a karboplatinou nebo cisplatinou, následně podávaný jako udržovací monoterapie, je indikován k první linii léčby dospělých pacientů s malobuněčným karcinomem plic v extenzivním stadiu (extensive-stage small cell lung cancer, ES-SCLC) dle studie CASPIAN.
- Durvalumab* je indikován jako konsolidační léčba u dospělých pacientů s malobuněčným karcinomem plic v limitovaném stadiu (limited-stage SCLC, LS-SCLC), kteří neprogredovali po dokončení konkomitantní chemoradioterapie (cCRT). V této indikaci vycházející ze studie ADRIATIC se podává maximálně po dobu 24 měsíců. - Serplulimab** je v kombinaci s karboplatinou a etoposidem a následně jako udržovací monoterapie indikován k první linii léčby dospělých pacientů s extenzivním stadiem malobuněčného karcinomu plic (ES-SCLC). (Studie ASTRUM-005)
*K 1. 3. 2026 nebyla v ČR pro durvalumab k léčbě LS-SCLC stanovena úhrada.
**K 1. 3. 2026 nebyla v ČR pro serplulimab k léčbě ES-SCLC stanovena úhrada.
8.2.3 Volba léčby v II. linii SCLC:
U nemocných s objektivní léčebnou odpovědí trvající alespoň 3 měsíce a s následným relapsem zjištěným nejméně po 3 měsících od ukončení chemoterapie I. linie je možno použít stejnou chemoterapii jako v I. linii, tedy platinový derivát a etoposid.
U nemocných, u kterých nebylo dosaženo objektivní léčebné odpovědi I. linií léčby nebo s relapsem v období kratším než 3 měsíce od skončení léčby I. linií je v II. linii nutno podat jiný chemoterapeutický režim.
8.3 Maligní mezoteliom pleury
Pečlivě selektovaní pacienti s maligním mesoteliomem pleury mohou být léčeni chirurgickou terapií se snahou o kompletní odstranění nádorové tkáně (jen jako součást multimodalitní terapie ve špičkových centrech). Operace není doporučována v případě TNM stádia IV, T4, N2 nemoci, u nádorů se sarkomatoidní histologií (či predominantně sarkomatoidní). Operace spočívá buď v extrapleurální pneumonektomii (EPP) nebo pleurektomii/dekortikaci (P/D). EPP spočívá v pneumonektomii současně s kompletní resekcí pleury, perikardu a příslušnou polovinou bránice doplněnou systematickou mediastinální lymfadenektomií. P/D znamená kompletní resekci viscerální i parietální pleury, v případě extenzivnějšího výkonu (EP/D) ještě i s resekcí perikardu a poloviny bránice. Je preferována spíše P/D či EP/D, ale efektivita chirurgických metod je nejasná, slibně se jeví kombinace P/D s hypertermickou intraoperační chemoterapií (HITHOC). Standardní kombinace pro 1. linii je cisplatina + pemetrexed.
Nivolumab* je indikován v kombinaci s ipilimumabem k léčbě neresekovatelného maligního mezoteliomu pleury u nepředléčených dospělých pacientů.
Pembrolizumab* v kombinaci s chemoterapií, pemetrexedem a platinou je indikován v první linii léčby dospělých pacientů s neresekovatelným jiným než epiteloidním mezoteliomem pleury.
* K 1. 3. 2026 nebyla v ČR pro nivolumab s ipilimumabem, pembrolizumab* v kombinaci s chemoterapií stanovena úhrada.
8.4 Thymom, thymický karcinom
U časných stadií thymomu s nebo bez myastenie je na prvním místě vždy zvažován resekční výkon, doporučována je totální thymektomie (s preferencí miniinvazivních technik – VATS či RATS). V případě pokročilých resekabilních stadií je nezbytný sternotomický přístup. V případě primárně inoperabilního, resp. potenciálně hraničně operabilního thymomu či thymického karcinomu (Masaoka-Koga III-IV) je indikována neoadjuvantní chemoterapie s následnou snahou o kompletní resekci, v indikovaných případech včetně resekce velkých cév. Adjuvantní radioterapie je zvažována od II. stádia (transkapsulární invaze).
V případě R1 resekce je indikována pooperační radioterapie, ev. v kombinaci s chemoterapií u thymického karcinomu.
V případě R2 resekce je indikována definitivní chemoradioterapie.
V případě lokálně pokročilých stádií, která nejsou indikována k operaci, je indikována konkomitantní chemo-radioterapie.
V případě metastatického postižení je indikována chemoterapie.
Doporučené režimy chemoterapie – viz tabulka 8.6.7.
Sledování po léčbě: CT hrudníku každých 6 měsíců po dobu 2 let, následně 1× ročně po dobu 5 let u thymického karcinomu a 10 let u thymomu.
8.5 Léčba kostní nádorové choroby
Součástí paliativní léčby kostní nádorové choroby (osteolytických, osteoblastických nebo smíšených kostních metastáz) ve všech liniích léčby jsou léky ovlivňující metabolismus kostí (BMA – bone modifying agents): Indikace, způsob podání, dávka, viz kapitola 27 – Farmakoterapie kostní nádorové nemoci.
8.6 Léčebné přípravky použité v léčbě nádorů plic, maligního mezoteliomu pleury a maligního thymomu a jejich doporučená schémata
Tab. 8.6.1a – neoadjuvantní a adjuvantní chemoterapie, imunoterapie a cílená léčba
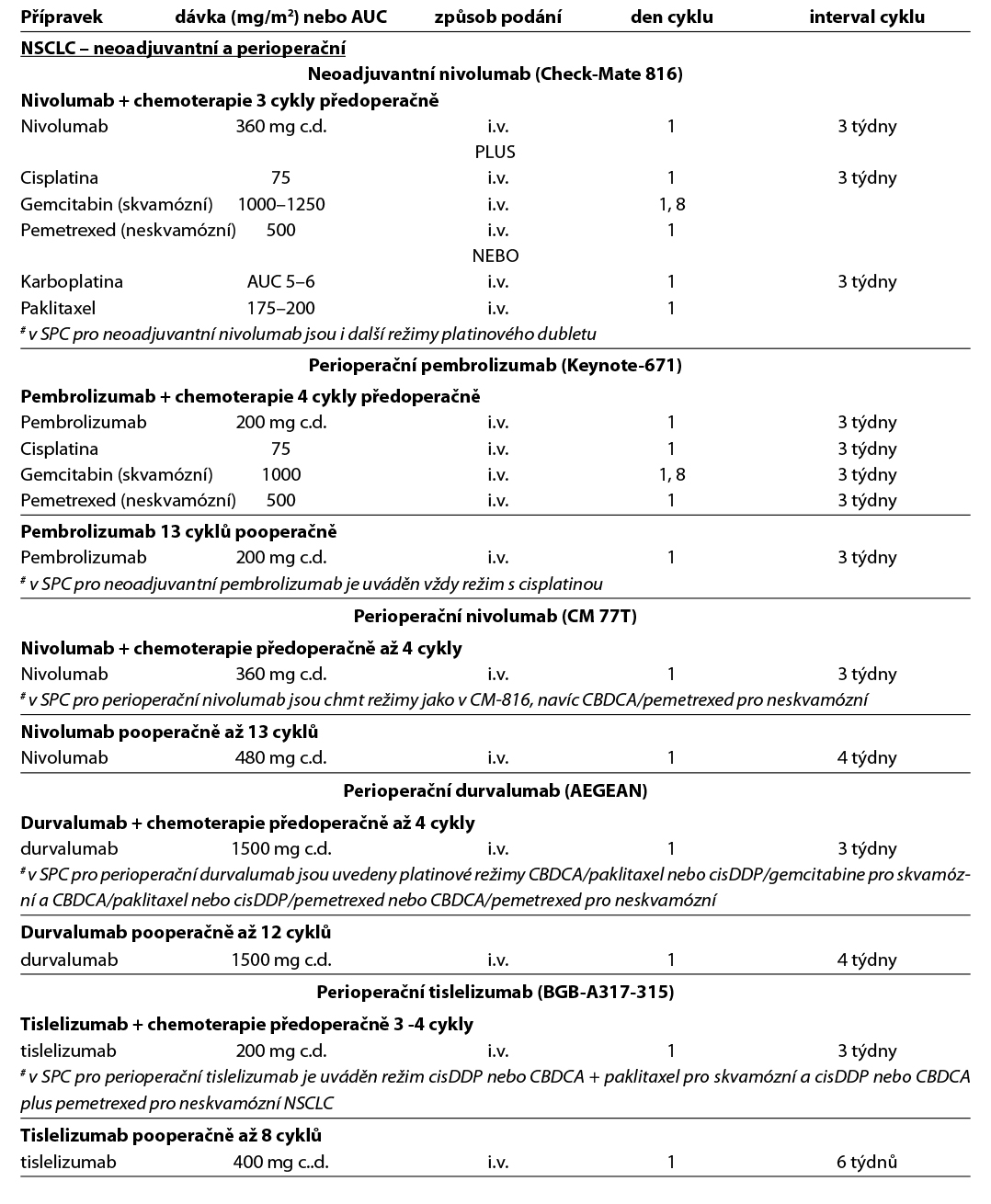
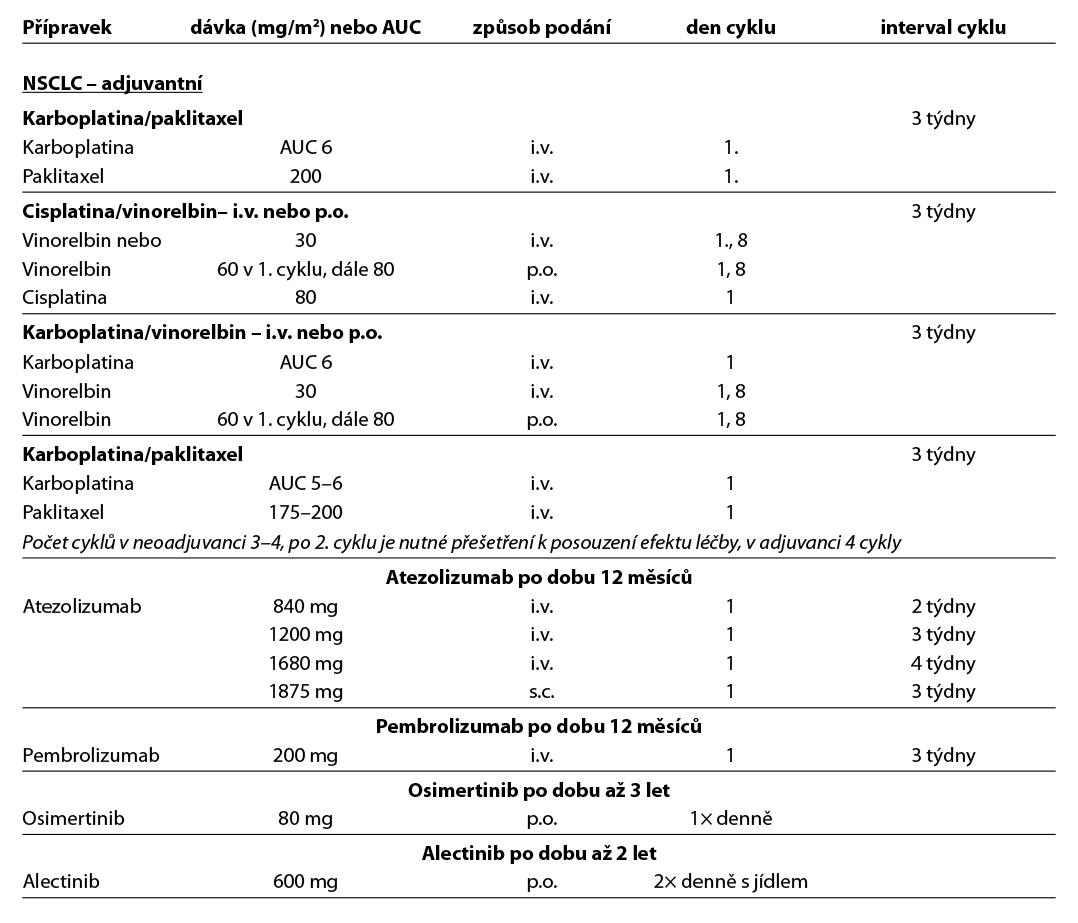
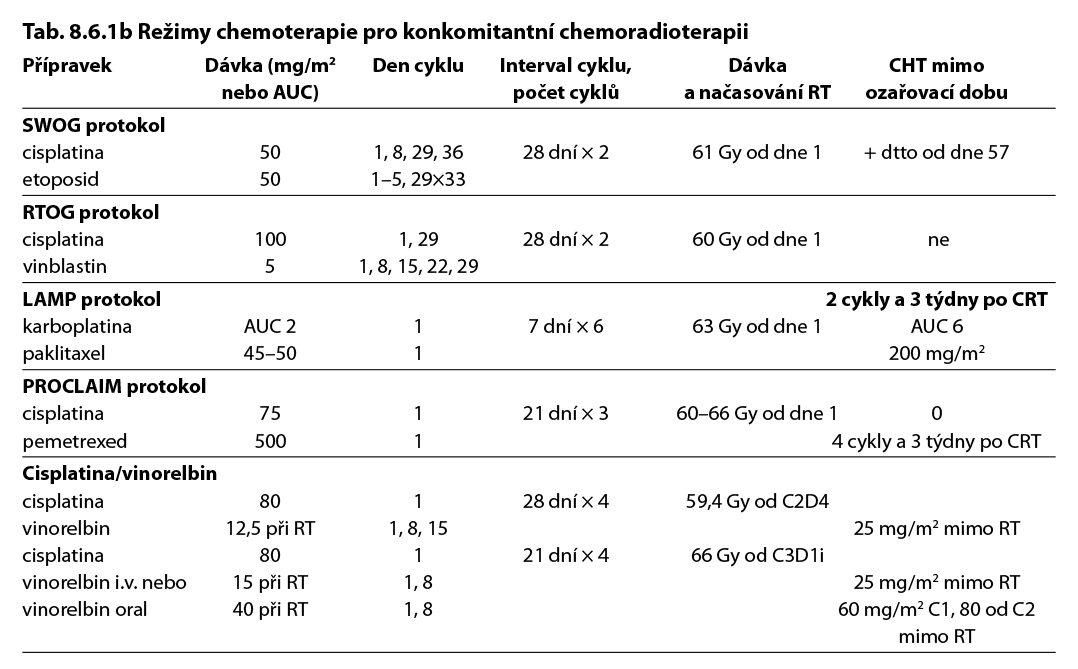
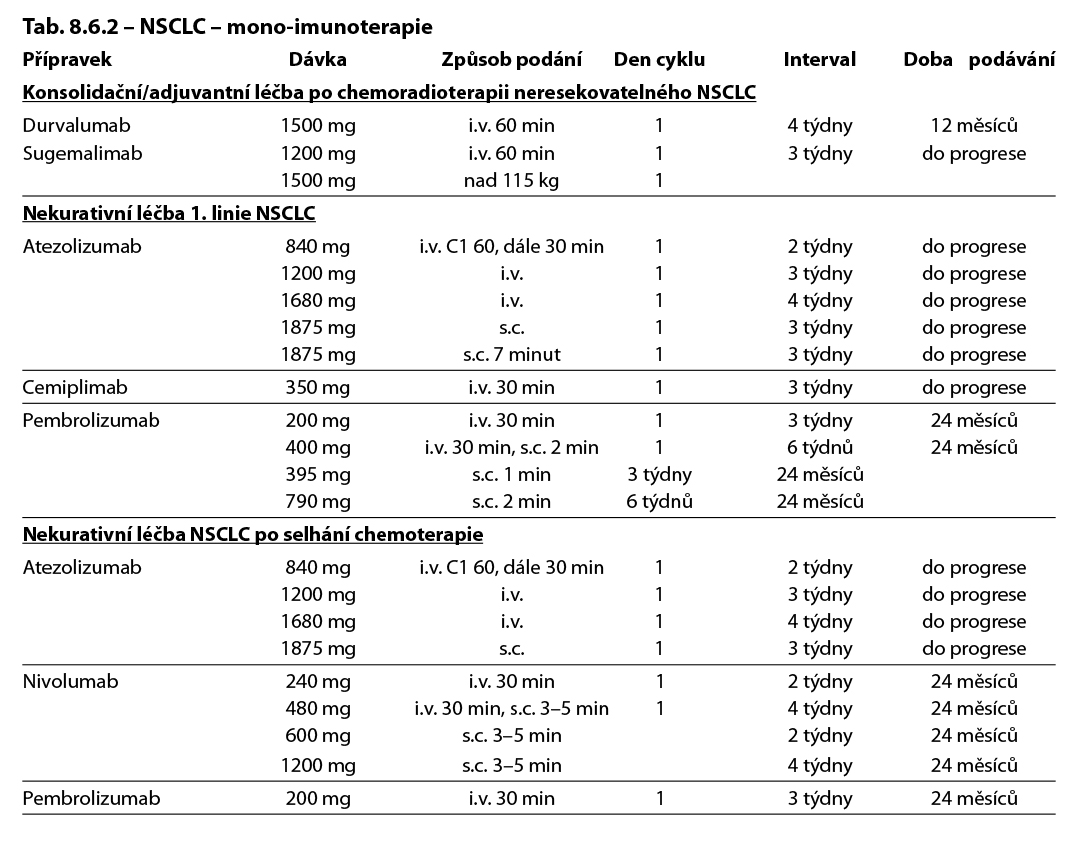
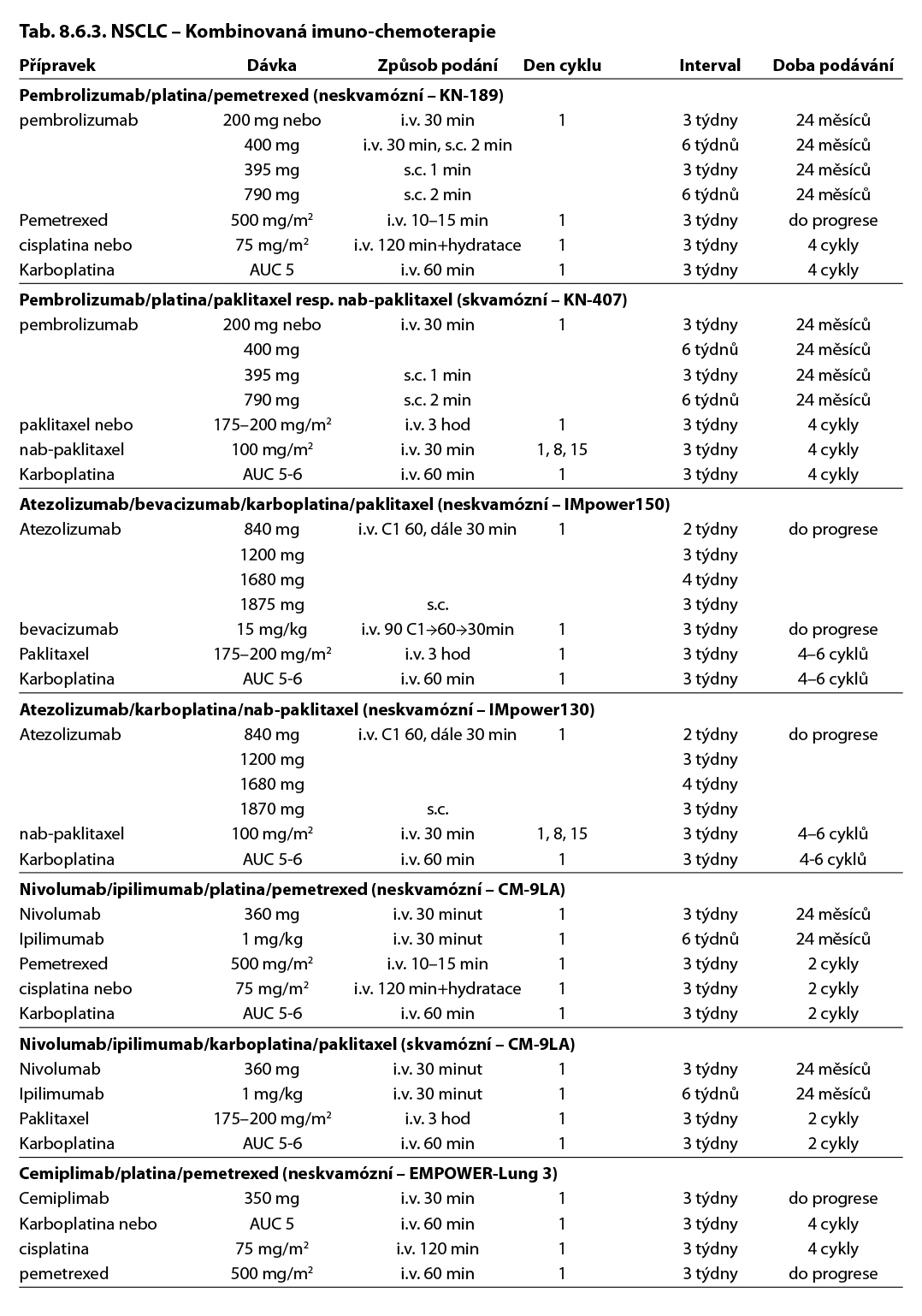
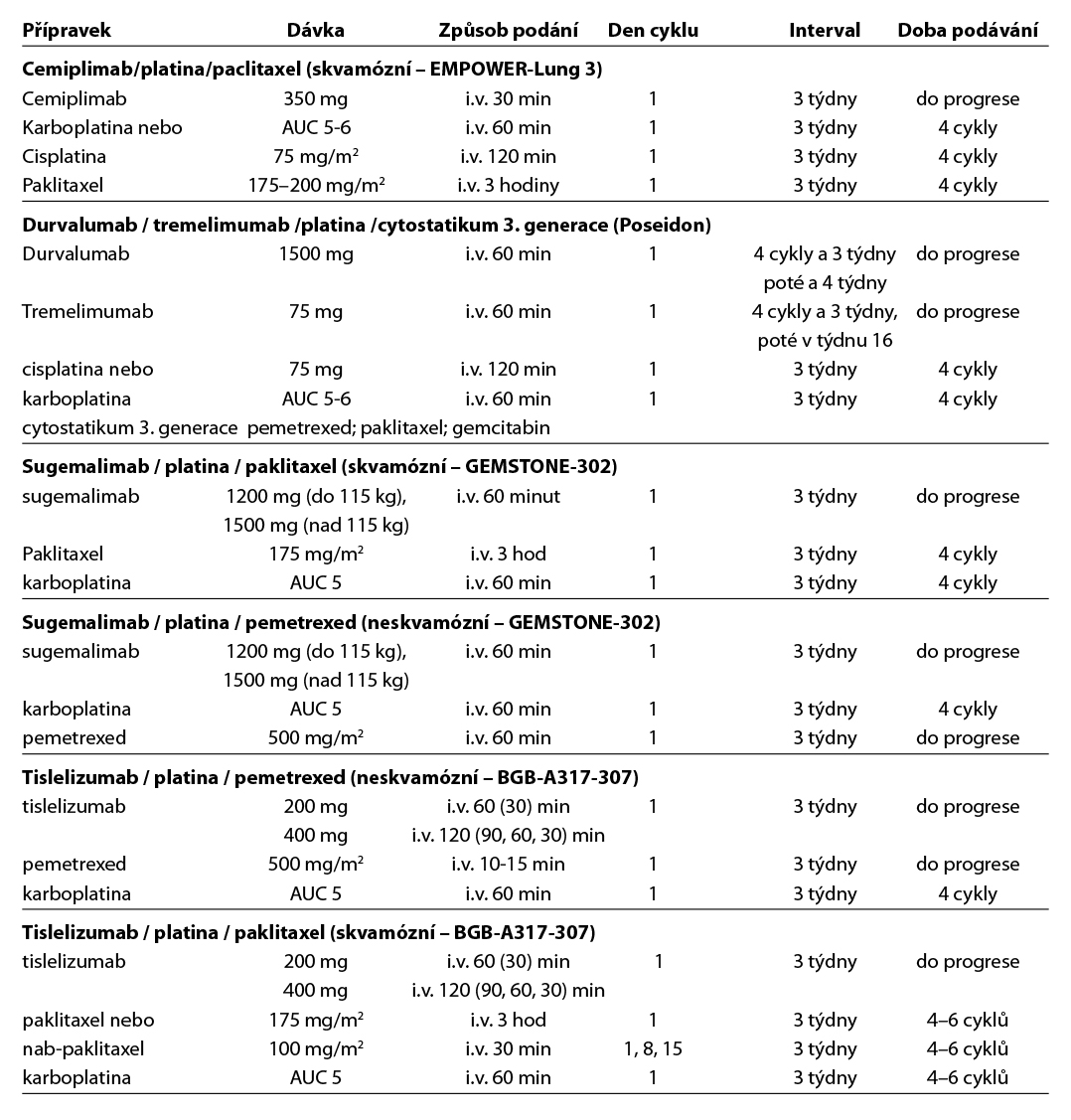
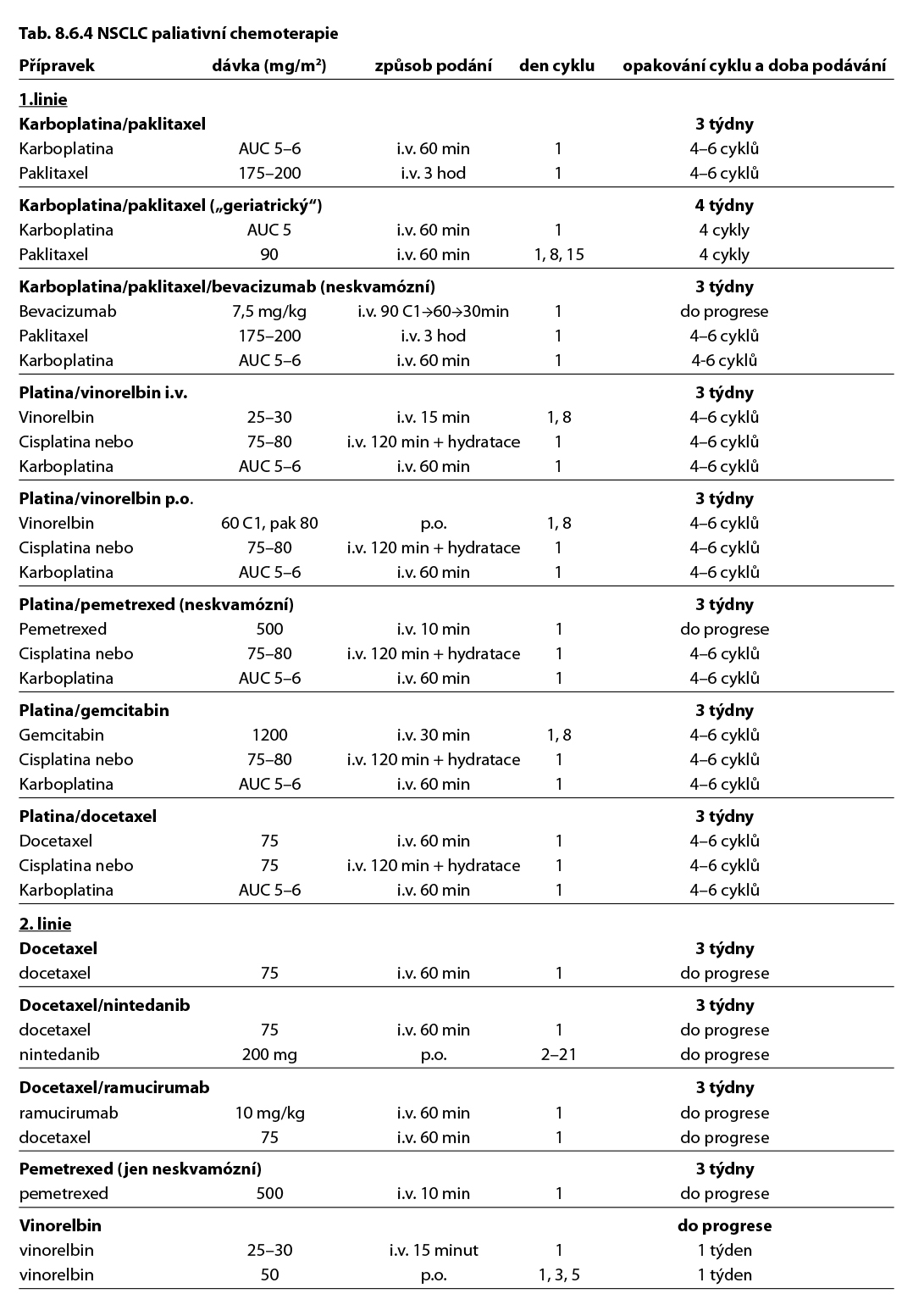
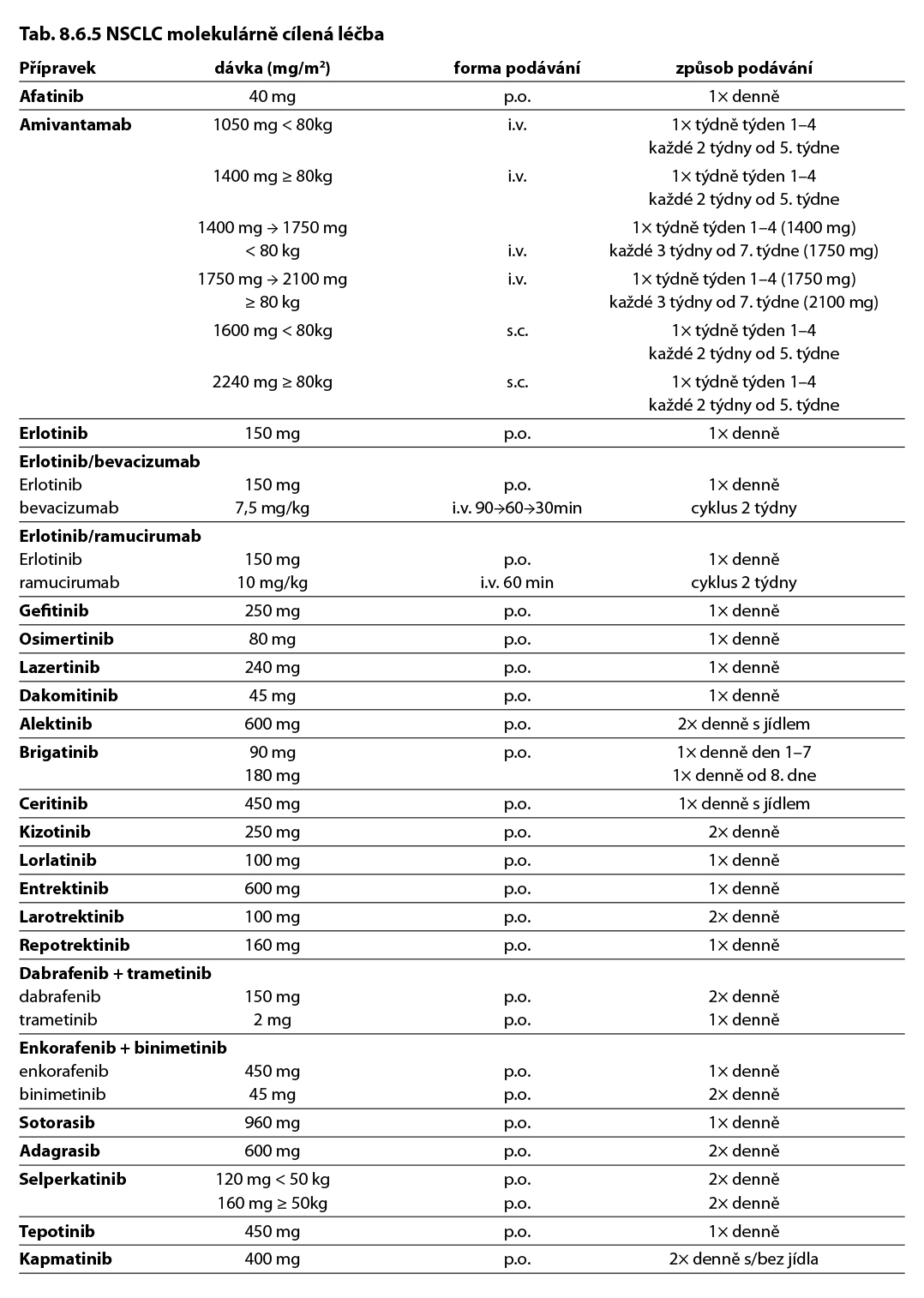
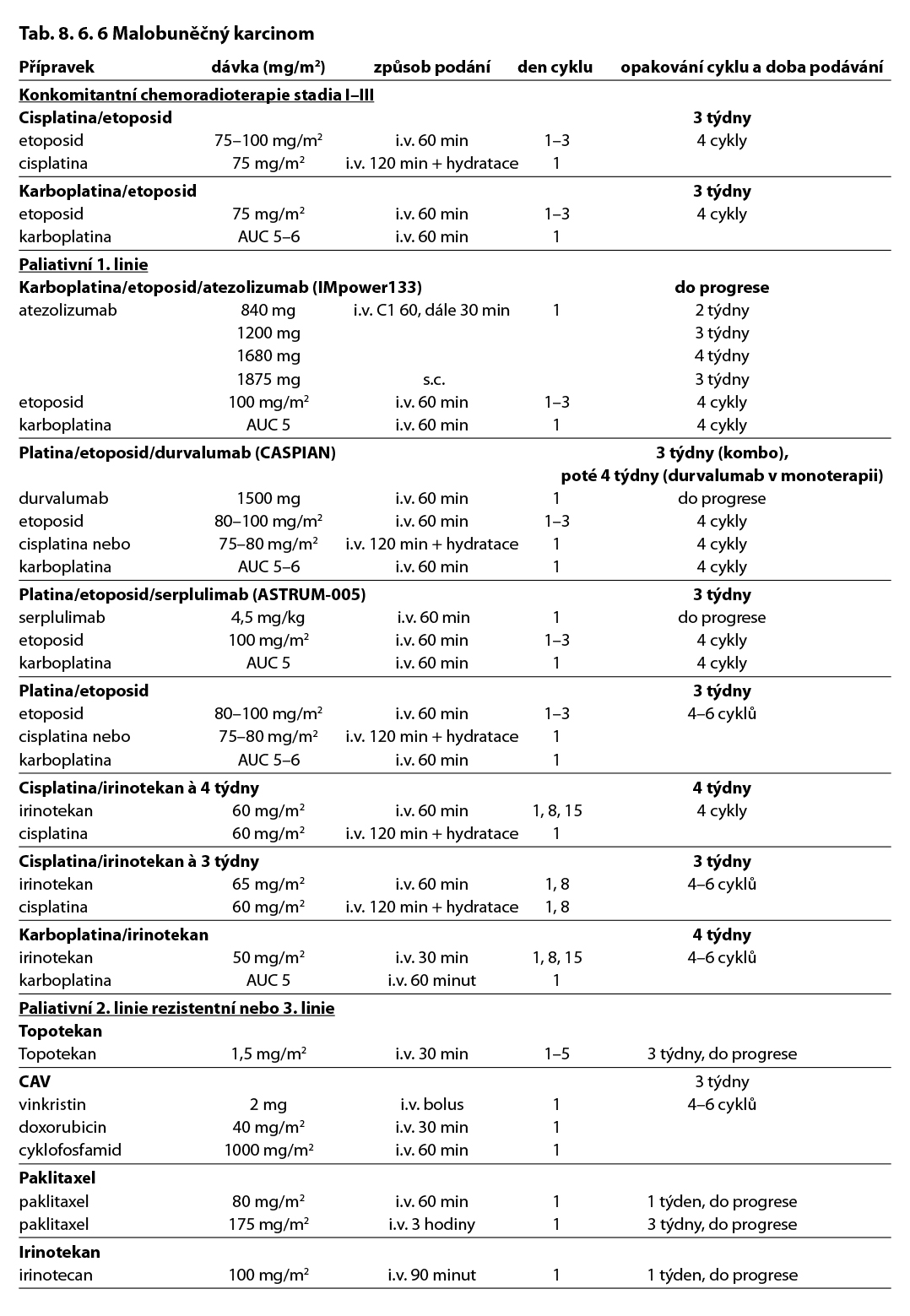
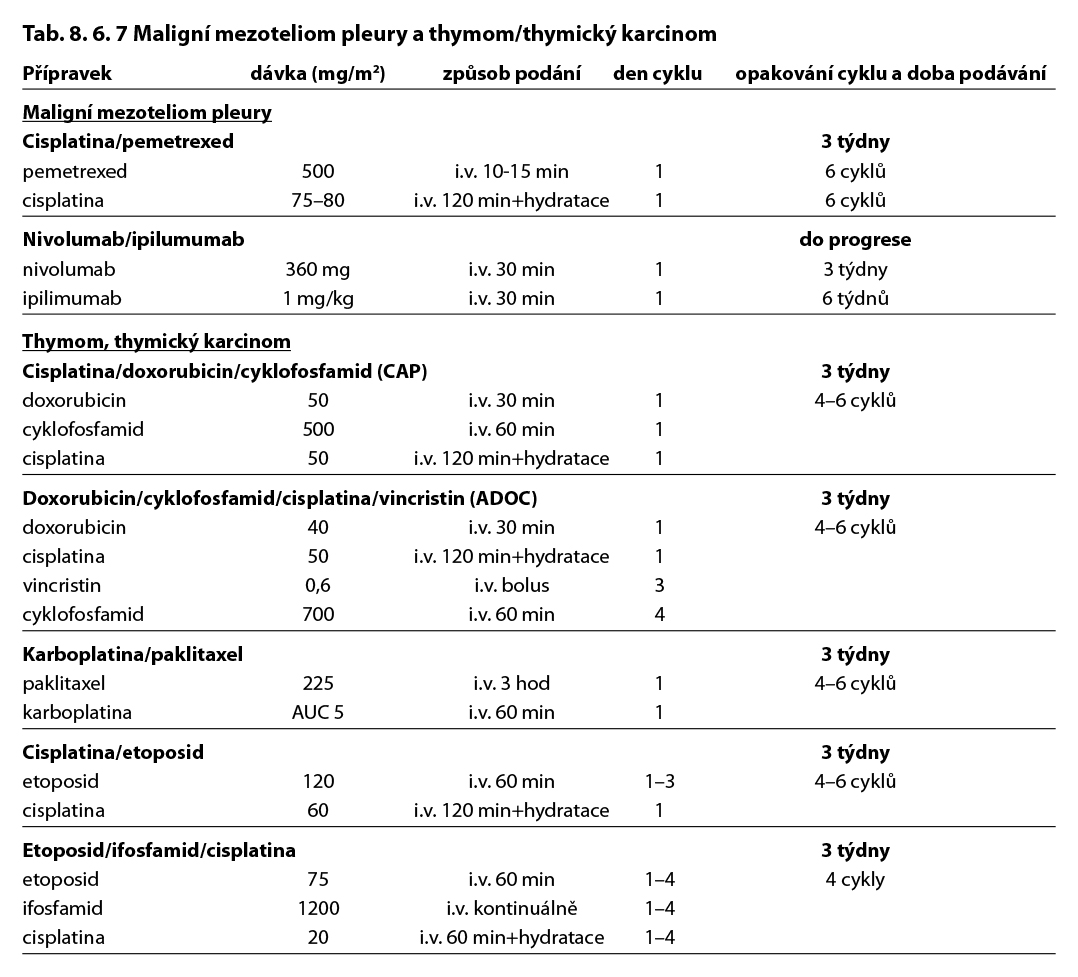
Komentář k léčebným schématům: Uvedená doporučení jsou založená na nejnovějších medicínských poznatcích a nemusí se vždy shodovat s pravidly úhrady léku od plátce péče. Nutno dodržovat aktuální indikační omezení a způsob úhrady stanované SÚKL. www.sukl.cz/modules/medication/search.php
8.7 Sledování nemocných po onkologické léčbě
I po diagnóze rakoviny plic je velmi důležité doporučit abstinenci od kouření včetně pasivní expozice tabákovému kouři. Ovlivní se tak významně doba přežití, účinnost onkologické léčby i kvalita života. Pokud lékař nemá kapacitu, měl by doporučit nejbližší možnost intenzivní léčby závislosti na tabáku. Kontakty jsou např. na webu Společnosti pro léčbu závislosti na tabáku www.slzt.cz: přes 40 center pro závislé na tabáku, cca 200 lékáren poskytujících poradenství, telefonní linka pro odvykání, adiktologické ambulance či mobilní aplikace zdarma. Další weby jsou např. www.koureni-zabiji.cz , www.bezcigaret.cz.
Nejlepší prognózu mají ti nemocní, u nichž byl nádor diagnostikován v operabilním stadiu a provedena úspěšná resekce plicního tumoru. Podíl radikálně operovaných nemocných ze skupiny všech pacientů s nemalobuněčným bronchogenním karcinomem je poměrně nízký a v jednotlivých regionech České republiky může být odlišný. V celé České republice nepřesahuje 20 %. Prognóza u pacientů s neoperabilním lokoregionálně pokročilým onemocněním či generalizovaným onemocněním je i přes aplikovanou léčbu špatná. Medián přežití těchto nemocných obvykle nepřesahuje 18–24 měsíců jde-li o místně pokročilý nádor, à 12–18 měsíců, byl-li v době stanovení diagnózy plicní nádor již diseminovaný. I přes výše uvedené údaje je vhodné sledování nemocných s karcinomem plic po ukončení léčby.
Sledování nemocných s karcinomem plic po ukončení onkologické léčby (dispenzarizace) se týká všech nemocných s karcinomem plic. Patří do rukou pneumologa, který se onkologické problematice věnuje dlouhodobě nebo do rukou klinického onkologa, který má nastavenou spolupráci s pneumologem. V průběhu sledování je potřebná spolupráce s praktickým lékařem, a pokud nebyl nemocný léčen v komplexním onkologickém centru i s klinickým onkologem a pneumologem. Sledování nemocných po ukončené léčbě má za cíl časně odhalit progresi v období, kdy je rozsah nádoru a stav výkonnosti takový, že je možná další léčba. Z publikovaných studií vyplývá, že k zachycení recidivy dochází většinou při klinickém vyšetření. Prodloužení života nebylo při pravidelném sledování prokázáno, ale včasné zahájení léčby při progresi vede k zamezení nebo zpomalení příznaků, které karcinom plic vyvolává. Včasné zachycení progrese umožňuje nejen léčbu chirurgickou, chemoterapii, biologickou léčbu, radioterapii, ale i včasné zahájení léčby paliativní.
Dalším cílem sledování je zachycení jiného, duplicitního nádoru (karcinomu plic nebo nádoru v jiné lokalizaci). Nemocní s karcinomem plic jsou totiž ohroženi vznikem duplicity ve 2–15 %.
V průběhu sledování nemocných s karcinomem plic lze identifikovat i neonkologické problémy, jako jsou komplikace dříve podané nebo provedené léčby, a také souběžná onemocnění, která jsou někdy mylně interpretována jako progrese základního onemocnění.
Po radikální léčbě karcinomu plic je v prvních dvou letech od jejího ukončení doporučeno provádět kontroly po 3–6 měsících s CT vyšetřením každých 6 měsíců, s hematologickým a biochemickým vyšetřením, individuálně s kontrolou nádorových markerů. V průběhu 3. až 5. roku jsou doporučeny kontroly každých 6 měsíců s CT vyšetření jedenkrát ročně.
Literatura:
- NCCN Gudelines version 1.2024 - Non-Small Cell Lung Cancer: www.nccn.org
- NCCN Gudelines version 2.2024 - Small Cell Lung Cancer: www.nccn.org
- NCCN Gudelines version 1.2024 - Malignant Pleural Mesothelioma: www.nccn.org
- NCCN Guidelines version 1.2024 - Thymomas and Thymic Carcinomas: www.nccn.org
- Hendriks L E, Kerr K, Menis J, et al. on behalf of the ESMO Guidelines Committee. Non-oncogene-addicted metastatic non-small-cell lung cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2023;34(4):358-376.
- Hendriks L E, Kerr K, Menis J, et al. on behalf of the ESMO Guidelines Committee. Oncogene-addicted metastatic non-small-cell lung cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2023;34(4):339-357.
- S. Popat, P . Bass, C. Faivre-Finn, et al, on behalf of the ESMO Guidelines Committee. Malignant pleural mesothelioma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. (2021)
- A-M.C. Dingemans, M. Früh, A. Ardizzoni et al. Small-cell lung cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Published in 2021 - Ann Oncol (2021)
