Nádory hlavy a krku zahrnují především karcinomy vycházející z epitelu horních dýchacích a polykacích cest – skvamózní karcinomy s různým stupněm diferenciace. Od skupiny skvamózních karcinomů hlavy a krku se oddělují karcinomy orofaryngu HPV pozitivní, jejichž incidence výrazně narůstá. HPV pozitivita je v této lokalitě spojena s lepší prognózou, ovšem dosud není pokládána za jednoznačně prediktivní faktor pro léčbu.
Před zahájením onkologické léčby musí být proveden staging onemocnění. U všech pacientů je zvažován multidisciplinární přístup. Indikační kritéria pro prezentaci pacienta na multidisciplinárním týmu jsou:
- všichni noví pacienti.
- rekurentní a metastatické nádory.
- pacienti po chirurgické léčbě s histologickým nálezem k indikaci adjuvantní terapie.
Léčba nádorů hlavy a krku je komplexní. Volba léčebné strategie závisí na lokalizaci a rozsahu primárního nádoru, jeho histologickém typu, přítomnosti regionálních nebo vzdálených metastáz, celkovém stavu pacienta, včetně nutrice, přítomnosti komorbidit, věku a preferencích pacienta. O způsobu léčby vždy rozhoduje multidisciplinární tým složený z otorinolaryngologa – chirurga, maxilofaciálního chirurga, radiačního a klinického onkologa, radiologa a dalších odborníků. Velký význam v kurativní i paliativní terapii má zajištění podpůrné léčby, které zahrnuje nutriční podporu, včetně případného včasného zavedení perkutánní gastrostomie, péči o chrup (sanace chrupu před radioterapií i poléčebná stomatologická péče), zajištění volných dýchacích cest (zvážení tracheostomie), rehabilitaci po léčbě atd.
Doporučení zahrnuje strategii léčby jednotlivých nádorů hlavy a krku a onkologickou léčbu s důrazem na léčbu systémovou. Podrobná doporučení pro jednotlivé indikace a provádění chirurgického výkonu a radioterapie jsou v kompetenci České společnosti otorinolaryngologie a chirurgie hlavy a krku a Společnosti radiační onkologie, biologie a fyziky.
1.1 Léčebná strategie nádorů hlavy a krku (vyjma nádorů nosohltanu a nádorů slinných žláz)
1.1.1 Lokalizované karcinomy (časné stadium)
V časných stadiích, T1-2N0, je hlavním léčebným přístupem jedna léčebná modalita, tj. chirurgická resekce nebo radioterapie. Volba modality závisí na řadě faktorů, jako je anatomická lokalizace, předpokládaný funkční a kosmetický výsledek, komorbidity a v neposlední řadě přání pacienta.
Radikální radioterapie u časných stadií znamená v mnoha případech rovnocennou alternativu radikálního chirurgického výkonu; přednost má v případech, kde lze od chirurgického výkonu očekávat větší mutilaci. Naopak chirurgický výkon je preferován u pacientů, kde je riziko mutilace minimální (kvalitu života může naopak zhoršit radioterapie) a určitě v případech, kde přináší lepší lokální kontrolu.
Elektivní uzlinová disekce (ND) je indikována vždy (riziko subklinických regionálních metastáz vyšší než 15–20 %) kromě nádorů nosu, vedlejších dutin nosních a glotické lokalizace karcinomu hrtanu.
Je-li po primárním operačním výkonu evidentní vyšší riziko recidivy (blízký či pozitivní resekční okraj#, angio/lymfangioinvaze, perineurální šíření, nedostatečné zhodnocení lymfatických uzlin), je nutné zvážit reoperaci či indikaci pooperační radioterapie.
1.1.2 Lokálně a regionálně pokročilé karcinomy
V dalším textu jsou lokálně a regionálně pokročilé nádory děleny na operabilní a inoperabilní. Obecně je však ústup od tohoto striktního rozdělení, zda nádor lze či nelze resekovat. Vždy je nutné přihlédnout k rozsahu resekce a možným následkům operačního výkonu. Definitivní rozhodnutí, zda je rozsah chirurgického výkonu pro pacienta akceptovatelný, záleží na samotném pacientovi.
1.1.2.1 Operabilní
Pro léčbu lokálně pokročilých, resekabilních onemocnění T3-4a nebo jakékoliv T, N1-3 je více možností:
- chirurgická resekce, včetně ND + adjuvantní radioterapie (bližší indikace adjuvantní radioterapie v jednotlivých lokalitách viz standardy SROBF ČLS JEP).
- chirurgická resekce, včetně ND + adjuvantní chemoradioterapie, indikace pro přidání konkomitantní chemoterapie: pozitivní resekční okraj, extranodální šíření, případně blízký resekční okraj, vícečetné uzlinové postižení, angioinvaze, lymfangioinvaze, perineurální šíření.
- indukční imunoterapie pembrolizumab 2 cykly, chirurgická resekce + adjuvantní radioterapie +/- chemoterapie + pembrolizumab 15 cyklů: tento režim prokázal benefit přidání pembrolizumabu ve studii KN 689. O úhradě pembrolizumabu ze zdravotního pojištění v této indikaci nebylo k 1. 3. 2026 rozhodnuto.
- primární konkomitantní chemoradioterapie: chirurgický výkon je ponechán v případě rezidua nebo recidivy jako záchranná léčba (týká se zejména larynx záchovných postupů),
- u karcinomu hypofaryngu je možný larynx záchovný postup: indukční chemoterapie 2–3 cykly se zhodnocením odpovědi po druhém cyklu, při dobré odpovědi nádoru radioterapie, při stabilním onemocnění či progresi nádoru indikace chirurgického výkonu,
- u pacientů v horším biologickém stavu je volen postup individuálně.
1.1.2.2 Inoperabilní
Standard
Chemoradioterapie – jako konkomitantní režim chemoterapie je preferována cisplatina v monoterapii. Indikaci konkomitantní chemoterapie je nutné zvážit s ohledem na celkový biologický stav pacienta (PS 0–1) a vedlejší onemocnění. Metaanalýzy neprokázaly přínos přidání chemoterapie u pacientů ve věku nad 70 let.
Alternativy
– radioterapie s použitím různých frakcionačních schémat (hyperfrakcionace, concomitant boost apod.),
– radioterapie s konkomitantním podáním cetuximabu.
Pozn. v subanalýze přínos konkomitantního cetuximabu nebyl prokázán u pacientů s KI < 80 % ve věku 65 let a starších,
přínos nebyl signifikantní ani při použití normofrakcionačního režimu RT (preferován alternativní frakcionační
režim).
- v sekundární analýze studie BOND omezené na pacienty s nádory hypofaryngu a laryngu nebyl prokázán přínos cetuximabu v těchto parametrech: v larynx záchovných operacích, celkové délce přežití do provedení laryngektomie a mOS,
- pro HPV+ karcinomy orofaryngu randomizované studie (RTOG 1016, DeEscalate HPV, TROG 12.01) prokázaly nižší účinnost radioterapie s cetuximabem ve srovnání se standardní chemoradioterapií,
- indukční chemoterapie + s následnou radioterapií samotnou nebo v konkomitanci s chemoterapií či cetuximabem. Tento postup nutno zvažovat individuálně – např. při primárně rozsáhlém uzlinovém postižení N3 s nutností okamžité léčby.
– samostatná radioterapie v normofrakcionačním režimu,
– u pacientů v horším biologickém stavu je volen postup individuálně.

1.1.3 Recidivující a metastatické karcinomy
Před zahájením terapie nutno zvážit možný přínos a účelnost jednotlivých léčebných modalit a jejich toxicitu s ohledem na celkový biologický stav, věk a morbiditu pacienta.
Lokální a/nebo regionální recidiva:
– operační řešení (kurativní možnost),
– paliativní operační řešení (např. zavedení tracheostomie),
– radioterapie nebo chemoradioterapie (kurativní možnost, pokud nebyla indikována v rámci primární léčby),
– reiradiace (kurativní nebo paliativní) má smysl, pokud je relativně malý rozsah recidivy, recidiva se objeví minimálně 12 měsíců po primární radioterapii, není závažná pozdní toxicita po primární radioterapii, je spojeno s výraznými riziky pozdní toxicity,
– paliativní chemoterapie,
– paliativní cílená léčba/chemoterapie,
– paliativní imunoterapie nebo imunoterapie/chemoterapie,
– symptomatická léčba.
Metastatické postižení
U oligometastatického onemocnění jsou zvažovány lokální metody léčby s kurativním záměrem: operace, radioterapie (např. stereotaktická radioterapie). Pokud není možná kurativní lokální léčba, pak je zvažována systémová protinádorová léčba (kombinace chemoterapie a imunoterapie, imunoterapie, cílená léčba/chemoterapie, paliativní chemoterapie) a/ nebo paliativní operační zákroky či radioterapie, případně symptomatická léčba.
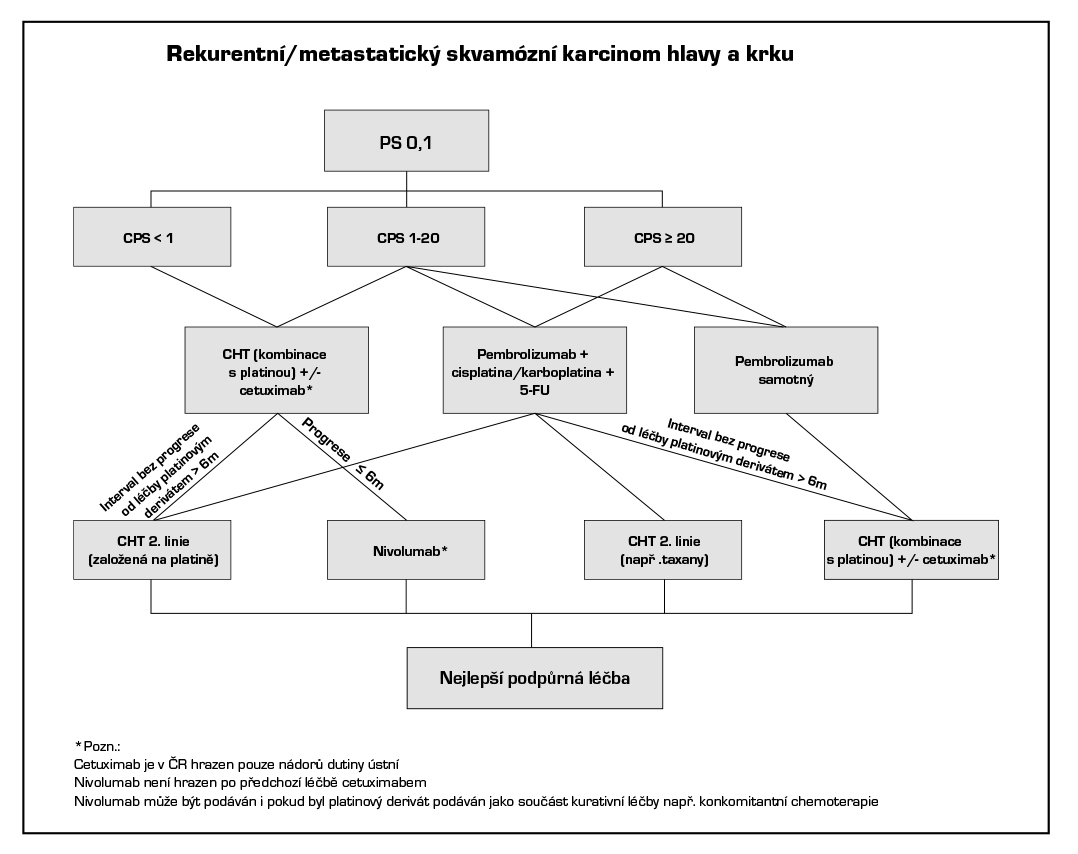
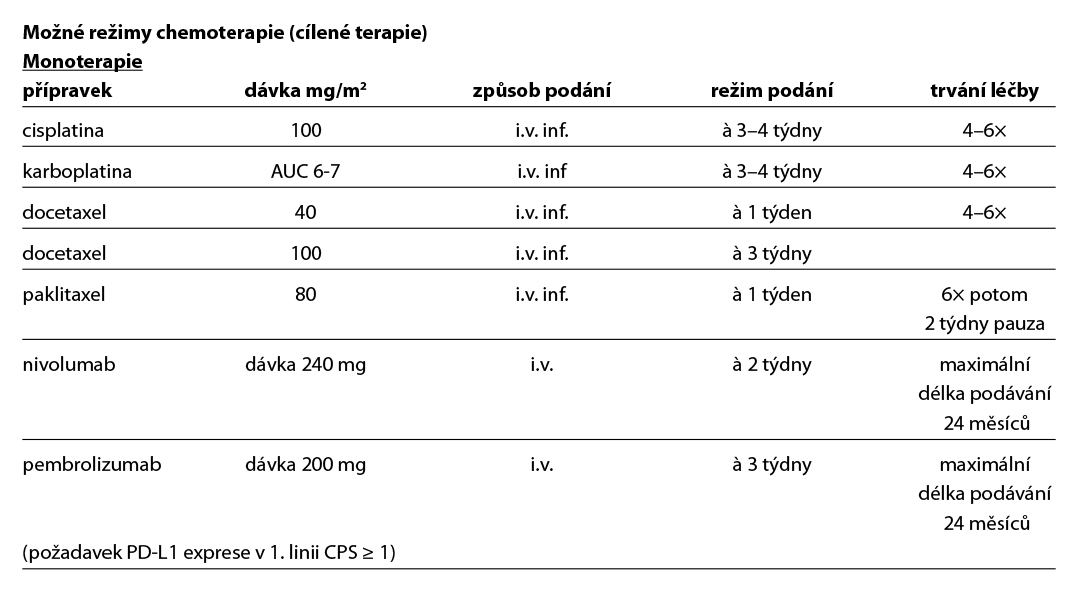
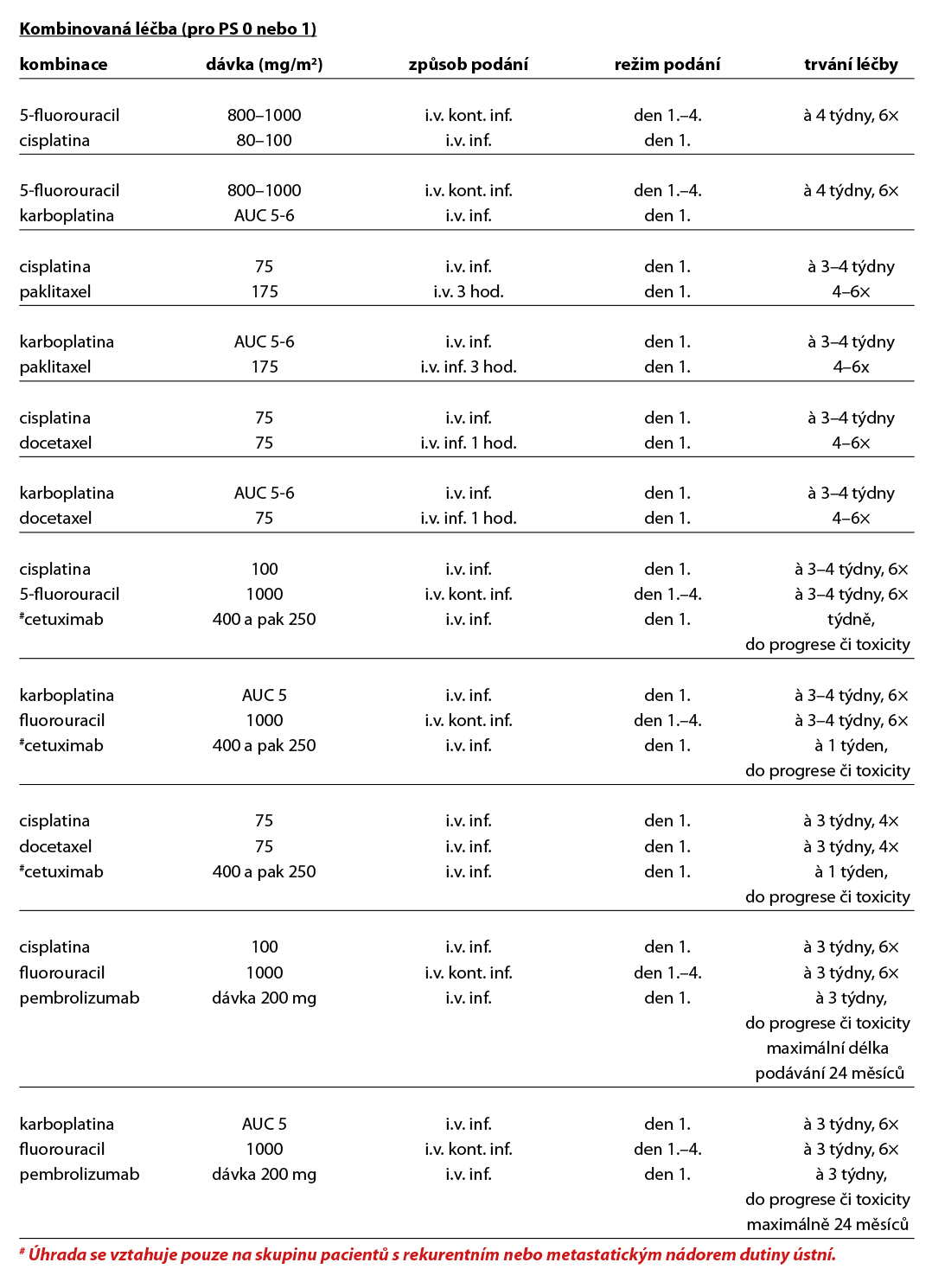
Systémová léčba rekurentního a metastatického onemocnění
Studie Keynote 048 prokázala efekt imunoterapie v léčbě metastatického onemocnění a vedla k úhradě pembrolizumabu v monoterapii nebo v kombinaci s chemoterapií založenou na platině a fluoruracilu (5-FU) v první linii léčby metastazujícího nebo neresekovatelného recidivujícího skvamózního karcinomu hlavy a krku u dospělých pacientů s ECOG je 0–1, a to v případě exprese PD-L1 s CPS ≥1. Maximální délka léčby je 24 měsíců. V případě CPS <1 či kontraindikace imunoterapie je léčebnou alternativou režim studie EXTREME (kombinace cisplatina (nebo karboplatina) – 5-fluorouracil – cetuximab), jehož použití vede k prodloužení celkového přežití proti samostatné chemoterapii, (medián OS 10,1 vs 7,4 měsíce). Alternativou je režim TPEx (cisplatina + docetaxel + cetuximab), který má srovnatelnou účinnost s režimem EXTREME při lepší komplianci a nižší toxicitě. Použití režimu s cetuximabem je v ČR hrazeno pouze u nádorů dutiny ústní. Pokud došlo k progresi nádoru během nebo do 6 měsíců po chemoterapii s platinovým derivátem pro metastatický/rekurentní skvamózní karcinom nebo po kombinované léčbě s platinovým derivátem (např. chemoradioterapii), je možné indikovat nivolumab v dávce 240 mg à 2 týdny. Randomizovaná studie fáze III CheckMate 141 prokázala účinnost nivolumabu ve druhé linii. V ČR není nivolumab hrazen po předchozí léčbě režimem s cetuximabem.
Při volbě režimu paliativní chemoterapie (monoterapie, kombinovaný režim) je nutné přihlédnout k celkovému stavu pacienta, vedlejším onemocněním, terapeutickému cíli i preferenci pacienta. Přínos chemoterapie pouze ve smyslu prodloužení života je obecně velmi sporný. Rozdíly mezi jednotlivými režimy jsou v pravděpodobnosti odpovědi, ale i toxicitě.
# Za pozitivní resekční okraj je považována přítomnost nádorových buněk v okraji řezu, za blízký okraj přítomnost nádorových buněk ve vzdálenosti < 5 mm, v případě endoskopických výkonů při časném karcinomu hlasivek < 1 mm.
(Konsensuální doporučení České kooperativní skupiny pro nádory hlavy a krku: www.hnc-group.cz/doporuceni.cz).
1.2 Léčebná strategie nádorů nosohltanu
Nádory nosohltanu jsou samostatnou nosologickou jednotkou vzhledem k odlišnému biologickému chování. Jsou charakteristické vysokou chemo- a radiosenzitivitou. Na druhou stranu je u nich vyšší riziko vzdálené diseminace, proto je kladen větší důraz na systémovou léčbu než u ostatních nádorů hlavy a krku.
1.2.1 Časná stádia
- pro stádium T1 N0 M0 a low risk T2 N0 M0 je dostatečná léčba samostatnou radioterapií.
Pozn. low risk T2 N0 M0 = non-bulky tumor, nízké hodnoty EBV-DNA před léčbou.
- pro high risk stádium (bulky tumor, vysoké hodnoty EBV-DNA před léčbou) T2 N0 M0 konkomitatní chemoradioterapie.
1.2.2 Lokálně pokročilé nádory
- neoadjuvantní (indukční) chemoterapie T1-2 N1-3 a T3-T4, jakékoliv N, s následnou konkomitantní chemoradioterapií (preferovaný postup),
- konkomitantní chemoradioterapie následovaná adjuvantní chemoterapií (pokud nebyla primárně indikována neoadjuvantní chemoterapie),
- konkomitantní chemoradioterapie bez adjuvantní chemoterapie, případně samostatná radioterapie – lze akceptovat u pacientů s horší tolerancí chemoterapie.
1.2.3 Lokálně recidivující a metastatické nádory
Postup se určuje individuálně podle rozsahu a lokality postižení, celkového stavu pacienta a předchozí léčby:
- paliativní chemoterapie,
- chemoradioterapie s paliativním záměrem, pokud již nebyla použita,
- reiradiace,
- záchranná chirurgie.
Preferovaným režimem chemoterapie první linie u metastatického nádoru nosohltanu je kombinace cisplatina-gemcitabin. Randomizovaná studie fáze III JUPITER-02 prokázala přínos anti-PD-1 protilátky toripalimab ke kombinaci cisplatina-gemcitabin proti stejné chemoterapii s placebem (mPFS 21,4 vs. 8,2 měsíce; HR 0.52 [95% CI, 0.37-0.73]; mOS při mediánu sledování 36,0 měsíce nebyl dosažen proti 33,7 měsíce v rameni s placebem; HR 0.63 [95% CI, 0.45-0.89]; P = .008). Studie byla provedena na asijské populaci a v roce 2024 přípravek Loqtorzi získal EMA registraci. O úhradě tohoto přípravku ze zdravotního pojištění v této indikaci nebylo k 1. 3. 2026 rozhodnuto.
Preferovaným režimem první linie u metastatického nádoru nosohltanu je kombinace cisplatina-gemcitabine. V druhé linii neexistuje standardní léčebný režim. K dispozici jsou následující cytostatika v monoterapii či vybraných kombinacích: paklitaxel, docetaxel, 5-flourouracil, capecitabine, irinotekan, vinorelbin, ifosfamid, doxorubicin, oxaliplatina a *cetuximab. Kombinované režimy jsou více efektivní, ale toxičtější.
Imunoterapie byla testována ve studiích fáze II, léčebnou možností je *pembrolizumab (pro TMB-H ≥10mut/Mb, a PD-L1 pozitivní nádory), a dále *nivolumab.

1.3 Léčebná strategie nádorů slinných žláz
Jako základní léčebný postup je u nádorů slinných žláz obvykle preferován radikální chirurgický výkon. V závislosti na rozsahu tumoru, histologickém typu, radikalitě výkonu a přítomnosti metastáz v regionálních lymfatických uzlinách je indikována pooperační radioterapie.
1.3.1 Časná stádia
- operace: stádium T1-2 N0 M0,
- příušní žláza: u tumorů G1 při lokalizaci v superficiálním laloku a při absenci parézy n. VII lze zvážit superficiální parotidektomii, u tumorů G2 a G3 je preferovaným výkonem totální parotidektomie,
- elektivní krční disekce vždy i u cNO (riziko okultních metastáz v regionálních lymfatických uzlinách LU 15–20 %),
- u nádorů submandibulární žlázy kompletní exstirpace a u nádorů menších slinných žláz jiných lokalit indikována resekce s okrajem minimálně 1 cm,
- elektivní krční disekce, obzvláště u tumorů vyššího gradu (G2-4) a u některých histologických podtypů (salivární duktální karcinom, nediferencovaný karcinom, adenokarcinom NOS, high-grade mukoepidermoidní karcinom (MEC), adenoidně cystický karcinom (AdCC) a skvamózní karcinom (SCC)) – riziko okultního postižení i při nehmatných uzlinách nad 50 %,
- rozšířená krční disekce: při nálezu pozitivních lymfatických uzlin,
- je-li po primárním operačním výkonu vyšší riziko recidivy (blízký či pozitivní resekční okraj, angio/lymfangioinvaze, perineurální šíření, nedostatečný počet lymfatických uzlin), je nutné zvážit reoperaci či indikaci pooperační radioterapie.
1.3.2 Lokálně pokročilé nádory
U lokálně pokročilých stadií (T3, T4 a T1-4 N+) je pro postup určujícím faktorem operabilita:
- resekce včetně krční disekce a následně radioterapie,
- kurativní radioterapie: inoperabilní nemetastatický nádor (rozsahem nebo pro komorbidity).
1.3.3. Recidivující či metastatické onemocnění
- při operabilní solitární metastáze či oligometastatickém onemocnění (např. játra, plíce, mozek) je preferována resekce metastázy/metastáz, případně stereotaktická radioterapie,
- při inoperabilním postižení – paliativní postupy, vycházející z rozsahu a lokality postižení, histologické charakteristiky nádoru i celkového stavu pacienta,
- u pacientů s pomalu progredujícím inoperabilním metastatickým postižením (např. u adenoidně cystického karcinomu) je zvažováno dlouhodobé sledování s indikací paliativní léčby při symptomech či hrozících symptomech, metastázy mohou být asymptomatické i několik let,
- u pacientů s rychle progredujícím nebo symptomatickým inoperabilním metastatickým postižením je indikována včasná systémová léčba, jejíž výběr se odvíjí od průkazu prediktorů, histologického typu a dalších parametrů (grade, proliferační aktivita, …),
- v případě kostních nebo jaterních metastáz je doporučeno započít systémovou léčbu co nejdříve,
- pro zvažování paliativní systémové léčby je doporučeno vyšetření molekulárně biologických prediktorů, které zahrnuje vyšetření NGS DNA a RNA panelů, imunohistochemické vyšetření hormonálních receptorů a HER2,
- při indikaci systémové terapie nejsou jednoznačně doporučené režimy vzhledem k nedostatku studií a heterogenitě jednotlivých nádorů, z chemoterapie jsou obvykle zvažovány režimy na bázi cisplatiny a/nebo antracyklinů,
- u adenoidně cystického karcinomů lze zvážit i cytostatickou léčbu cisplatinou nebo i kombinovaný režim CAP (RR 13– 25 %), zvážit lze i inhibitory angiogeneze jako *sorafenib, *lenvatinib nebo *axitinib,
- u adenokarcinomů NOS a salivárního duktálního karcinomu prokázal efekt paklitaxel a vinorelbin v kombinaci s karboplatinou,
- u HER2 pozitivních metastatických tumorů je možno indikovat *trastuzumab. Dle literatury je nejvyšší HER2 pozitivita zachycena u salivárního duktálního karcinomu (až 55 %) s podobnou senzitivitou k trastuzumabu jako u karcinomu prsu. Je možno zvážit kombinaci trastuzumabu a taxanu (ORR 70,2 % medián OS 39,7 měsíce), dobré zkušenosti jsou i s *TDM1 a *pertuzumabem.
- v případě pozitivity androgenního receptoru jsou publikována data o účinnosti *bicalutamidu nebo totální androgenní blokády (kombinace *bicalutamidu a *LHRH),
- u pacientů s karcinomy slinných žláz, zejména u sekrečních karcinomů, je vhodné testování NTRK fúze a zvážení podání TRK inhibitoru (*larotrectinib, *enctrectinib).
- Pro nádory s vysokou mutační náloží (TMB-H) vhodná terapie *pembrolizumabem.
*Žádná cílená biologická léčba ani imunoterapie nemá primárně stanovenu úhradu v této indikaci.
1.4 Vybrané informace k biologické léčbě
1.4.1 Cetuximab v léčbě karcinomu hlavy a krku
Cetuximab je indikován k léčbě pacientů se skvamózním karcinomem hlavy a krku
- v kombinaci s radioterapií k léčbě lokálně pokročilého onemocnění,
- v kombinaci s chemoterapií na bázi platiny k léčbě relabujícího a/nebo metastazujícího onemocnění (pro skupinu pacientů s relabujícím anebo metastatickým nádorem ústní dutiny, jejichž Karnofsky performance skóre je ≥ 90). Léčba cetuximabem je hrazena do progrese onemocnění.
Přípravek KEYTRUDA
- je v monoterapii nebo v kombinaci s chemoterapií platinou a fluorouracilem (5-FU) indikován v první linii k léčbě metastazujícího nebo neresekovatelného recidivujícího skvamózního karcinomu hlavy a krku (HNSCC) u dospělých, jejichž nádory exprimují PD-L1 s CPS ≥ 1,
- *je v monoterapii indikován k léčbě recidivujícího nebo metastazujícího HNSCC u dospělých, jejichž nádory exprimují PD-L1 s TPS ≥ 50 %, a kteří podstupují nebo podstoupili chemoterapii obsahující platinu.
Přípravek OPDIVO
- monoterapii skvamózního karcinomu hlavy a krku (karcinomu dutiny ústní, faryngu a laryngu) u dospělých, kteří progredovali v průběhu nebo do šesti měsíců po ukončení léčby založené na platinových derivátech a kteří nebyli v minulosti léčeni cetuximabem.
*O úhradě přípravku ze zdravotního pojištění v této indikaci nebylo k 1. 3. 2026 rozhodnuto.
1.5 Molekulárně prediktivní vyšetření u nádorů hlavy a krku
1/ časný karcinom – p16, EBV, PD-L1 (CPS)
2/ metastatický karcinom – PD-L1 (CPS), MMR
1.6 Nádory hlavy a krku – follow up
Vzhledem k tomu, že nádory hlavy a krku zahrnují soubor onemocnění nehomogenní z hlediska histologie, etiologie a biologického chování, lokality postižení, rozsahu postižení, použitých léčebných modalit atd., je následující doporučení definováno obecně a u každého pacienta může být postup modifikován výše uvedenými parametry.
Klinické kontroly:
Frekvence klinických kontrol kromě výše uvedených faktorů ovlivňuje také možnost provedení záchranné kurativní léčby, např. v případě těsných/pozitivních resekčních okrajů s možností reoperace jsou doporučovány klinické kontroly častěji. Obecné doporučení pro frekvenci kontrol je v tabulce. Klinické kontroly by měly být prováděny ve spolupráci s otorhinolaryngologem (event. stomatochirurgem), aby byly vyšetřeny horní dýchací a polykací cesty.
Laboratorní vyšetření:
U nádorů hlavy a krku není v současné době přínosem vyšetřování nádorových markerů. U pacientů, kteří prodělali ozáření v oblasti krku a u kterých je riziko rozvoje postradiační hypothyreozy, jsou doporučovány pravidelné (1–2× ročně) odběry thyreostimulačního hormonu (TSH).

Zobrazovací metody:
U asymptomatických pacientů se zobrazovací vyšetření obligatorně neprovádí. K indikaci zobrazovacích vyšetření se kloníme v případě oblasti nepřístupné klinickému vyšetření (např. primární nádor v oblasti nepřístupných vedlejších dutin nosních).
Pro skvamózní karcinomy N+ po radikální chemoradioterapii je vhodné provedení PET/CT 3 měsíce po léčbě kvůli zvážení případné krční disekce. V ostatních případech jsou diagnostické zobrazovací metody voleny individuálně, obvykle v případě symptomů či jiného podezření na relaps nemoci.
Další vyšetření:
Vzhledem k riziku komplikací po náročné komplexní léčbě musí být dlouhodobě u řady pacientů zajištěna také péče nutriční, stomatologická apod.
1.7 Molekulárně prediktivní vyšetření u nádorů slinných žláz
metastatický karcinom – panel pr okomplexní genomové profilovní (DNA + RNA), HER2 (IHC +/- ISH), AR, MMR/MSI, PD-L1.
1.8 Nádory slinných žláz – follow up
Neexistují jednoznačná data pro závazné doporučení sledování pacientů. Sledování by mělo být zaměřeno na časný záchyt rekurence a disseminace, kromě klinického vyšetření doporučujeme zvážit i MRI krku (nebo jiné lokality prima) a CT plic, zejména v prvních 2 letech od kurativní léčby.
U pacientů s reziduálním, rekurentním nebo metastatickým onemocněním individuálně upravit frekvenci vyšetření dle aktivity růstu nádoru, podané léčby a hodnocení jejího efektu.
Literatura:
- Bossi P, Chan AT, Even C, Machiels JP; ESMO Guidelines Committee. ESMO-EURACAN Clinical Practice Guideline update for nasopharyngeal carcinoma:
adjuvant therapy and first-line treatment for recurrent/metastatic disease. Ann Oncol. 2023;34: 247-250. - Machiels J-P, René Leemans C, Golusinski W, et al. Squamous cell carcinoma of the oral cavity, larynx, oropharynx and hypopharynx: EHNS-ESMO-ESTRO
Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2020;11:1462-1474. - Národní radiologické standardy – radiační onkologie (revize 2016).
- NCCN Clinical Practice Guidelines in Oncology. Head and Neck Cancers, Version 1.2026.
- Resteghini C, Baujat B, Bossi P,et al.; ESMO Guidelines Committee. Sinonasal malignancy: ESMO-EURACAN Clinical Practice Guideline for diagnosis, treatment
and follow-up. ESMO Open. 2025;10:104121. - van Herpen C, Vander Poorten V, Skalova A, et al.; ESMO Guidelines Committee. Salivary gland cancer: ESMO-European Reference Network on Rare Adult
Solid Cancers (EURACAN) Clinical Practice Guideline for diagnosis, treatment and follow-up. ESMO Open 2022; 7:100602. - Vošmik M, Klozar J, Laco J, et al. Konsensuální doporučení České kooperativní skupiny pro nádory hlavy a krku (2019): Definice resekčních okrajů, reportování
krčních disekcí a vyšetřování HPV/p16, Cesk Patol. 2021; 57:53-56,
