12. ZHOUBNÝ NOVOTVAR PRSU (C50)
12.1. Obecná doporučení před zahájením systémové terapie
Neoadjuvantní a adjuvantní terapie
Před zahájením jakékoliv léčby včetně operačního výkonu je nutné u pacientek s karcinomem prsu I. – III. klinického stádia konzultovat léčebný postup v rámci multidisciplinárního týmu (MDT), jehož součástí je obligatorně chirurg, klinický onkolog a radiodiagnostik, fakultativně pak patolog a radioterapeut. Pokud je indikována neoadjuvantní terapie, tak je další postup po jejím ukončení opět indikován cestou MDT.
Rozhodnutí o konkrétním léčebném postupu je založeno na podtypu karcinomu prsu, rozsahu onemocnění, předpokládané citlivosti k léčbě, benefitu terapie, možných rizicích a nežádoucích účincích spojených s léčbou, celkovém stavu pacienta, komorbiditách a preferencích pacienta. Stanovení přesného rozsahu onemocnění v prsu a axile a vyloučení/ potvrzení vzdáleného postižení je klíčové k volbě optimálního léčebného postupu. MG vyšetření je základní metodou ke zhodnocení rozsahu onemocnění v prsu, UZ vyšetření je metodou doplňkovou a je důležité ke zhodnocení stavu spádových lymfatických uzlin. MRI vyšetření prsů je indikováno individuálně, nejčastěji v případě nejasného nálezu na MG/ UZ vyšetření nebo upřesnění rozsahu postižení v prsu; v případě lobulárního karcinomu a optimálně u pacientek před zahájením neoadjuvantní terapie (NAT), zvláště u kterých je plánováno provedení prs záchovného výkonu. V případě NAT terapie a plánovaném prs záchovném výkonu je doporučeno označení ložiska v prsu, v případě podezření na uzlinové postižení je doporučeno provedení histologické verifikace s označením bioptované uzliny. V rámci stagingových vyšetření je obligatorně prováděno u klinického st. I RTG vyšetření hrudníku a UZ vyšetření jater, scintigrafie skeletu obligatorně prováděna není. U pacientek od klinického stádia IIB, zvláště u pacientek s agresivními podtypy onemocnění (HER2+ a TNBC) je vhodné zvážit v rámci stagingu onemocnění provedení CT trupu +/- scintigrafie skeletu nebo provedení celotělového FDG PET/CT. U pacientek s lokálně pokročilými hormonálně dependentními nádory, zvláště u pacientek s lobulárními a low grade karcinomy, lze v rámci stagingu zvážit provedení FES PET/CT vyšetření, pokud je k dispozici. Provedení vyšetření je indikováno cestou MDT.
Obecná léčebná doporučení jsou uvedena v Tab. 1.
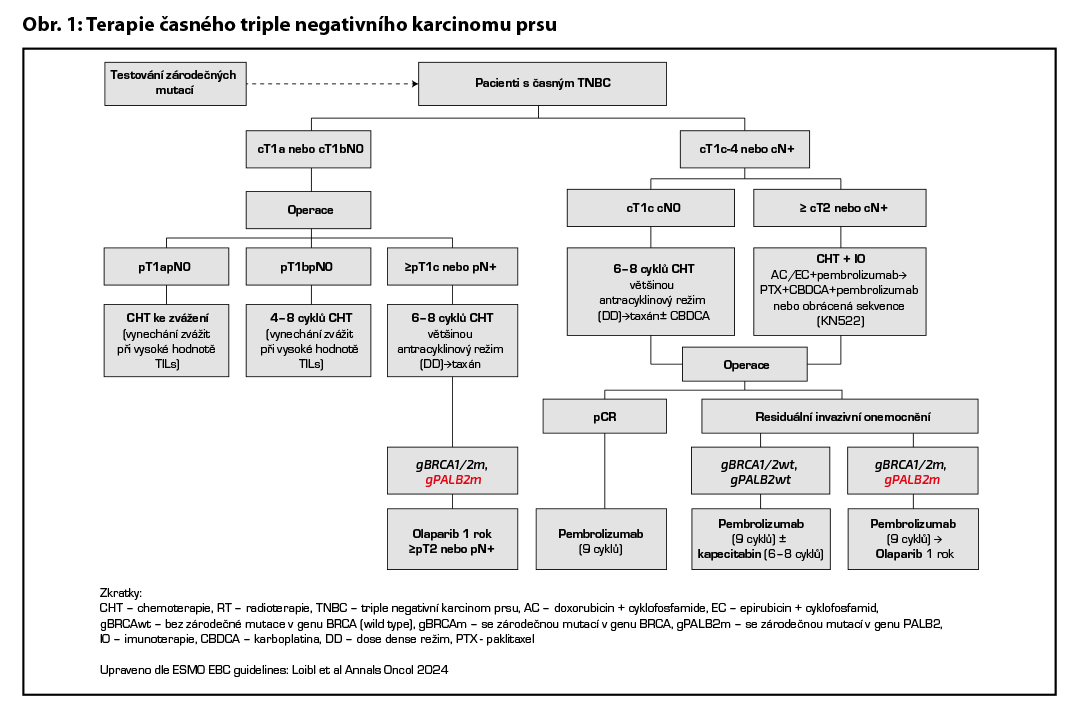
Neoadjuvantní terapie (NAT) je preferována u pacientek s triple negativním karcinomem prsu (cT1c a vyšší) a u pacientek s HER2 pozitivním karcinomem prsu (cT2 a vyšší, cT1c individuálně). U pacientek s luminálním HER2 negativním karcinomem je NAT volena individuálně (rozsah postižení v prsu a axile, operabilita onemocnění, předpokládaný benefit – léčebnou odpověď lze očekávat spíše u pacientek s nádory vyššího gradu, nižší expresí steroidních receptorů a vysokou proliferací dle indexu Ki-67). Luminální HER2 negativní karcinom je podtyp s nejmenší léčebnou odpovědí na NAT, četnost patologických kompletních remisí (pCR) se pohybuje do 15 %. Nutné pamatovat na riziko nadléčení pacientky v rámci NAT. Ke stanovení benefitu NAT a prognózy u pacientek s luminálními HER negativními karcinomy je možné využít multigenových testů (podrobně kapitola 12.2 Neoadjuvantní terapie).
Adjuvantní terapie by měla být zahájena do 3–6 týdnů od provedení operačního výkonu, u triple negativního karcinomu prsu (TNBC) do 4 týdnů. Hormonální léčba (HT) by měla být použita u všech pacientek s expresí hormonálních receptorů (HR), podrobně viz doporučení dále v textu.
Indikace podání adjuvantní chemoterapie (CHT) u luminálních B HER2 negativních karcinomů je individuální, vychází z rozsahu onemocnění, jeho biologického chování, rizika relapsu a menopauzálním stavu pacientky. V indikovaných případech lze použít multigenové testy k upřesnění prognózy onemocnění a predikci benefitu systémové terapie. Adjuvantní HT je součástí léčby všech pacientek s luminálním HER2 negativním karcinomem, pokud není jednoznačný důvod k jejímu vynechání. U pacientek ER-/PR+ není adjuvantní HT indikována. Tento stav je vhodné ověřit druhým čtením histologického vyšetření. U vysoce rizikových pacientek je podávána kombinace HT a abemaciklibu (MonarchE) nebo ribociklibu (NATALEE), u vysoce rizikových pacientek s germinální BRCA1/2 a PALB2 mutací je indikována léčba olaparibem (OlympiA). Premenopauzální pacientky, u kterých jsou podávána LHRH analoga, jsou léčeny jako postmenopauzální.
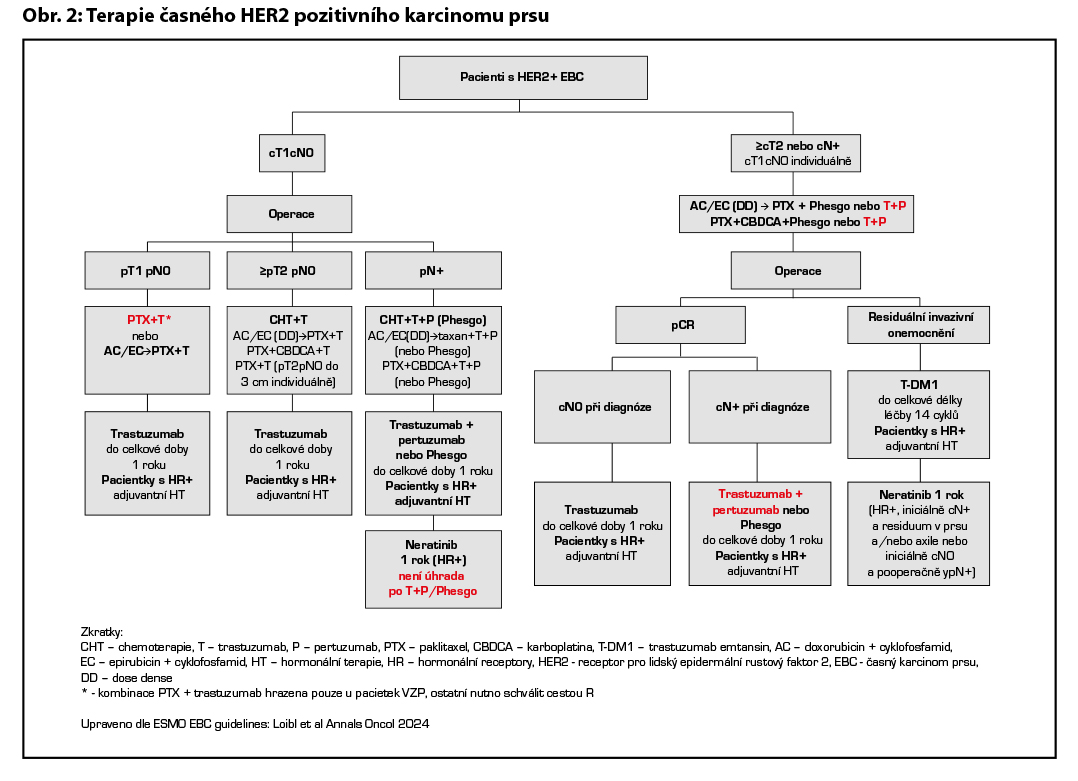
Pacientky s HER2 pozitivním karcinomem po primárním operačním výkonu (I. klinické stádium) by měly být adjuvantně léčeny kombinací CHT a anti-HER2 terapie. Pacientky vyšších klinických stádií jsou ve většině případů léčeny NAT. Pacientky s TNBC by měly být ve většině případů po primárním operačním výkonu (pT1a, pT1b) léčeny CHT. U pacientek s větším rozsahem onemocnění (≥ cT1c a vyšší, N+) je preferována NAT; CHT (cT1c) nebo kombinace CHT + imunoterapie (cT2 a vyšší). Pacientky s expresí ER < 10% (tzv. ER-low karcinomy) tvoří značně heterogenní populaci, avšak i u těchto pacientek je adjuvantní HT doporučena. U pacientek s expresí ER < 5 % klinického stádia II. je vhodné podání NAT (CHT + pembrolizumab). Konkrétní léčebný postup vychází vždy z doporučení MDT. U vysoce rizikových pacientek s TNBC, které jsou nosičkami germinální mutace BRCA1/2 nebo PALB2 je indikována léčba olaparibem (úhrada je stanovena pouze v případě BRCA1/2 mutace).
Na přítomnost germinálních mutací, jakožto prediktivního markeru, by měly být testovány všechny pacientky s HER2 negativním karcinomem prsu splňující kritéria pro adjuvantní léčbu olaparibem.
Doporučení léčebných postupů v rámci (neo)adjuvantní terapie u jednotlivých podtypů je shrnuto v Tab. 1 a na Obr. 1 a Obr. 2.
Gravidní pacientky
Léčba gravidních pacientek a pacientek v laktaci je značně specifická, náleží do onkologických center se zkušeností s touto problematikou. Léčebný postup musí být u těchto pacientek indikován v rámci MDT. Na základě výsledků klinické studie POSITIVE lze u pacientek s časným HR pozitivním karcinomem prsu akceptovat přerušení adjuvantní HT (nejdříve po 18 měsících užívání HT) s cílem těhotenství a po porodu pokračovat v plánované adjuvantní HT. Gravidita po léčbě pro karcinom prsu nezhoršuje prognózu pacientek ve smyslu vyššího rizika relapsu onemocnění nebo zhoršení celkového přežití.
Prezervace ovariální funkce
Onkologická léčba může mít negativní dopad na fertilitu, s pacientkou by před léčbou měla být tato problematika diskutována. Pacientkám zvažujícím těhotenství po dokončení onkologické léčby lze nabídnout prezervaci ovariální funkce pomocí kryoprezervace embryí nebo oocytů ve spolupráci s IVF centrem, popř. je další možností podání LH-RH analog v průběhu systémové CHT nebo imunoterapie (podle studie POEMS – goserelin 3,6 mg s. c. týden před zahájením CHT, po celou dobu podávání CHT a 2 týdny po ukončení CHT).
Geriatrické pacientky
Léčba této skupiny pacientek se řídí stejnými pravidly jako terapie pacientek mladších. Vhodné je zvažovat i v adjuvanci úvodní redukci dávek CHT s ohledem na sníženou hepatální a renální clearance a dle tolerance v následujících cyklech dávky CHT při dobré toleranci navýšit. Preferovány jsou v adjuvanci kombinační režimy. Při indikaci rozsahu adjuvantní terapie je vhodné zvážit očekávanou délku života s ohledem na interkurence pacientů. Lze využít např. Charlson comorbidity index (CCI). https://www.mdcalc.com/calc/3917/charlson-comorbidity-index-cci
Muži
Muži, u kterých byl diagnostikován karcinom prsu, by měli být léčeni dle léčebných doporučení pro karcinom prsu u žen.

12.2 Neoadjuvantní a adjuvantní systémová terapie
12.2.1 Neoadjuvantní systémová terapie
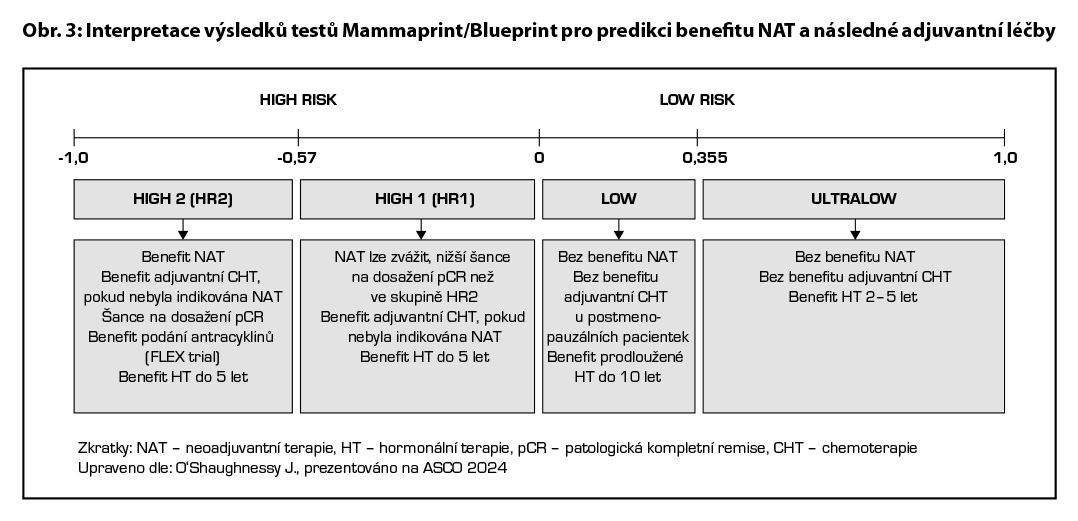
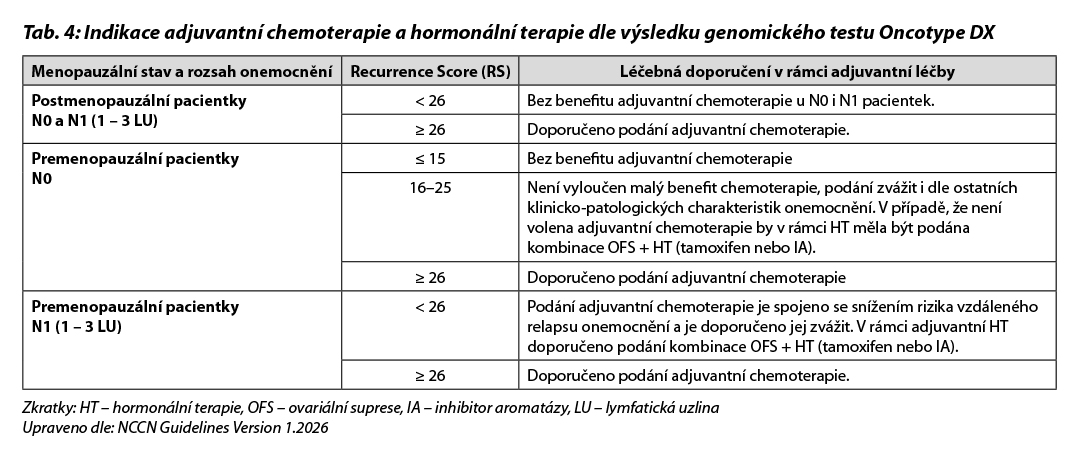
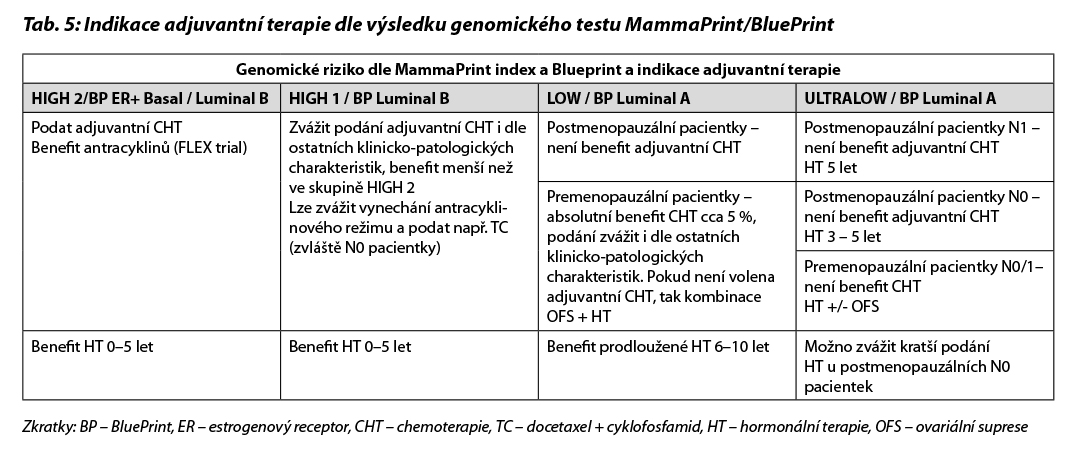
Neoadjuvantní terapie je vhodná u pacientek, u kterých lze očekávat odpověď na CHT/cílenou terapii/imunoterapii (nádory s nízkými nebo negativními HR, s vysokým gradem, karcinomy s vysokým Ki- 67, HER2+, TNBC). Dále je neoadjuvantní terapie volena u pacientek s lokálně pokročilým inoperabilním onemocněním, u pacientek s inflamatorním karcinomem prsu a u pacientek, u kterých lze v případě regrese postižení provést prs záchovný výkon a/nebo menší operační výkon v axile (cílená axilární disekce). Ke zhodnocení benefitu neoadjuvantní chemoterapie lze u pacientek s HR+/HER2karcinomy využít multigenových testů. Indikace vyšetření má stejná kritéria jako v rámci adjuvantní terapie a provedení vyšetřen je nutné schválit v rámci MDT v KOC. Pokud je vyšetření provedeno před operačním výkonem, není možné již jeho opakované provedení po provedení operace. V případě použití testu Oncotype DX lze největší benefit NAT očekávat u pacientek s vysokým RS ( ≥ 26, zejména > 30). U premenopauzálních pacientek může být benefit NAT i v případě nižšího RS (16 – 25), obdobně jako je tomu v případě benefitu adjuvantní terapie. V případě použití multigenového testu MammaPrint/BluePrint mají největší benefit z NAT pacientky zejména ve skupině high risk 2 (vyšší pravděpodobnost dosažení pCR) a následně ve skupině high risk 1 (pravděpodobnost dosažení pCR nižší než ve skupině high risk 2). U pacientek s nízkým a ultra nízkým rizikem není benefit NAT. Možné interpretace výsledků vyšetření MammaPrint/Blueprint pro využití v rámci NAT jsou uvedeny na Obr. 3
Podání NAT umožní:
- provedení parciálního operačního výkonu,
- dosažení operability původně inoperabilního nálezu,
- zisk důležitých prognostických informací dle efektivity neoadjuvantní léčby,
- poskytnutí času pro genetické testování,
- možné naplánování rekonstrukční operace,
- redukce rozsahu operačního výkonu v axile (při původní N+ při regresi nálezu provedení pouze cílené axilární disekce místo disekce axily),
- v případě TNBC a HER2 pozitivního karcinomu je dosažení patologické kompletní remise (pCR) po neoadjuvantní terapii signifikantně spojeno s lepší prognózou onemocnění (nižší četnost relapsů onemocnění a lepší celkové přežívání pacientek).
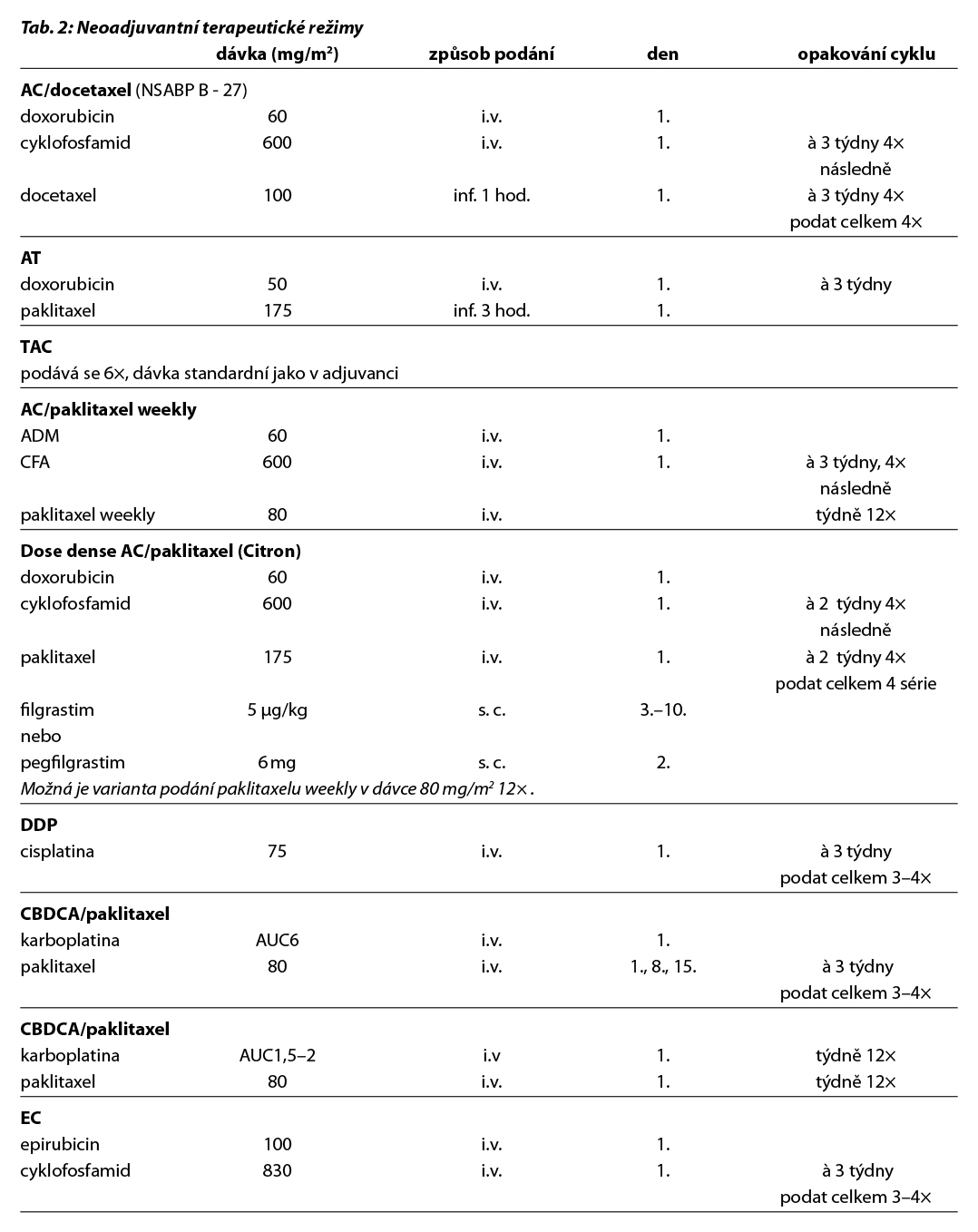
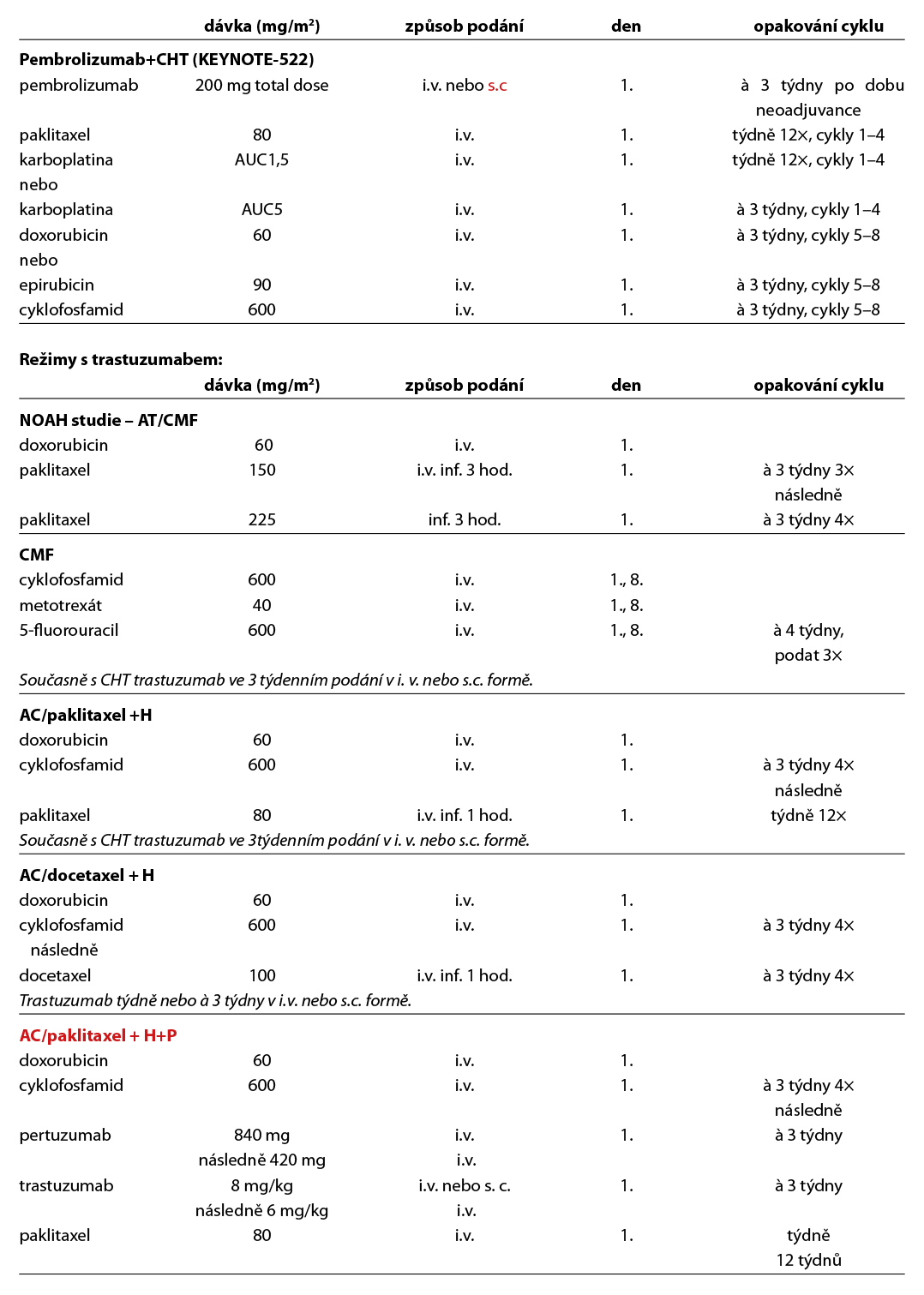
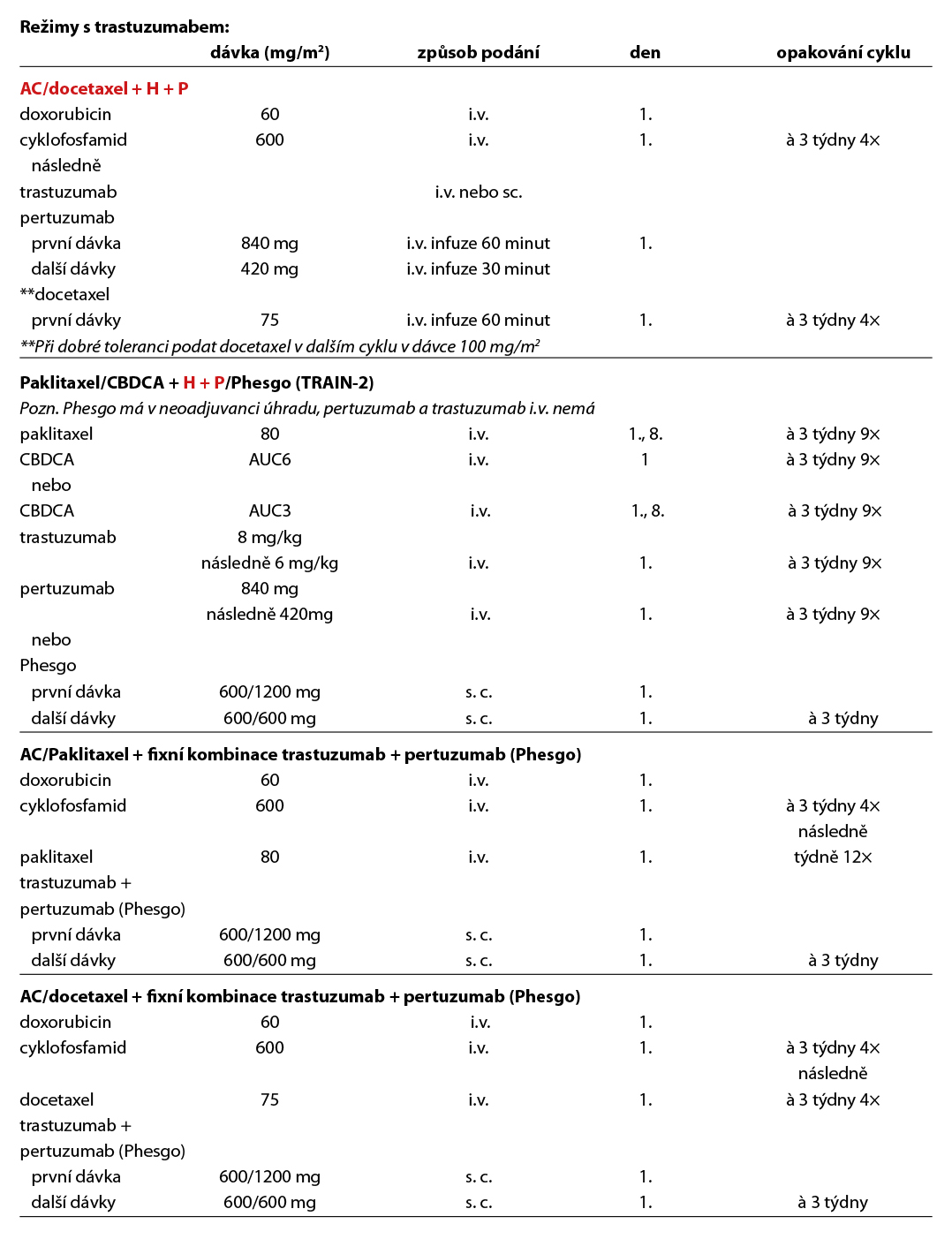
Před zahájením neoadjuvantní terapie je, v případě plánovaného prs záchovného výkonu nebo cílené axilární disekce, nutné zavedení klipu do nádoru v prsu a do bioptované axilární uzliny. Ve většině případů je volena sekvence antracyklinového režimu a taxánu nebo antracyklinového režimu a paklitaxelu s karboplatinou (pacientky s TNBC), podání dose-dense režimů je preferováno u všech podtypů. Možné je i podání neatracyklinových režimů, zvláště u pacientek s HER2 pozitivním karcinomem. Doporučuje se podat nejméně 6 cyklů CHT v rozmezí 4 až 6 měsíců. Veškerá plánovaná CHT by měla být podána před operací. U high-risk pacientek s TNBC ( cT2-4 a/nebo N+) je indikováno podání kombinace CHT a pembrolizumabu v i.v. nebo s.c. formě (KEYNOTE-522). Tato léčba zvyšuje pravděpodobnost dosažení pCR a zlepšuje dlouhodobé parametry léčebné odpovědi (EFS, OS). U pacientek s HER2 pozitivním karcinomem je standardem kombinace CHT a duální anti-HER2 terapie (NeoSphere, TRAIN2). Neoadjuvantní HT lze zvažovat u pacientek, u kterých není indikována neoadjuvantní ani adjuvantní CHT, a u kterých lze očekávat odpověď na HT (nádory s vysoce pozitivními HR, s nízkým gradem, s nízkým proliferačním indexem Ki67). U premenopauzálních pacientek je preferována kombinace ovariální suprese (OFS)+IA, u postmenopauzálních pacientek terapie inhibitorem aromatázy (IA). Doporučená doba podávání je 6–8 měsíců. Neoadjuvantní režimy jsou uvedeny v Tab. 2.
12.2.2 Adjuvantní systémová terapie
12.2.2.1 Adjuvantní chemoterapie
Adjuvantní CHT by měla být zvažována u TNBC, HER2 pozitivních nádorů a u nádorů luminálního typu, které jsou specifikovány níže. Adjuvantní terapie by zpravidla měla být zahájena do 3–6 týdnů po operačním výkonu, u TNBC do 4 týdnů.
A – u luminálního A podtypu karcinomu prsu je CHT doporučována při postižení 4 a více axilárních lymfatických uzlin a u nádorů prsu velikosti T3 a více.
B – u nádorů luminálních B HER2 negativních není podání CHT nezbytné u všech pacientek. Indikace CHT vychází z rozsahu postižení v prsu a ev. axile a biologického chování tumoru (exprese HR, hodnota proliferačního indexu Ki-67, nádorový grade a histologický typ onemocnění). U pacientek s malým rozsahem onemocnění lze podat pouze antracyklinový režim nebo kombinaci TC. Přidání taxanů by mělo být zvažováno u více extenzivního onemocnění. K posouzení hormonální senzitivity je možné podání krátkého režimu HT (2–4 týdny před operačním výkonem). V případě poklesu hodnoty Ki-67 pod 10 % se jedná o hormonálně senzitivní onemocnění a u těchto pacientek lze zvážit vynechání adjuvantní chemoterapie. V případě nejasného benefitu adjuvantní CHT je indikováno došetření pomocí multigenového testu (MammaPrint/BluePrint nebo Oncotype DX. Vyšetření je indikováno multidisciplinárním týmem v KOC. V případě nemožnosti provedení genomického testování lze použít jako surogátní marker hodnotu proliferačního indexu Ki-67. Pacientky s hodnotou Ki-67 ≤ 5 % by neměly být léčeny adjuvantní CHT, pacientky s hodnotou Ki-67 ≥ 30 % by měly být adjuvantní CHT léčeny. Jako pomocný nástroj k určení rizika recidivy nemoci a přínosu jednotlivých adjuvantních léčebných modalit (CHT, hormonoterapie) je možné použít kalkulátor rizika, např. Adjuvant Breast Cancer Tool, https://breast.predict.nhs.uk/tool. Multigenové testy jsou v ČR hrazeny při splnění podmínek uvedených v Tab. 3. Indikace konkrétního postupu v rámci adjuvantní terapie dle výsledku multigenového testování je znázorněna v Tab. 4 a Tab. 5.

C – u triple negativních nádorů je adjuvantní CHT založena ve většině případů na antracyklinech a taxanech. U nádorů nízkého rizika lze zvážit podání pouze antracyklinového režimu (např. AC) nebo TC. U high risk pacientek léčených kombinací CHT + pembrolizumab v rámci NAT je indikováno pokračování pembrolizumabem v monoterapii (9 cyklů à 3 týdny i.v. nebo s.c. bez ohledu na efekt neoadjuvantní terapie). V individuálních případech (toxicita léčby) lze u pacientek s pCR adjuvantní terapii pembrolizumabem nepodat. V případě reziduálního postižení po NAT zvážit u pacientek s gBRCAwt/gPALB2wt konkomitantní podání pembrolizumabu a kapecitabinu (6–8 cyklů), u pacientek s gBRCAm/gPALB2m je indikováno podání pembrolizuzmabu a následně olaparibu na dobu 1 roku. U pacientek po primárním operačním výkonu (≥pT2N0 nebo pN+) s germinální mutací BRCA1/2 nebo PALB2 je indikováno podání olaparibu na dobu 1 roku. Adjuvantní CHT lze vynechat u nízce rizikových tumorů (sekretorický, adenoidně cystický karcinom). Vynechání adjuvantní chemoterapie lze individuálně zvažovat u pacientek s malými tumory s vysokou infiltrací tumor infiltrujících lymfocytů. Doporučený léčebný postup u pacientek s TNBC je výše na Obr. 1.
D – v případě HER2 pozitivních tumorů by adjuvantní terapie měla být založena na kombinaci CHT a anti-HER2 terapie. Anti-HER2 terapie je indikována a hrazena pouze u pacientek s HER2 pozitivitou (IHC 3+, IHC 2+ s ověřenou amplifikací dle ISH) na základě vyšetření akreditované laboratoře. Duální anti-HER2 terapie je hrazena u pacientek s uzlinovým postižením po primárním operačním výkonu. Alternativou k i. v. podání duální anti-HER2 terapie je podání této kombinace podkožně (Phesgo). Pacientky s reziduálním postižením po neoadjuvantní terapii by měly být léčeny T-DM1 (do celkového počtu 14 cyklů). U rizikových HR+ pacientek s uzlinovým postižením lze po primárním operačním výkonu nebo NAT s reziduálním postižením (v prsu a/nebo uzlině) pokračovat po dokončení adjuvantní anti-HER2 terapie prodlouženou sekvenční terapií neratinibem na dobu 1 roku (není stanovena úhrada po adjuvantní duální anti-HER2 terapii, po adjuvantním podání T-DM1 je neratinib hrazen, zahájení do 12M od ukončení předchozí adjuvantní anti-HER2 léčby). Standardní délka podávání anti-HER2 terapie je 1 rok, u pacientek s nižším rizikem relapsu, komorbiditami nebo s vyšším rizikem kardiotoxicity lze individuálně zkrátit podávání anti-HER2 terapie na 6 měsíců. Součástí anti-HER2 terapie je pravidelná monitorace kardiálních parametrů. U pacientek s expresí HR je indikována adjuvantní HT. U pacientek s pozitivními HR, které jsou léčené v adjuvanci T-DM1, by měla být adjuvantní HT podávána konkomitantně. Adjuvantní radioterapii lze indikovat buď konkomitantně s T-DM1, nebo sekvenčně – nejdříve adjuvantní radioterapie, po skončení adjuvantní T-DM1.
Doporučený postup terapie u HER2 pozitivních pacientek je na Obr. 2.
Obecná doporučení pro adjuvantní chemoterapii
Nejčastěji používanými režimy jsou režimy založené na antracyklinech a taxanech, u selektovaných pacientek lze použít i režim CMF. Použití 4 cyklů AC je považováno za stejně efektivní jako použití 6 cyklů FEC100 u pacientek s N0 postižením (NSABP B36). Použití 4 cyklů AC je považováno za stejně efektivní jako 6 cyklů CMF. Přidání taxanu zvyšuje efektivitu CHT bez ohledu na N status, věk pacientek, velikost tumoru, grade nebo expresi HR. Režim s taxánem bez antracyklinů (4× TC) lze použít jako alternativu režimu 4× AC. CHT se doporučuje podávat 12–24 týdnů s ohledem na individuální riziko pacientky a dle vybraného režimu. V současné době je preferováno podání režimu AC v dose denzním schématu nejenom u TNBC a HER2 pozitivních nádorů, ale i u nádorů luminálních. V případě podání dose-dense režimu je nutné pacientku zajistit G-CSF.
Nejčastější kombinace cytostatik jsou uvedeny v Tab. 5. Taxany v adjuvantní léčbě je možné podat v následujících kombinacích: AC-T (doxorubicin, cyklofosfamid 4×, paklitaxel 4× à 21 dní, preferovaný paklitaxel weekly 12×), v kombinaci AC-D (ADM, CFA 4×, následně docetaxel 4× vše à 21 dní), TAC (docetaxel, doxorubicin, cyklofosfamid 6×), 4–6× TC (docetaxel, cyklofosfamid), v režimu 4× FEC 100 – paklitaxel weekly 100 mg/m2 8× nebo v režimu – 3× FEC 100 a 3× docetaxel (PACS 01).
Benefit adjuvantního podání bisfosfonátů je prokázán u postmenopauzálních pacientek s časným karcinomem prsu klinického stádi II a III, nezávisle na expresi hormonálních receptorů a uzlinového postižení. Terapie bisfosfonáty snižuje riziko relapsu onemocnění ve skeletu a vzniku osteoporózy. Adjuvantni režimy jsou uvedeny v Tab. 6.
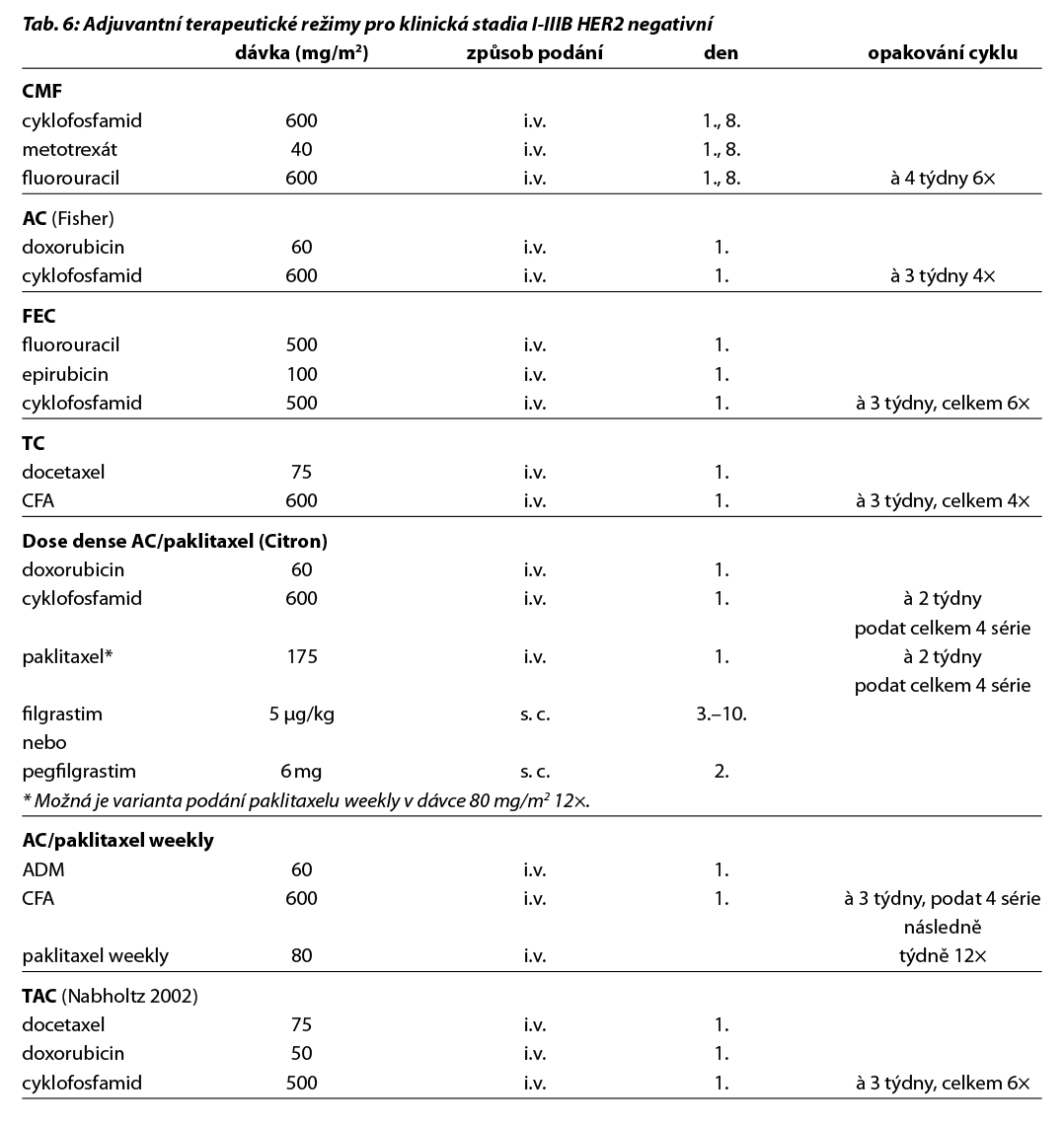
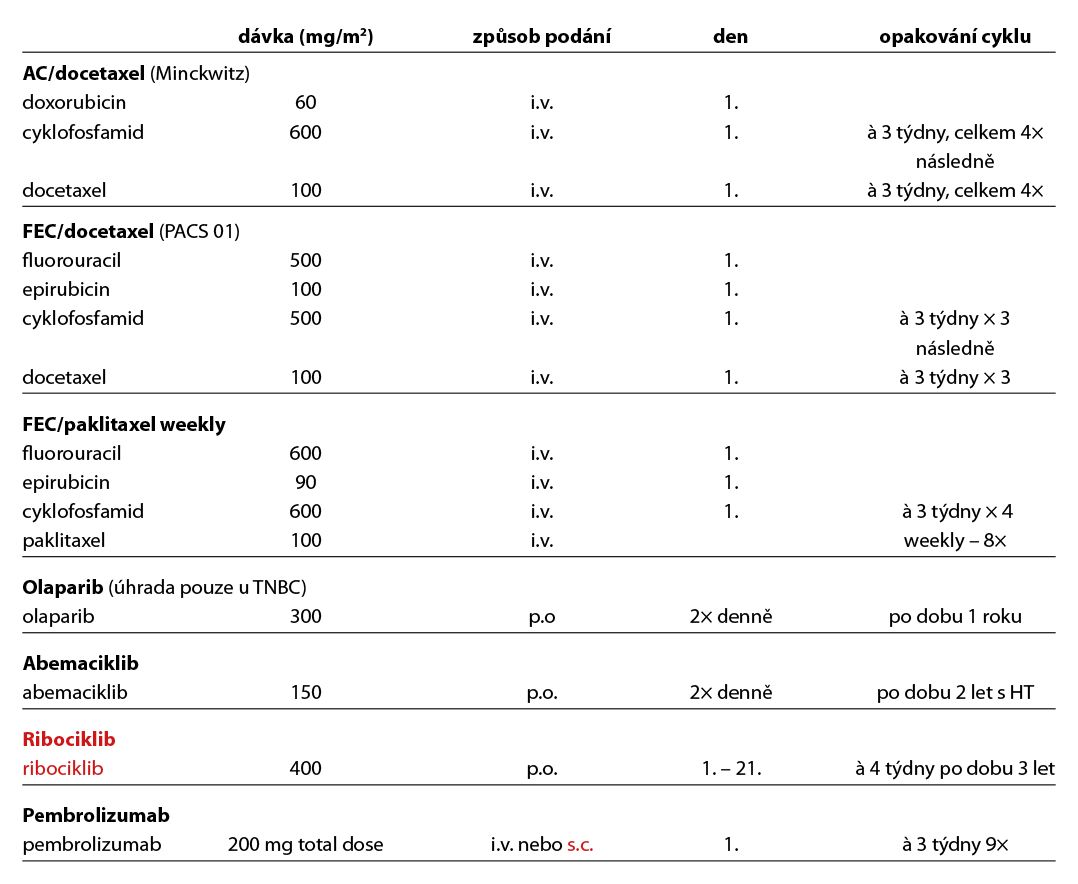
Adjuvantní terapeutické režimy pro klinická stadia I-IIIB HER2 pozitivní
Trastuzumab lze podávat v i. v. nebo s. c. formě. Při s. c. podání je fixní dávka 600 mg à 3 týdny, při i. v. podání je saturační dávka 8 mg/m2 a následně 6 mg/m2 (à 3 týdny) nebo 4 mg/m2 a následně 2 mg/m2 (weekly režim). Pertuzumab v kombinaci s trastuzumabem je podáván i. v., saturační dávka je 840 mg, následně se pokračuje dávkou 420 mg.
Neratinib je podáván v dávce 240 mg, po dobu jednoho roku.

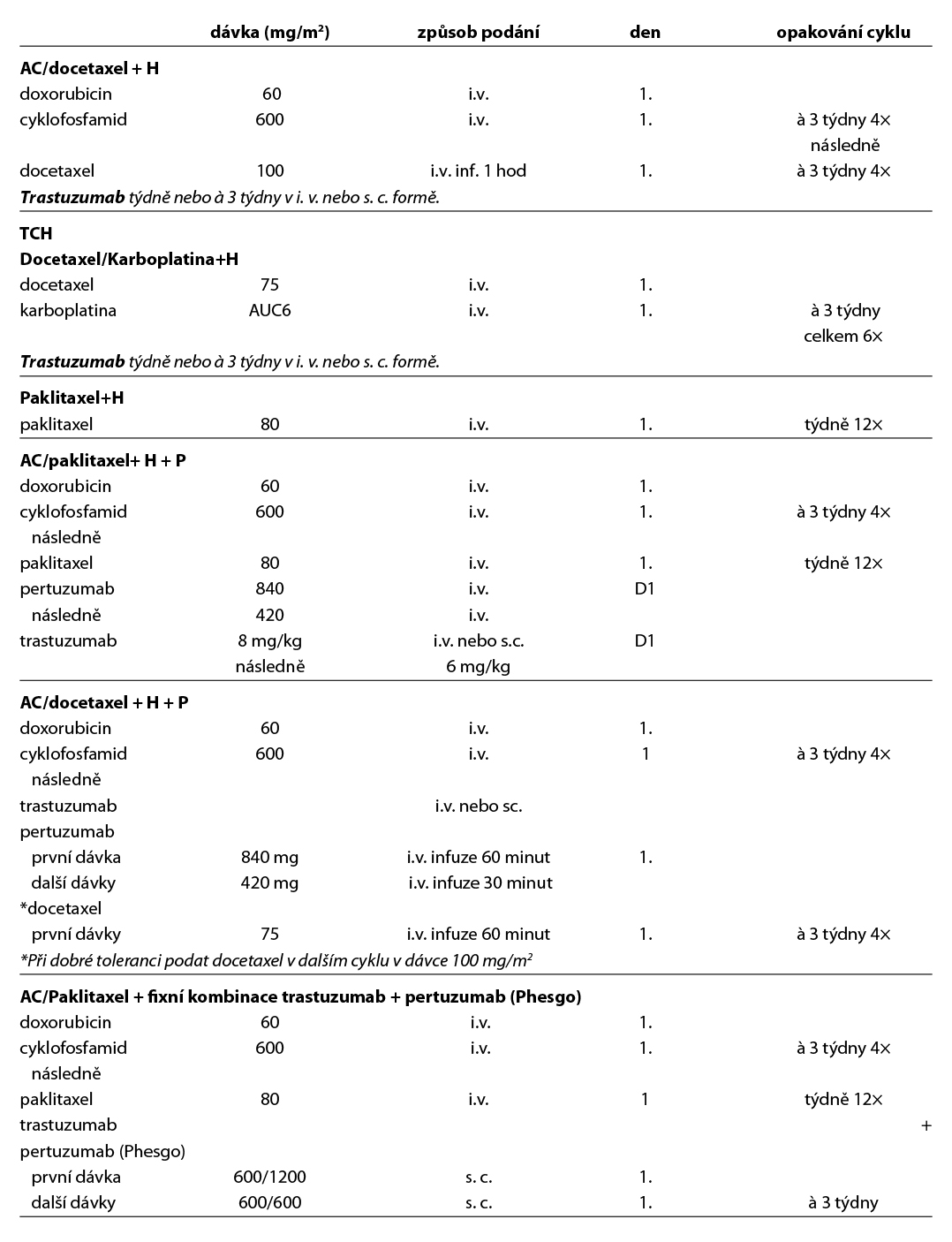
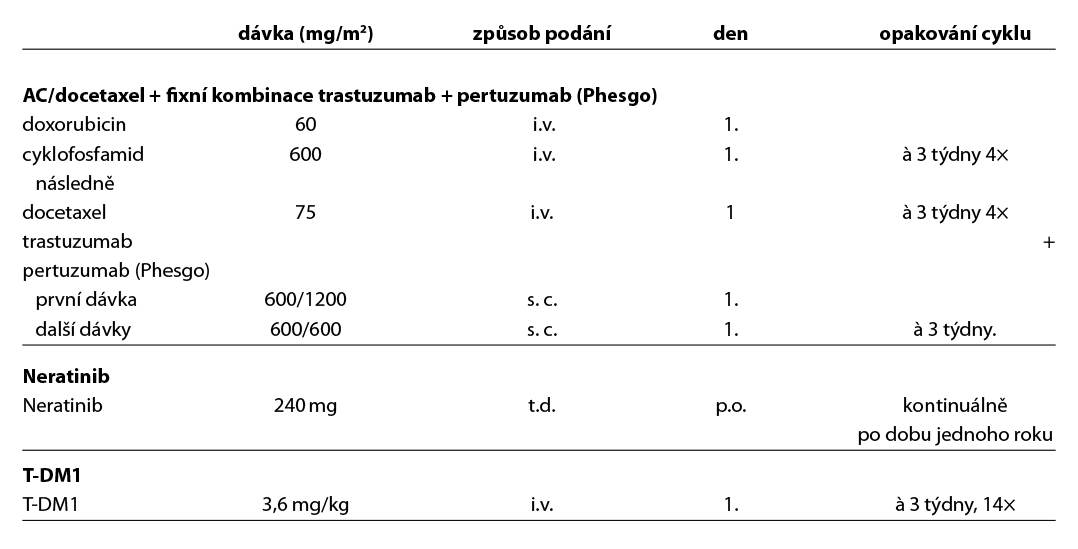
12.2.2.2 Adjuvantní hormonální a cílená terapie
Pre- nebo perimenopauzální pacientky
Všechny pacientky s pozitivitou HR by měly být léčeny adjuvantní HT. U pacientek s nízkým rizikem relapsu (I. klinické stádium) je standardem léčby TX v dávce 20 mg/den po dobu 5 let. V případě vyššího rizika relapsu je indikována OFS v kombinaci s TX (ve studii SOFT zlepšení DFS a OS) nebo IA (absolutní rozdíl v 8 letech u nemocných s vysokým rizikem relapsu >15 % při srovnání s léčbou samotným TX). Největší absolutní benefit z přidání OFS mají pacientky mladší 35 let, nemocné léčené adjuvantní CHT a pacientky, které nedosáhly postmenopauzálních hormonálních hladin po adjuvantní chemoterapii. Klinicky signifikantní benefit z podání IA vs TX pro celkové přežití mají dle dlouhodobých dat kombinované analýzy studií SOFT + TEXT (12letý follow-up) pacientky vysokého klinického rizika (ženy mladší 35 let, s nádory > 2 cm a grade 3 tumory). K identifikaci žen, které budou mít z eskalace léčby prospěch, je možné využít výpočet tzv. kompozitního rizika z tradičních prognostických znaků (tj. věk pacientky, velikost nádoru, grade, stav lymfatických uzlin, exprese HR a Ki67) po zadání do kalkulátoru, odečet benefitu OFS resp kombinace OFS + IA proti samotnému TX z grafu je možný zde: https://rconnect.dfci.harvard.edu/CompositeRiskSTEPP/.
Premenopauzální pacientky s vyšším rizikem relapsu by měly být léčeny TX až 10 let (benefit v parametru OS u pacientek s uzlinovým postižením). U žen, které se staly během 5 let užívání TX trvale postmenopauzálními, by měl být zvážen switch na IA (benefit v OS). U pacientek léčených CHT, u kterých dojde k obnově menstruace (během prvního roku až 2 let po CHT), by mělo být zváženo přidání OFS k HT. U žen mladších 35 let, jejichž onemocnění nevyžaduje podání adjuvantní CHT, je význam OFS nejasný, ale vzhledem k horší prognóze luminálních karcinomů v této věkové skupině je doporučeno podání nejefektivnější HT (HT + OFS). Mladé ženy s karcinomem prsu ve stádiu I nebo II, které nemohou užívat TX (z důvodu kontraindikací nebo závažných nežádoucích účinků), mohou být léčeny samotným LH-RH agonistou, oophorektomií nebo kombinací IA + LH-RH agonista. Podání IA bez OFS je u premenopauzálních žen kontraindikováno. U nemocných léčených OFS mají být monitorovány hladiny estradiolu, v případě nedostatečné suprese by měly být použity alternativní strategie (oophorektomie nebo samotný TX). Optimální délka OFS není známa, ačkoliv v recentních studiích byla standardem doba 5 let, obvyklá doba je 2–5 let. V případě, že je OFS indikována, měl by být použit goserelin 3,6 mg sc. 1× za 28 dní nebo je možno použít triptorelin v dávce 3 mg 1× za 28 dní (v této indikaci není hrazen). Je nutno mít na paměti, že u části pacientek LH-RH analoga nejsou účinná (ve studii SOFT mělo během prvního roku léčby 17 % pacientek trvale vyšší hodnoty estradiolu, než byl definovaný limit). Při terapii LH-RH analogy i při terapii s TX je vhodná pravidelná monitorace kostní denzity a krevního tlaku. Současné podávání inhibitorů CYP2D6 a TX není vhodné.
U vysoce rizikových pacientek s germinální mutací BRCA1/2 nebo PALB2 je indikováno podání olaparibu (OlympiA – pacientky s reziduálním postižením po neoadjuvantní terapii s CPS + EG score ≥ 3 nebo pacientky s postižením ≥ 4 lymfatických uzlin po primárním operačním výkonu).
U vysoce rizikových pacientek je indikováno podání HT a abemaciklibu na dobu 2 let (studie MonarchE) nebo HT a ribociklibu (NATALEE) na dobu 3 let. U pacientek s germinální mutaci BRCA1/2 nebo PALB2, které splňují kritéria pro podání olaparibu i abemaciklibu nebo ribociklibu , lze zvážit podání obou preparátů sekvenčně (adjuvantní podání olaparibu v kombinaci s HT, následně abemaciklib nebo ribociklib). Pro tento postup není stanovena úhrada.
Nežádoucí účinky HT (hot flashes) lze řešit farmakologicky – v případě TX není vhodné podávat paroxetin (CYP2D6), ale volit jiné léky z této skupiny – např. escitalopram 10mg. U pacientek léčených IA je naopak paroxetin v dávce 20 mg denně vhodný (prokázán efekt, indikace dle FDA).
Nově lze k ovlivnění nežádoucích účinků spojených s HT využít antagonistů NK3 (fezolinetant nebo elinzanetant). Léčba je hrazena pacientkou. V případě intolerance OFS+IA je vhodným postupem switch na OFS+TX, nebo pouze TX a to i u vysoce rizikových pacientek, kde by byl standardně volen IA (benefit jakékoliv HT je vyšší než předčasné ukončení terapie IA nebo špatná compliance ze strany pacientky z důvodu nežádoucích účinků).
Indikace adjuvantní terapie u pacientek s HR+/HER2- karcinomy je uvedena v Tab. 7.
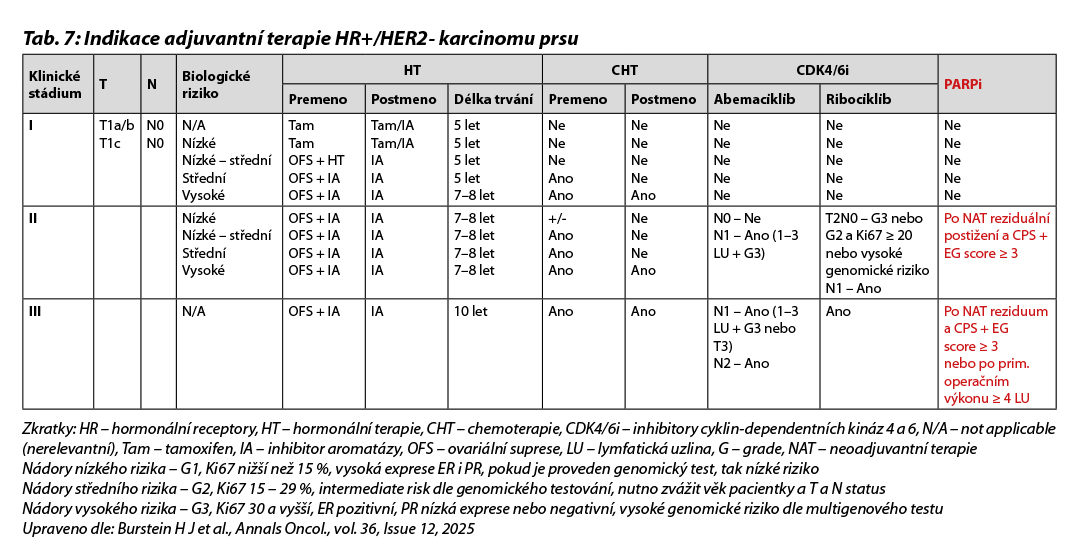
Postmenopauzální pacientky
Definice menopauzy dle NCCN 2022: předchozí bilaterální ovarektomie, věk ≥ 60 let, věk < 60 let a amenorea ≥ 12 měsíců za předpokladu, že není podávána CHT, TX nebo OFS a hladiny estradiolu a FSH jsou postmenopauzální. U žen mladších 60 let, léčených TX, pokud je estradiol a FSH v postmenopauzálním rozmezí. IA ve srovnání s TX přinášejí pacientkám asi 4% absolutní benefit v parametru DFS (pro upfront podání, switch po 2–3 letech léčby TX a prodlouženou léčbu po 5 letech TX), OS benefit je nesignifikantní (1–2 %). Podání IA déle než 5 let má význam pouze pro selektovanou skupinu nemocných s vyšším rizikem pozdního relapsu (velké tumory, pozitivní uzliny). Optimální trvání a režim HT není dosud znám. Léčbu doporučujeme podle individuálního rizika relapsu, komorbidit, profilu nežádoucích účinků a přání pacientky. Pacientky léčené TX nemají současně užívat inhibitory enzymu CYP2D6. V případě léčby IA má být monitorována kostní denzita (DEXA), zajištěn dostatečný přívod vápníku a vitamínu D. V případě použití IA u pacientek, které byly před CHT premenopauzální, je doporučována pravidelná monitorace hladin estradiolu a FSH, hlavně u pacientek mladších 45 let. Obdobně jako u premenopauzálních pacientek, tak i u postmenopauzálních, vysoce rizikových pacientek, je indikováno podání kombinace HT a abemaciklibu nebo IA a ribociklibu. U vysoce rizikových pacientek s gBRCA1/2 nebo PALB2 mutací je indikováno podání olaparibu (OlympiA). Management nežádoucích účinků je obdobný jako u premenopauzálních pacientek, v případě intolerance IA vhodná změna na TX i u vysoce rizikových pacientek. Přehled adjuvantní terapie je uveden v Tab. 7.
Adjuvantní bisfosfonáty: postmenopauzální pacientky středního a vysokého rizika (kyselina zoledronová 4 mg iv. 1× za 6 měsíců po dobu 3–5 let nebo klodronát 1200 mg denně perorálně 2–3 roky).
12.3 Stadium IV – metastatické onemocnění
Obecná doporučení léčby metastatického onemocnění
Při prvním relapsu onemocnění zvažovat provedení biopsie z metastatické léze k ověření subtypu karcinomu prsu (stanovení ER, PR, HER2 statusu, Ki67) a vyšetření prediktivních markerů – gBRCA a PALB2 mutace, somatická mutace PI3CA, ESR1 mutace, AKT mutace, PTEN mutace, exprese PD-L1.
Systémová terapie metastatického onemocnění je léčebným standardem, ale v určitých případech (oligometastatické onemocnění, ovlivnění symptomů) může být doplněna lokoregionální terapií (chirurgické metody, RT, RFA…).
V případě smíšené léčebné odpovědi pro diseminované je vhodné vzít v úvahu heterogenitu nádorového onemocnění a zvážit provedení rebiopsie (histologické vyšetření, individuálně provedení NGS). Odběr se doporučuje z progredující (CT) nebo aktivní (PET/CT) léze. Pokud je diskordance mezi fenotypem metastázy a primárního nádoru je indikováno druhé čtení vzorku z primárního nádoru.
Vzhledem k nádorové heterogenitě na úrovni nízké exprese HER2 a možnému vývoji exprese HER2 v průběhu onemocnění je vhodné u pacientek s původně negativním výsledkem HER2 exprese (IHC0) zvážit nové testování HER2 v průběhu onemocnění. U metastatického onemocnění je možné použít již dříve účinného léčebný režim (rechallenge).
Provedení NGS zvažovat v případě, že výsledek vyšetření může ovlivnit další léčebný postup. Vyšetření je indikováno multidisciplinárním týmem v KOC (MTB – Molecular tumor board).
Lokoregionální relaps onemocnění
U pacientek s lokoregionální recidivou onemocnění bez přítomnosti vzdáleného postižení by pacientka po operačním výkonu měla být léčena standardní adjuvantní terapií. U pacientek s lokoregionálním relapsem TNBC lze zvážit podání neoadjuvantní chemoterapie v kombinaci s pembrolizumabem. U pacientek indikovaných k adjuvantní hormonální léčbě pro lokoregionální relaps onemocnění zvážit zařazení adjuvantních CDK 4/6i, pokud splňují kritéria pro jejich podání. Přítomnost vzdáleného postižení by měla být vyloučena pomocí PET/CT nebo FES PET/CT (luminální karcinomy, lobulární karcinomy, indikace cestou MDT v KOC, nutné vysazení fulvestrantu – cca 6 měsíců a tamoxifenu – cca 3 měsíce před provedením vyšetření).
Oligometastatické onemocnění
U nemocných s de novo metastatickým onemocněním (stádium IV v době diagnózy) operace prsu nezlepšuje celkové přežití (OS). Oligometastatické onemocnění (1, maximálně 2 MTS léze) má být léčeno multimodálně. Pacientka má být došetřena pomocí PET/CT, FES PET/CT (doporučení viz. výše) nebo celotělového MR. Primárně je indikována systémová terapie. V závěru léčby má být použita další, definitivní léčba v místě metastatického onemocnění (operace, radioterapie). Je doporučeno histologické ověření takové léze biopsií. Konkrétní léčebný postup u pacientek s oligometastatickým onemocněním je vhodné konzultovat v rámci MDT. V případě 3 a více metastatických ložisek má být onemocnění léčeno podle standardů pro pokročilé onemocnění, se zařazením lokální léčby dle symptomů.
12.3.1 Léky ovlivňující metabolismus kosti (BMA – bone modifying agents)
- bisfosfonáty (klodronát + ibandronát p.o., zoledronát, pamidronát, ibandronát i.v.)
- monoklonální protilátka denosumab
Indikovány při zjištění osteolytických, osteoblastických nebo smíšených metastáz do osového skeletu (dg. dle radiologických metod – RTG, CT, MRI).
Všechny pacientky by měly mít vyšetření dutiny ústní a případné dentální zákroky by měly být provedeny před zahájením terapie BMA.
Z důvodu zvyšující se incidence osteonekrózy čelisti při dlouhodobém podávání některých bisfosfonátů je u těchto nutno zvážit benefit terapie trvající déle než 2 roky. Dle nových dat lze zoledronát již iniciálně podávat 1× za 3 měsíce. Denosumab je podáván 1× za 4–6 týdnů (data bezpečnosti na dobu 5 let).
12.3.2 Terapie metastatického HR+/HER2 negativního karcinomu prsu:
Definice hormonální rezistence:
Primární hormonální rezistence: k progresi onemocnění dojde v prvních 2 letech podávání adjuvantní HT nebo do 6 měsíců podání první linie HT u metastatického onemocnění.
Sekundární (získaná) hormonální rezistence: k progresi onemocnění dojde po více jak 2 letech podávání adjuvantní HT nebo do 12 měsíců od ukončení adjuvantní HT nebo za více jak 6 měsíců od zahájení úvodní HT pro metastatický karcinom prsu.
Premenopauzální pacientky jsou léčeny stejně jako postmenopauzální pacientky. Je nutné provést OFS nebo ablaci. Možné metody ablace (suprese): chirurgická bilaterální adnexektomie, podání LH-RH analog, radiační kastrace.
Výběr úvodní linie u luminálního MBC je závislý na typu a délce adjuvantní HT, DFI, rozsahu postižení, biologickému věku pacientky, PS, potřebě rychlé kontroly nemoci, preferencím pacientky, na sociálně-ekonomických a psychologických faktorech, na spolupráci pacientky.
První linie léčby:
Kombinace HT a inhibitoru CDK 4/6 (palbociklib, ribociklib, abemaciklib) je standardní léčebnou modalitou. Použít lze kombinaci IA + inhibitoru CDK 4/6, popř. fulvestrant + inhibitor CDK 4/6 – volba kombinace dle parametrů viz výše. Na základě výsledků klinických studií je preferovaným CDK 4/6i do první linie léčby v kombinaci s inhibitorem aromatázy pro pre- ale i postmenopauzální pacientky ribociklib.
U skupiny pacientek relabujících na adjuvantní HT nebo do 12 měsíců od jejího ukončení je indikováno testování somatických mutací a v případě PI3CAm je možno podat kombinaci fulvestrant + palbociklib + inavolisib (studie INAVO120). Lze také podat pouze HT samotnou – IA, TX nebo fulvestrant (hrazen pouze u pacientek nepředléčených HT a bez viscerálních MTS) a to u skupiny pacientek se závažnými komorbiditami nebo při špatném PS, při non-compliance pacientky. U pacientek s viscerální krizí je lékem volby paliativní CHT, lze však volit i kombinaci IA + ribociklibu (studie RIGHT Choice). U pacientek s HER2-low karcinomem, u kterých došlo k relapsu v průběhu adjuvantní CHT nebo do 6 měsíců po jejím ukončení je možné podání T-DXd.
Druhá linie léčby:
Po selhání kombinace HT+ inhibitor CDK 4/6 – vhodné stanovení prediktorů: gBRCA/PALB2, PI3CA, ESR1, PTEN, AKT. Optimální sekvence 2. a dalších linií není jednoznačně známá, záleží na výběru předchozí léčby v neo/adjuvanci, kombinaci v 1. linii, trvání efektu předchozí linie léčby rozsahu onemocnění, preferencích pacientky a mutačním stavu výše uvedených prediktorů. Léčebné možnosti jsou:
- fulvestrant + CDK4/6i (pokud nebyl podán v rámci I. linie),
- exemestan + everolimus,
- v případě PIK3CA mutace kombinace alpelisib + fulvestrant (PI3CAm) nebo kombinace kapivasertib + fulvestrant (PI3CAm, AKTm nebo PTEN loss),
- v případě BRCA1/2 nebo PALB2 mutace PARP inhibitor – olaparib (úhrada pouze pro pacientky nevhodné k další HT a nepředléčené CHT pro metastatické onemocnění) nebo talazoparib,
- v případě ESR1 mutace elacestrant nebo imlunestrant,
- fulvestrant + everolimus,
- monoterapie – fulvestrant, TX,
- CHT – preferována u pacientek s hrozícím orgánovým selháním.
Třetí a další linie léčby:
U pacientek s hormonálně sensitivním onemocněním je vhodné pokračovat v HT lékem, který doposud nebyl použit. U nádorů hormonálně rezistentních je preferována CHT – v monoterapii, preference kombinované CHT pouze při výrazných klinických symptomech a hrozícímu orgánového selhání. Z cytostatik lze volit antracyklin, taxan, kapecitabin, eribulin, vinorelbin, gemcitabin – sekvence jednotlivých cytostatik dle NÚL, předléčení, PS, compliance, preference pacientky. U pacientek s již limitovanými léčebnými možnostmi lze provést NGS vyšetření, ideálně z aktuálně provedené biopsie. Cílem je detekovat genovou alteraci, kterou lze léčebně ovlivnit. Terapii lze podat na základě doporučení MTB (molekulárního tumor boardu), úhradu je nutno následně řešit přes paragraf 16.
U pacientek s HR+/HER2-low karcinomem (IHC 1+ nebo 2+ bez amplifikace HER2 genu dle ISH/FISH), předléčených minimálně jedním režimem CHT pro metastatické onemocnění, je indikováno podání trastuzumabu deruxtekanu.
U pacientek HR+/HER2 0 dle IHC, které v rámci předchozí léčby podstoupily HT a alespoň dvě další systémové terapie pro pokročilé onemocnění, je indikována terapie sacituzumabem govitecanem. Pacientky splňující kritéria k léčbě více konjugáty mohou být léčeny jejich sekvencí, jednoznačná data o efektivitě tohoto postupu však nejsou k dispozici. Léčebná strategie HR+/HER2 negativního metastatického karcinomu prsu je zobrazena na Obr. 4.
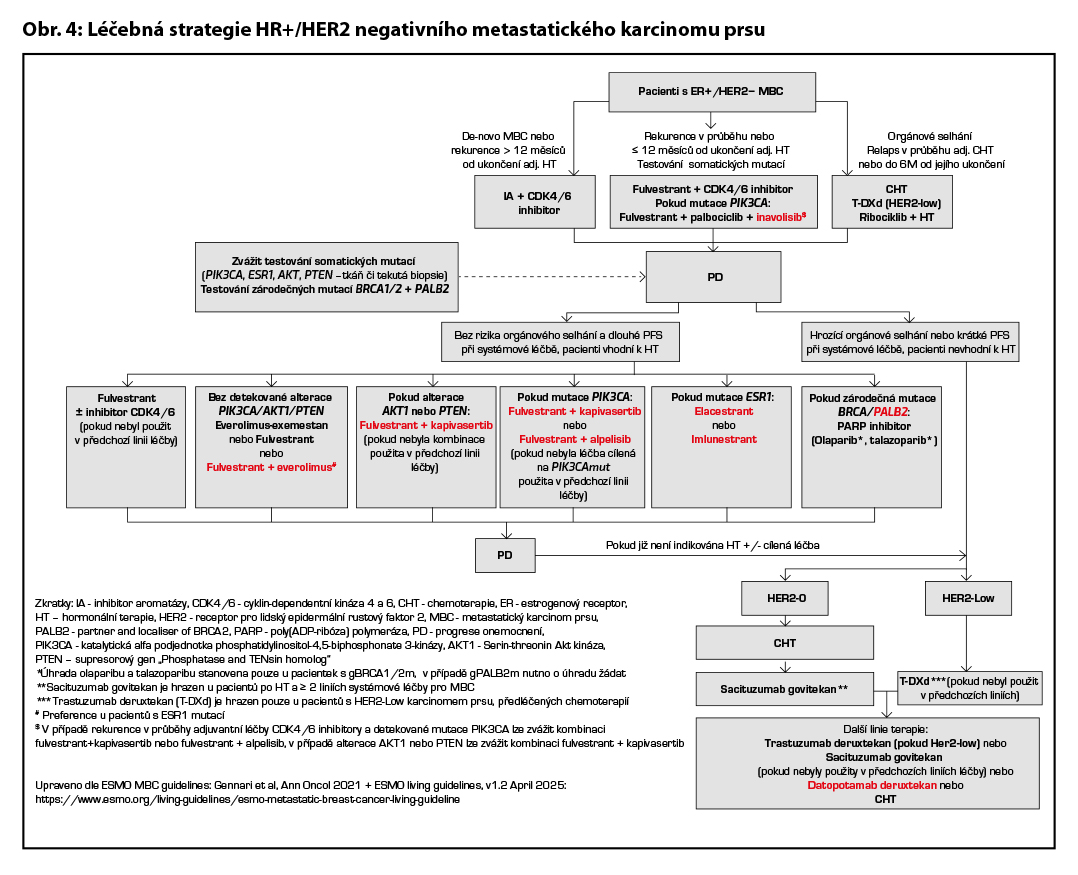
12.3.3 Terapie metastatického HER2 pozitivního karcinomu prsu
Všechny pacientky s HER2 pozitivním metastatickým karcinomem prsu by měly být léčeny anti-HER2 léčbou. Výjimkou jsou pouze ty pacientky, u kterých je anti-HER2 léčba kontraindikována. Po selhání první linie anti-HER2 léčby by měla být pacientce nabídnuta další linie anti-HER2 léčby (kontinuální anti-HER2 blokáda je zásadní k dosažení dlouhodobé kontroly onemocnění). Léčba je dlouhodobá, s přihlédnutím k benefitu a možným komplikacím. U pacientek s dlouhodobou remisí metastatického onemocnění (≥2 roky) je možným postupem přerušení/ukončení anti-HER2 léčby a sledování pacientky, deeskalace anti-HER2 léčby (např. T+P→T nebo T-DXd→T) nebo kontinuální pokračování v iniciálně voleném režimu do progrese/relapsu onemocnění.
První linie léčby
Nejefektivnější léčbou v 1. linii je kombinace taxánu a duální anti-HER2 terapie (trastuzumab + pertuzumab). Pokud má pacientka kontraindikaci k taxanům, lze použit vinorelbin nebo kapecitabin. Po ukončení alespoň 6 cyklů konkomitantní léčby s CHT by měly být pacientky léčené udržovací léčbou trastuzumab + pertuzumab. U pacientek s HR+ přidat HT, u premenopauzálních pacientek v kombinaci s OFS. U HR+/HER2+ pacientek s dosažením léčebné odpovědi v 1. linii lze k udržovací duální HER2 blokádě a IA přidat ještě palbociklib na základě výsledků klinické studie PATINA (palbociklib nemá v této indikaci schválení EMA, ESMO guidelines tuto možnost uvádějí).
Druhá linie léčby
Nejefektivnějším preparátem v rámci 2. linie po progresi onemocnění na kombinaci taxán + trastuzumab/pertuzumab je T-DXd (DESTINY-Breast03). Výrazný benefit přináší T-DXd i u pacientek s mozkovým MTS postižením (aktivní i stabilní léze) dle výsledků studie DESTINY-Breast12). Pokud byly pacientky léčeny v rámci I. linie T-DXd, lze jim ve 2. linii nabídnout kombinaci trastuzumab + kapecitabin + tukatinib, hlavně u pacientek s aktivním mozkovým postižením.
Třetí a další linie léčby
Volba terapie ve třetí a vyšších liniích léčby vždy závisí na léčbě v liniích předchozích, celkovém stavu pacientky i toxicitě předchozí léčby. Lze volit (dle předchozí léčby a přítomnosti aktivních mozkových metastáz) mezi léčbou kombinací tucatinib + kapecitabin + trastuzumab, T-DXd, T-DM1 (nemá úhradu po pertuzumabu a lapatinibu), případně pak lapatinib v kombinaci s kapecitabinem, lapatinibem v kombinaci s trastuzumabem či kombinací trastuzumabu s CHT . Po vyčerpání cílené HER2 blokády lze volit i samotnou CHT. Léčebná strategie metastatického HER2 pozitivního karcinomu prsu je zobrazena na Obr. 5 a Obr. 6.
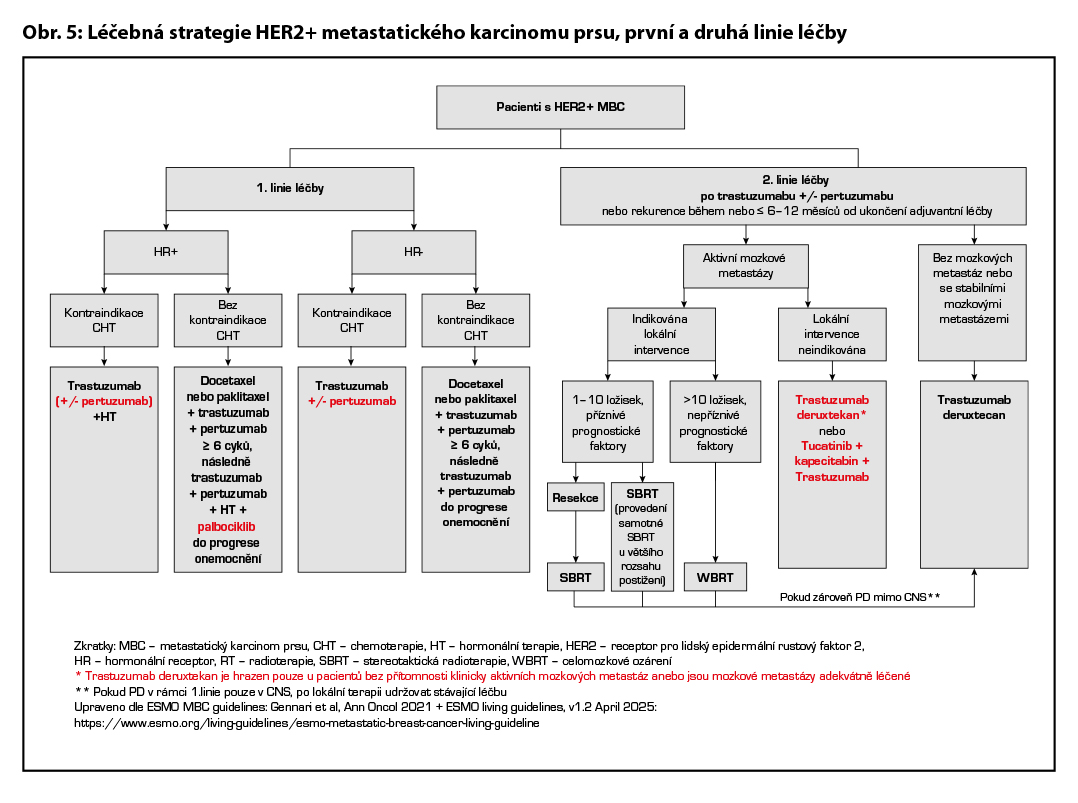
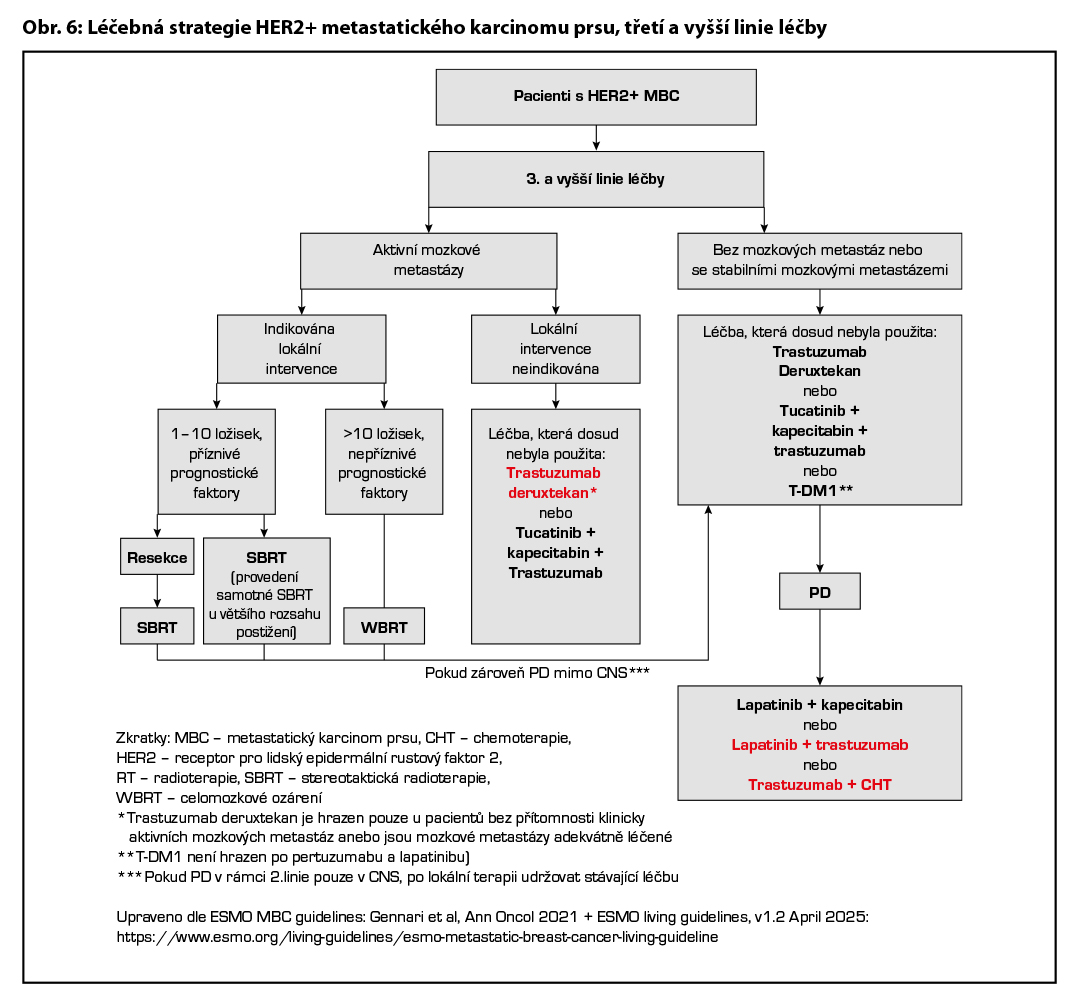
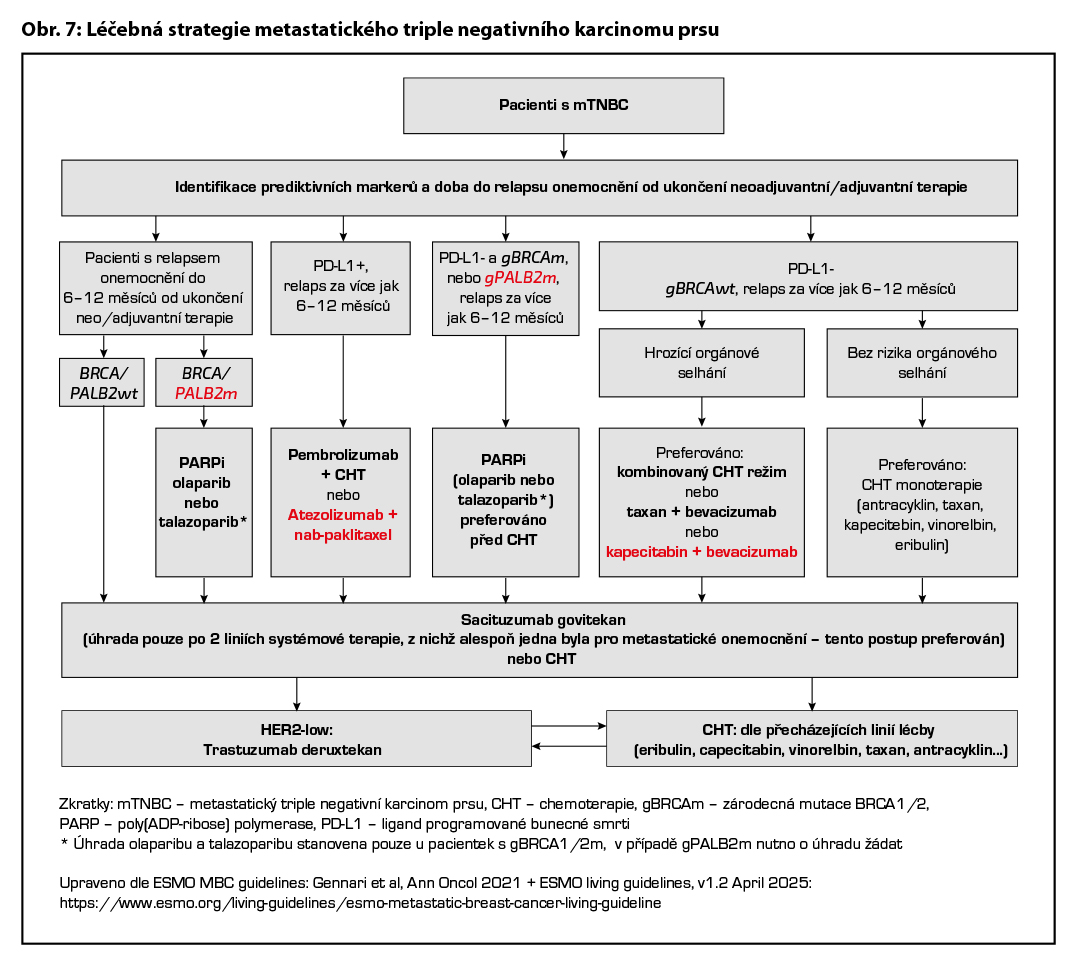
12.3.4 Terapie metastatického triple negativního karcinomu prsu
Terapie metastatického TNBC je aktuálně volena na základě výsledku prediktivních markerů. Dále je nutno zvážit, zda se jedná o de novo metastatického onemocnění nebo relaps onemocnění po předcházející neoadjuvantní/adjuvantní terapii a za jak dlouho k relapsu onemocnění došlo. U pacientek s rychlým relapsem onemocnění (≤ 6–12 měsíců) je v případě BRCA1/2 nebo PALB2 mutace indikována terapie PARP inhibitorem. U pacientek bez přítomnosti germinální BRCA1/2 nebo PALB2 mutace je nejefektivnější léčbou sacituzumab govitecan. U pacientek PD-L1+ s de novo metastatickým onemocněním nebo s relapsem po delší době jak 6–12 měsíců je indikováno podání kombinace imunoterapie (atezolizumab nebo pembrolizumab) a CHT, přičemž musí být splněna indikační kritéria pro pozitivitu PD- L1 (pro atezolizumab ≥1 % dle Ventana SP142, nebo CPS ≥10 pro pembrolizumab). Pacientky PD-L1- se zárodečnou mutací BRCA1/2 nebo PALB2 nejsou vhodné k léčbě PARP inhibitory (olaparib, talazoparib) za podmínky, že byly léčeny CHT s antracykliny a taxany v rámci neoadjuvantní nebo adjuvantní terapie. Olaparib je hrazen pouze u pacientek, které nebyly doposud léčeny chemoterapií pro metastatické onemocnění. Talazoparib může být použit i u pacientek léčených pro metastatické onemocnění CHT nebo kombinací CHT a IT. U pacientek se zárodečnou mutací PALB2 není olaparib ani talazoparib hrazen. Pokud je u této skupiny volena CHT, je vhodné zvážit podání platinového derivátu. U pacientek PD-L1 negativních s absencí zárodečné mutace BRCA1 nebo BRCA2 je léčba založena na CHT. U pacientek v dobrém klinickém stavu, s rychle progredujícím onemocněním a hrozícím orgánovým selháním lze volit kombinovaný chemoterapeutický režim s cílem dosažení co nejrychlejší léčebné odpovědi. U ostatních pacientek je vhodná léčba monoterapií. Konkrétní chemoterapeutický režim je volen dle klinického stavu pacientky, předchozí léčby a její efektivity. Při progresi onemocnění je preferováno podání sacituzumabu govitecanu (pokud nebyl použit iniciálně) v rámci II. linie léčby při splnění úhradových podmínek (alespoň dvě linie systémové léčby, z nichž alespoň jedna byla pro metastatické onemocnění). Při progresi onemocnění po II. linii léčby lze při dobrém klinickém stavu pacientky a léčebné odpovědi na předcházející linie pokračovat další linií paliativní CHT.
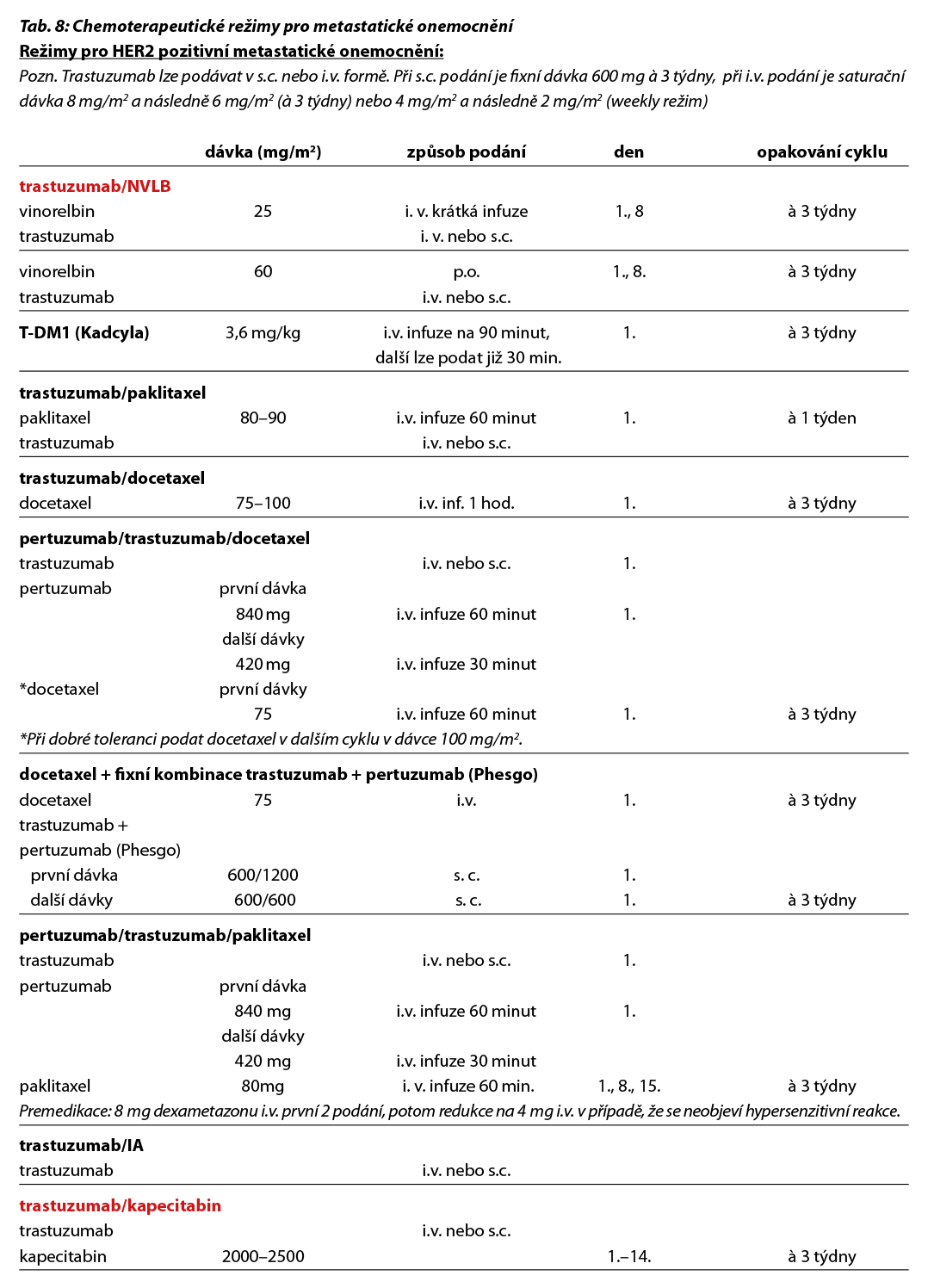
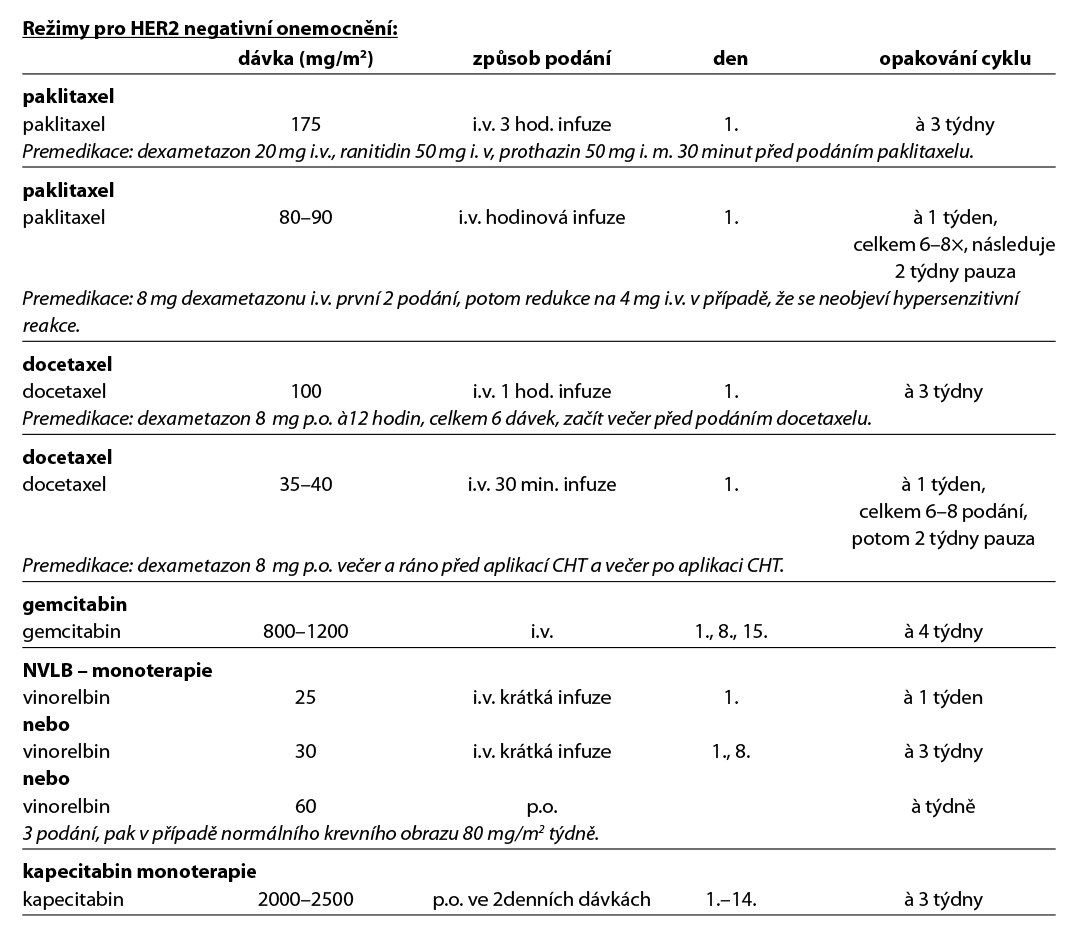
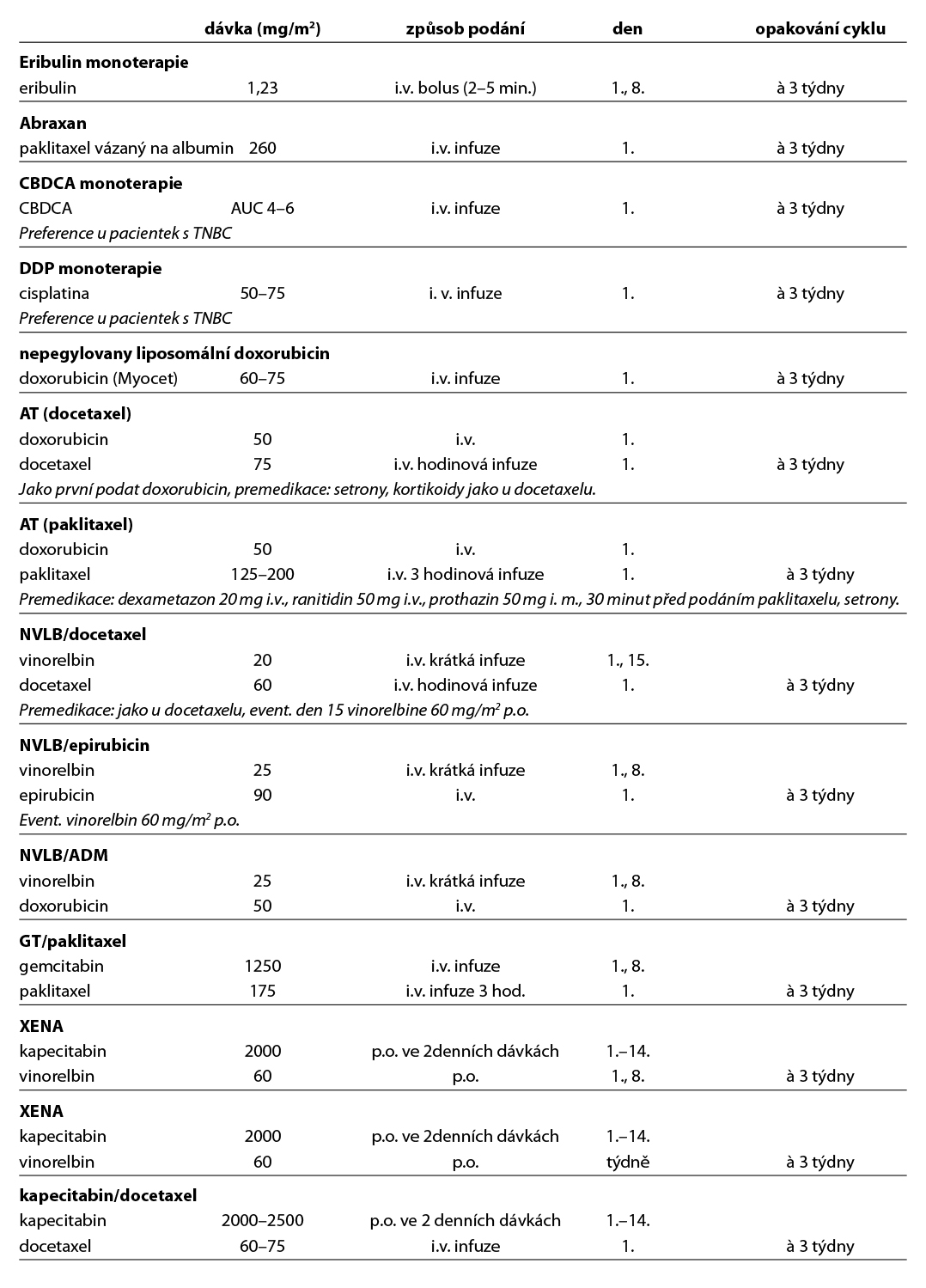
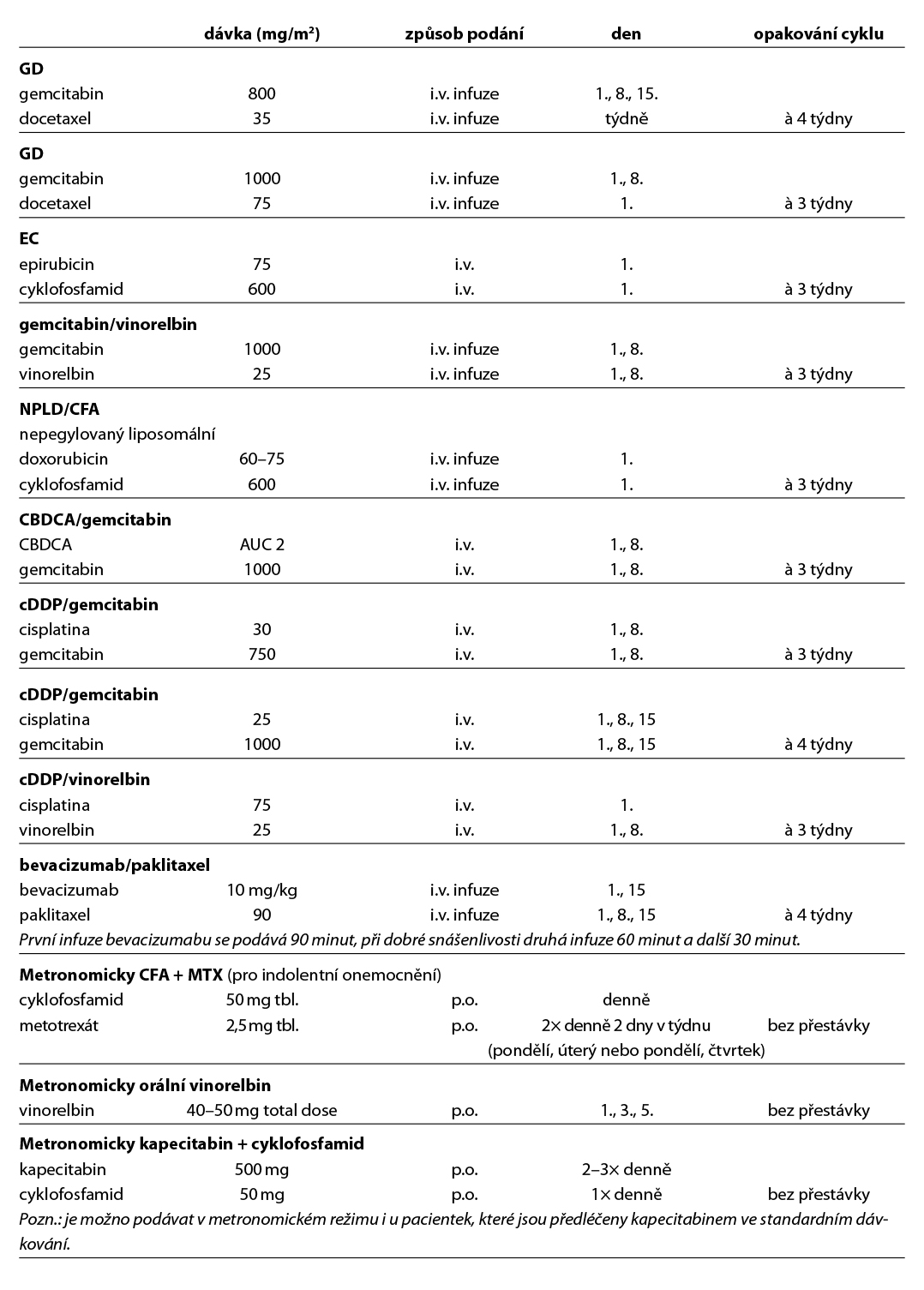
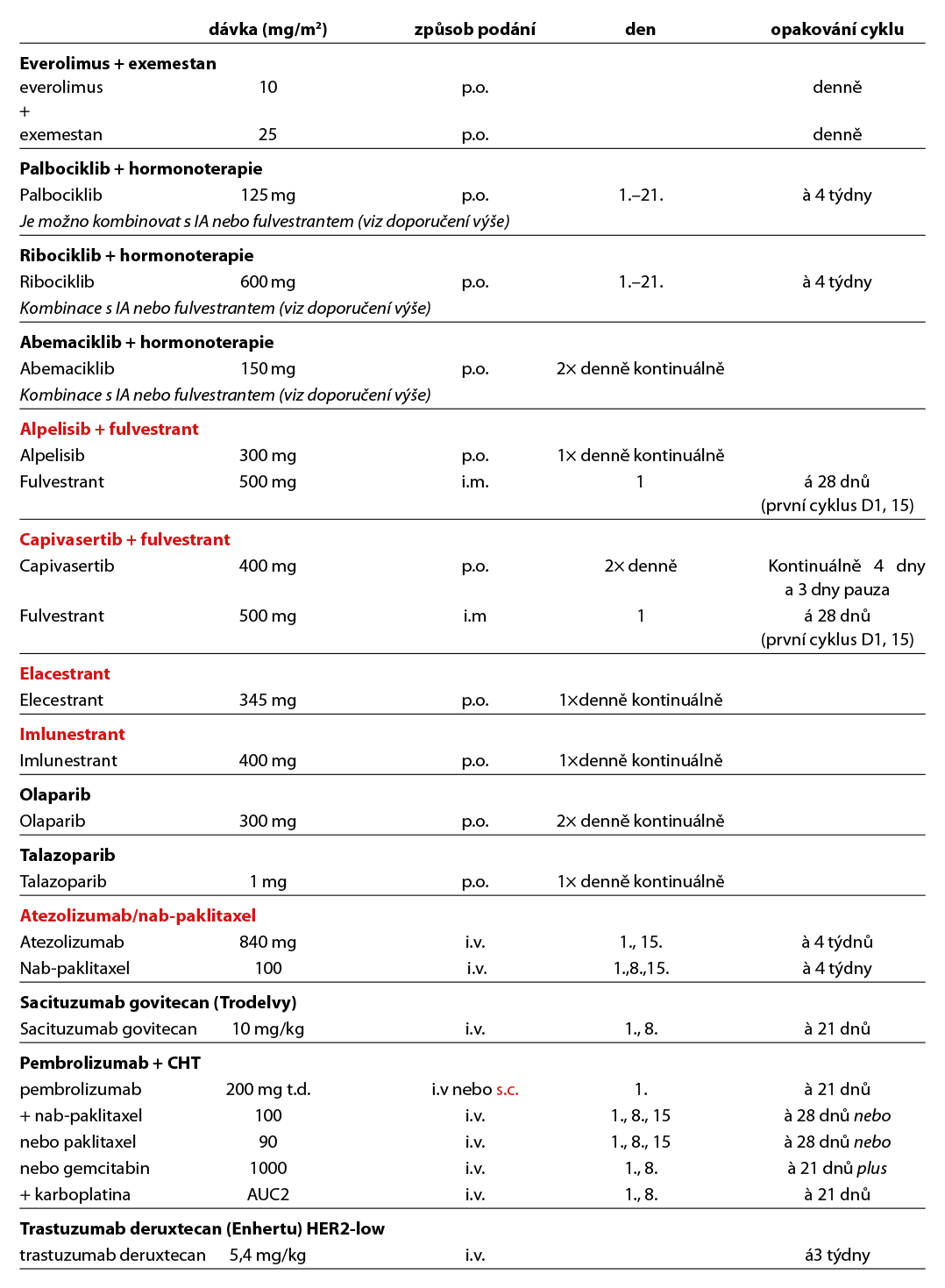
U pacientek s HER2-low karcinomem prsu je možné sekvenční podání T-DXd po terapii sacituzumabem govitecanem. Prospektivní data o efektivitě tohoto postupu nejsou k dispozici. Obecné doporučení pro léčbu metastatického triple negativního karcinomu prsu je zobrazeno na Obr. 7. Přehled režimů, které lze použít v rámci léčby metastatického karcinomu prsu, je uveden v Tab. 8.

12.4. Terapie karcinomu prsu u mužů
Terapie je analogií léčby karcinomu prsu u žen. Každý pacient by měl být indikován ke genetickému testování.
Časný karcinom prsu u mužů
U časného karcinomu prsu je terapie stejně jako u žen indikována na základě fenotypu nádoru. Adjuvantní CHT je indikována stejně jako u ženského karcinomu prsu. Adjuvantní HER2 blokáda je indikována stejně jako u ženského karcinomu prsu. V adjuvantní HT je preferován TX. Délka standardně na 5 let. U pacientů, kteří dobře HT tolerují a mají vysoké riziko relapsu onemocnění lze pokračovat v podávání TX do celkové doby 10 let. Možno je zvolit i IA, ale ten by měl být vždy podáván současně s LH-RH analogy. U mužů by neměly být podávány bisfosfonáty v adjuvantní indikaci redukce relapsu onemocnění.
Metastatický karcinom prsu u mužů
U HR+/HER2 – nádorů je indikována HT +- s podáním inhibitoru CDK4/6. Lze podat palbociklib a ribociklib, pro tyto preparáty jsou k dispozici data, pro ribociklib není stanovena úhrada, palbociklib je hrazen u mužů s mBC v dávce 125 mg a 100 mg. Dále je možno podat TX, fulvestrant a IA s LH-RH analogy v sekvencích stejně jako u ženského karcinomu prsu. Cílená terapie podle HR, HER2 statutu, PDL-1 statutu, mutace v PIK3CA a mutace v BRCA1/2 by měla mít stejné indikace a kombinace stejně jako je tomu u ženského karcinomu prsu. Potřeba je vždy ale kontrola, zda je úhrada i pro muže s nádorem prsu, většinově tomu tak není.
12.5 Doporučení pro follow-up pacientek po léčbě pro karcinom prsu stádia I-III
Klinické vyšetření jedou za 3–4 měsíce během prvních 2 let (každých 6 měsíců u pacientek s nízkým rizikem relapsu nebo DCIS), každých 6–8 měsíců 3.–5. rok (interval dle rizika relapsu). Bilaterální MG jednou za rok, s doplněním UZ nebo MRI dle potřeby. Provedení UZ zvážit hlavně u pacientek s lobulárním karcinomem prsu. U asymptomatických pacientek nejsou další vyšetření (biochemie, nádorové markery, RTG plic, UZ jater, CT, PET/CT) doporučena. Pravidelné vyšetření kostní denzity u pacientek léčených IA nebo OFS. Vhodné pacientky nabádat ke zdravému životnímu stylu (pravidelné cvičení, kontrola váhy). HRT by u pacientek po terapii pro karcinom prsu neměla být indikována. U pacientek po bilat. mastektomii (s/bez rekonstrukce) není pravidlené vyšetřování pomocí zobrazovacích metod indikováno.
Literatura:
- ESMO Living Guideline Metastatic Breast Cancer, v1.2 - April 2025
- Burstein, H. J., et al. “Tailoring treatment to cancer risk and patient preference: the 2025 St Gallen International Breast Cancer Consensus Statement on individualizing therapy for patients with early breast cancer.” Annals of Oncology (2025).
- Gennari, A., André, F., Barrios, C. H., Cortes, J., De Azambuja, E., DeMichele, A., ... & Harbeck, N. (2021). ESMO Clinical Practice Guideline for the diagnosis, staging and treatment of patients with metastatic breast cancer. Annals of oncology, 32(12), 1475-1495.
- Balic, M., Thomssen, C., Gnant, M., & Harbeck, N. (2023). St. Gallen/Vienna 2023: Optimization of Treatment for Patients with Primary Breast Cancer–A Brief Summary of the Consensus Discussion. Breast Care, 18(3), 213-222.
- Gradishar, W. J., Moran, M. S., Abraham, J., Abramson, V., Aft, R., Agnese, D., ... & Kumar, R. (2023). NCCN Guidelines® Insights: Breast Cancer, Version 4.2023: Featured Updates to the NCCN Guidelines. Journal of the National Comprehensive Cancer Network, 21(6), 594-608.
- Allison, K. H., Hammond, M. E. H., Dowsett, M., McKernin, S. E., Carey, L. A., Fitzgibbons, P. L., ... & Wolff, A. C. (2020). Estrogen and progesterone receptor testing in breast cancer: ASCO/CAP guideline update.
- Wolff, A. C., Hammond, M. E. H., Allison, K. H., Harvey, B. E., Mangu, P. B., Bartlett, J. M., ... & Dowsett, M. (2018). Human epidermal growth factor receptor 2 testing in breast cancer: American Society of Clinical Oncology/College of American Pathologists clinical practice guideline focused update. Archives of pathology & laboratory medicine, 142(11), 1364-1382.
- NCCN Guidelines Breast Cancer, ver. 1.2025, https://www.nccn.org/login?ReturnURL=https://www.nccn.org/professionals/physician_gls/pdf/breast.pdf
- Loibl, S., André, F., Bachelot, T., Barrios, C. H., Bergh, J., Burstein, H. J., ... & Harbeck, N. (2024). Early breast cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Annals of Oncology, 35(2), 159-182.
