U pacientek s karcinomem děložního hrdla stádia I-IVB by před zahájením jakékoliv léčby včetně operačního výkonu měl být léčebný postup konzultován v rámci multidisciplinárního týmu (MDT). Pacientka by měla být znovu konzultována cestou MTD po provedení operace. Oligometastatické onemocnění (1, maximálně 2 MTS léze) má být léčeno multimodálně. Konkrétní léčebný postup u pacientek s oligometastatickým onemocněním by měl být konzultován v rámci MDT. U nemocných s de novo metastatickým onemocněním (stádium IV v době diagnózy) je primárně preferovaná systémová léčba se zařazením lokální léčby dle symptomů.
Molekulární prediktivní vyšetření u karcinomu děložního čípku
Pokročilé onemocnění (stadium III a stadium IV): exprese PD-L1 – CPS skóre (při zvažované kombinované terapii s pembrolizumabem).
Fakultativně: HER 2, MSI-H/dMMR/TMB-H, NTRK fúze, eventuálně NGS testování dle indikace lokálního MDT.
15.1 Léčba časných stadií onemocnění
Standardem je chirurgická léčba do stádia IB2 včetně (u stádií IB3 a IIA2, tedy u bulky tumorů, se postup může lišit dle věku, polymorbidity ženy a jejího přání). Preferovaným přístupem k radikální hysterektomii je laparotomie. Minimálně invazivní přístupy (laparoskopie, robotická chirurgie) jsou akceptovatelným postupem u vybraných karcinomů do stadia IB1 bez rizikových faktorů. U nádorů do 2 cm bez hluboké invaze do stromatu je dostačujícím výkonem prostá hysterektomie, u větších nádorů radikální hysterektomie. U nádorů do 4 cm je výkon kombinován s biopsií sentinelové lymfatické uzliny oboustranně, v případě jednostranné detekce je vyžadována na straně bez detekce systematická pánevní lymfadenektomie. U nádorů nad 4 cm je standardním výkonem pro lymfatický staging systematická pánevní lymfadenektomie. Při peroperační pozitivitě sentinelové uzliny je doporučeno upustit od hysterektomie i pánevní lymfadenektomie (s výjimkou extirpace bulky uzlin) a může být provedena nízká (tj. do dostupu a. mesenterica inferior) stagingová paraaortální lymfadenektomie, nebo extirpace bulky uzlin v paraaortální oblasti.
U žen požadujících zachování fertility je volen individualizovaný management s rozsahem chirurgického výkonu na děložním hrdle dle velikosti nádoru a lokalizace nádoru. Standardní indikací jsou nádory do velikosti 2 cm v největším rozměru s negativitou sentinelových uzlin.
Všechny ženy s invazivním karcinomem mají být referovány po diagnostickém výkonu do Onkogynekologického centra k dovyšetření a rozvaze MDT.
Stádium IA
- Konizace, vaginální prostá trachelektomie nebo prostá hysterektomie
- IA1 + LVSI nebo IA2 - SLNB
- Alternativou chirurgické léčby je EBRT na pánev + BRT (pokud pacientka není schopna operace).
Stadium IB1/IB2/IIA1
- Prostá hysterektomie u nádorů do 2 cm bez hluboké invaze do stromatu, pokud bylo dosaženo zdravých okrajů z konizace
- Radikální hysterektomie (typ C1 nebo C2) u nádorů nesplňujících výše uvedená kritéria
- Hysterektomie v kombinaci se SLNB u nádorů do 4 cm, u nádorů větších v kombinací se systematickou pánevní lymfadenektomií (19.)
- Alternativou chirurgické léčby je primární kombinovaná chemoradioterapie (EBRT+BRT+CHT) – pokud operace není první volba
Stadium IB3, IIA2
- Primární kombinovaná chemoradioterapie (EBRT+BRT+CHT) – pokud operace není první volba
- Radikální hysterektomie typ C2, SLNB, pánevní lymfadenektomie

15.2 Léčba pokročilého a recidivujícího onemocnění
15.2.1 Lokálně pokročilá a metastatická onemocnění
Lokálně pokročilá onemocnění jsou léčena RT nebo konkomitantní CH/RT. U vzdáleného oligometastatického onemocnění je indikována resekce s/nebo bez následné radioterapie. V případě, že kompletní resekce není možná, lze zvážit lokální ablativní metody s/nebo bez radioterapie nebo samotnou RT eventuálně konkomitantní CHT/RT. V případě mnohočetné diseminace onemocnění je indikována paliativní chemoterapie, ev. v kombinaci s bevacizumabem (po zvážení individuálního rizika vzniku píštělí). Kombinace platinového derivátu s paklitaxelem je preferovaný režim. U pacientek s PD-L1 pozitivními nádory s kombinovaným pozitivním skóre ≥1 je indikována kombinace s pembrolizumabem.
Stadium IIB, IIIA, IIIB, IVA
- Primární kombinovaná chemoradioterapie (EBRT+BRT+CHT)
U stádia III a IVA (dle FIGO klasifikace z roku 2014 – tedy T3,T4 s/nebo bez N+) lze přidat k chemoradioterapii i imunoterapii Keytrudou na základě registrační studie KEYNOTE-A18 / ENGOT-cx11.

Přípravek KEYTRUDA je v kombinaci s chemoradioterapií (zevní radioterapií následovanou brachyterapií) indikován k léčbě lokálně pokročilého karcinomu děložního hrdla stadia III - IVA dle FIGO 2014 u dospělých, kteří dosud nepodstoupili definitivní léčbu. Indikace není závislá na PDL-1 statusu.
Léčba podléhá schválení RL.
Alternativou je podání indukční chemoterapie (dose-dense Paklitaxel 80mg/m2/CBDCA AUC2) následované chemoradioterapií dle studie INTERLACE:
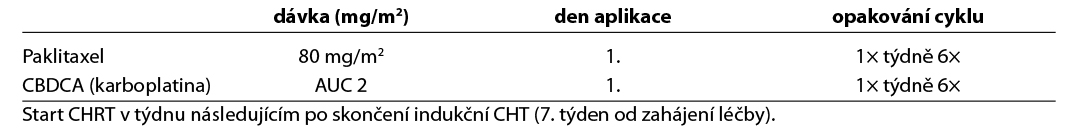
Stadium IVB
- Paliativní CHT +/- bevacizumab* +/- pembrolizumab** +/- pánevní RT***.
* po zvážení individuálního rizika vzniku urogenitálních či intestinálních píštělí
** PD-L1 pozitivní nádor s kombinovaným pozitivním skóre ≥1
*** při dobré odpovědi vzdáleného metastatického onemocnění
Léčba pembrolizumabem je hrazena v kombinaci s chemoterapií (zahrnující platinový derivát + paklitaxel) s nebo bez bevacizumabu v léčbě perzistentního, recidivujícího nebo metastazujícího karcinomu děložního hrdla s expresí PD-L1 s CPS více nebo rovno 1.
15.2.2 Léčba recidivujícího onemocnění
Management léčby lokoregionálních recidiv je závislý na předchozí léčbě, kterou pacientka absolvovala s adjuvantním či kurativním záměrem. Pokud pacientka neabsolvovala RT, je možné nabídnout samotnou RT nebo konkomitantní CHT/RT.
U centrální recidivy v oblasti pánve by vždy měla být zvážena možnost chirurgické léčby (exenterace pánve v případě centrální recidivy nebo laterálně extendovaná resekce v případě laterální recidivy). V případě pacientek po RT, kde chirurgická exstirpace s dosažením kompletní resekce není možná, je indikována paliativní chemoterapie. U pacientek s PD-L1 pozitivním nádorem s kombinovaným pozitivním skóre ≥1 je možné přidání pembrolizumabu.
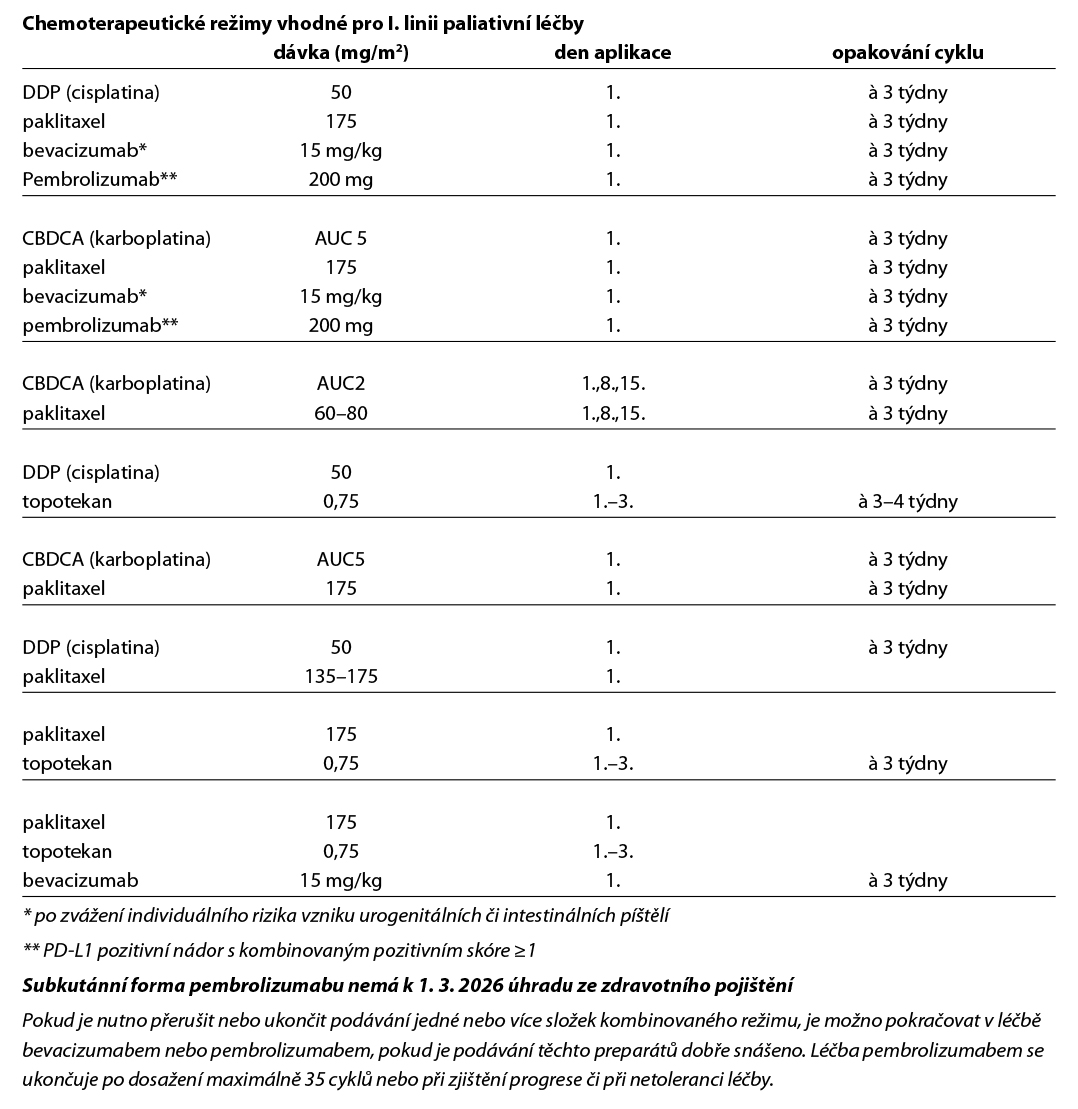
V monoterapii I. linie lze použít: DDP, CBDCA, ifosfamid, topotekan, paklitaxel.
Ve 2. linii léčby lze použít: docetaxel, ifosfamid, epirubicin, topotekan, gemcitabin, 5-fluorouracil.
U pacientek s MSI-H/dMMR tumory nepředléčené imunoterapií lze zvážit po schválení na paragraf 16 aplikaci pembrolizumabu.
U pacientek s progresí po předchozí léčbě s platinovým derivátem, které nebyly předléčeny imunoterapií, je ke zvážení imunoterapie s cemiplimabem. Indikace tohoto preparátu je nezávislá na PDL-1 statusu.
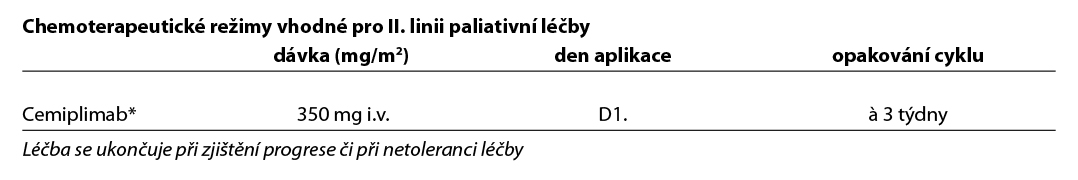
Literatura:
- Plante M, Kwon JS, Ferguson S, Samouelian V, Ferron G, Maulard A, de Kroon C, Van Driel W, Tidy J, Williamson K, Mahner S, Kommoss S, Goffin F, Tamussino K, Eyjolfsdottir B, Kim JW, Gleeson N, Brotto L, Tu D, Shepherd LE; CX.5 SHAPE investigators; CX.5 SHAPE Investigators. Simple versus Radical Hysterectomy in Women with Low-Risk Cervical Cancer. N Engl J Med. 2024 Feb 29;390(9):819-829. doi: 10.1056/NEJMoa2308900. PMID: 38416430.
- Potter R, Haie-Meder C, Van Limbergen E, et al. Recommendations from gynaecological (GYN) GEC ESTRO working group (II): concepts and terms in 3D image-based treatment planning in cervix cancer brachytherapy-3D dose volume parameters and aspects of 3D image-based anatomy, radiation physics, radiobiology. Radiother Oncol 2006;78:67-77.
- Viswanathan AN, Erickson BA. Three-dimensional imaging in gynecologic brachytherapy: a survey of the American Brachytherapy Society. Int J Radiat Oncol Biol Phys 2010;76:104-109.
- del Carmen MG, McIntyre JF, Goodman A. The role of intraoperative radiation therapy (IORT) in the treatment of locally advanced gynecologic malignancies. Oncologist 2000;5:18-25.
- Monk BJ, Sill MW, McMeekin DS, et al. Phase III trial of four cisplatin-containing doublet combinations in stage IVB, recurrent, or persistent cervical carcinoma: A Gynecologic Oncology Group Study. J Clin Oncol 2009 0:JCO.2009.21.8909.
- Moore DH, Blessing JA, McQuellon RP, et al. Phase III study of cisplatin with or without paclitaxel in stage IVB, recurrent, or persistent squamous cell carcinoma of the cervix: a gynecologic oncology group study. J Clin Oncol. 2004;22:3113-3119.
- Moore KN, Herzog TJ, Lewin S, et al. A comparison of cisplatin/paclitaxel and carboplatin/paclitaxel in stage IVB, recurrent or persistent cervical cancer. Gynecol Oncol 2007;105:299-303.
- Long HJ, 3rd, Bundy BN, Grendys EC, Jr., et al. Randomized phase III trial of cisplatin with or without topotecan in carcinoma of the uterine cervix: a Gynecologic Oncology Group Study. J Clin Oncol 2005;23:4626-4633.
- Tewari KS, Sill M, Long HJ, et al. Incorporation of bevacizumab in the treatment of recurrent and metastatic cervical cancer: A phase III randomized trial of the Gynecologic Oncology Group [abstract]. J Clin Oncol 2013;31:Abstract 3.
- Brewer CA, Blessing JA, Nagourney RA, et al. Cisplatin plus gemcitabine in previously treated squamous cell carcinoma of the cervix. Gynecol Oncol 2006;100:385-388.
- Tewari KS1, Sill MW, Long HJ 3rd, et al. Improved survival with bevacizumab in advanced cervical cancer. N Engl J Med. 2014 Feb 20;370(8):734-43.
- Kitagawa R, Katsumata N, Shibata T, et al. A randomized, phase III trial of paclitaxel plus carboplatin (TC) versus paclitaxel plus cisplatin (TP) in stage IVb, persistent or recurrent cervical cancer: Japan Clinical Oncology Group study (JCOG0505) [abstract]. J Clin Oncol 2012;30(Suppl 15):Abstract 5006.
- Weiss GR, Green S, Hannigan EV, et al. A phase II trial of carboplatin for recurrent or metastatic squamous carcinoma of the uterine cervix: a Southwest Oncology Group study. Gynecol Oncol 1990;39:332-336.
- Kudelka AP, Winn R, Edwards CL, et al. An update of a phase II study of paclitaxel in advanced or recurrent squamous cell cancer of the cervix. Anticancer Drugs 1997;8:657-66.
- Blatha N., Berek J.S., Fredes M.C. et al.: Revised FIGO staging for carcinoma of the cervix uteri. Int J Gynecol Obstet 2019, Apr;145:129-135.
- Cibula D, Mburu A, Planchamp F, Zapardiel I, Atallah D, Al-Rubaish S, Baiocchi G, Elghazaly H, Heredia F, Guzha B, Kamfwa P, Lertkhachonsuk AA, Mahantshetty U, Martinez Perez DA, Matylevich O, Mukhopadhyay A, Nasser S, Pareja R, Sehouli J, Slimane M, Vieira M, Refky B, Nout R. European Society of Gynaecological Oncology resource-stratified guidelines for the management of patients with cervical cancer. Int J Gynecol Cancer. 2026 Jan;36(1):102747. doi: 10.1016/j.ijgc.2025.102747. Epub 2025 Oct 17. PMID: 41494219.
- Cibula D, Marnitz S, Jarkovský J, Kocián R, Dundr P, Klát J, Zapardiel I, Arencibia O, Landoni F, Presl J, Raspagliesi F, Zikán M, van Lonkhuijzen LR, Torne A, Sláma J, Minar L, Ostojich M, Pilka R, Petiz AF, Petzel A, Burgetová A, Fischerová D, Nemejcova K, Köhler C. Sentinel lymph node biopsy without systematic pelvic lymphadenectomy in females with early-stage cervical cancer: final outcome of the SENTIX prospective, single-arm, noninferiority, international trial. Nat Cancer. 2025 Sep;6(9):1585-1594. doi: 10.1038/s43018-025-01016-y. Epub 2025 Jul 4. PMID: 40615729.
- Cibula D, Rosaria Raspollini M, Planchamp F, Centeno C, Chargari C, Felix A, Fischerová D, Jahnn-Kuch D, Joly F, Kohler C, Lax S, Lorusso D, Mahantshetty U, Mathevet P, Raj Naik M, Nout RA, Oaknin A, Peccatori F, Persson J, Querleu D, Rubio Bernabé S, Schmid MP, Stepanyan A, Svintsitskyi V, Tamussino K, Zapardiel I, Lindegaard J. ESGO/ESTRO/ESP Guidelines for the management of patients with cervical cancer - Update 2023. Radiother Oncol. 2023 Jul;184:109682. doi: 10.1016/j.radonc.2023.109682. Epub 2023 May 1. PMID: 37336614.
- Plante M, Kwon JS, Ferguson S, Samouëlian V, Ferron G, Maulard A, de Kroon C, Van Driel W, Tidy J, Williamson K, Mahner S, Kommoss S, Goffin F, Tamussino K, Eyjólfsdóttir B, Kim JW, Gleeson N, Brotto L, Tu D, Shepherd LE; CX.5 SHAPE investigators; CX.5 SHAPE Investigators. Simple versus Radical Hysterectomy in Women with Low-Risk Cervical Cancer. N Engl J Med. 2024 Feb 29;390(9):819-829. doi: 10.1056/NEJMoa2308900. PMID: 38416430.
