Zahrnuje skvamozní karcinom (lokalizován zejména v proximálních 2/3 jícnu) a adenokarcinom (v distálním jícnu a gastroezofageální junkci). Posouzení strategie léčby probíhá cestou multidisciplinární komise. Primární léčba je založena na lokalizaci a rozsahu nádoru, histologickém typu, komorbiditách/PS pacienta. Všem pacientům by mělo být poskytnuto komplexní nutriční poradenství, od běžné plnohodnotné stravy, přes enterální až po kompletní parenterální výživu. Všem pacientům by rovněž měla být nabídnuta rehabilitační a psychoonkologická péče.
Kritéria ke konzultaci multidisciplinárního týmu:
- všichni noví pacienti
- oligometastatické postižení, je-li zvažována lokální léčba – definice oligometastatického onemocnění: DOI: 10.1016/j.ejca.2024.114062
- pacienti zvažovaní k indikaci HIPEC či PIPAC
Doporučené léčebné postupy jsou kategorie 1, není-li uvedeno jinak.
Chirurgická léčba
Chirurgická resekce karcinomu jícnu (ezofagektomie) je indikována u resekabilního nádoru jícnu a ezofagogastrické junkce (EGJ) ve stadiu I–IV a vždy po individuálním posouzení multidisciplinární komise. Za resekabilní se považuje primární nádor T1 až T4a (invaze do resekabilních struktur jako pleura, perikard či bránice). Za neresekabilní se považuje nádor T4b invadující okolité vitální či neresekabilní struktury (trachea, bronchy, srdce, obratel, velké cévy mediastina). Chirurgická léčba se týká všech oddílů jícnu s výjimkou krčního jícnu (horní okraj tumoru < 5 cm od horního jícnového svěrače dle ezofagoskopie), kde je preferována definitivní chemoradioterapie. Vyjímečně lze i zde volit chirurgické řešení, a to v případě nemožnosti podání definitivní CHRT, nebo lokální persistence či recidivě nádoru po definitivní CHRT – tzv. salvage ezofagektomie. Klíčovým faktorem úspěšnosti chirurgické resekce je vzhledem k náročnosti výkonu a zátěže pro pacienta optimální selekce pacientů schopných prodělat extenzivní chirurgický výkon. Mandatorní je zhodnocení kardiopulmonální rezervy a nutričního stavu pacienta. Důležitá je adekvátní předoperační příprava včetně rehabilitace a nutriční intervence. V případě kurativní léčby se nedoporučuje zavádět jícnový stent ani provádět PEG či chirurgickou gastrostomii (riziko poškození žaludečního konduitu). Doporučena je enterální nutrice cestou naso-enterální sondy nebo chirurgické jejunostomie, v případě těžší malnutrice a dysfagie. Rozsah resekce jícnu a typ výkonu je dán lokalizací nádoru a rozsahem nádorového postižení včetně uzlin. Dále zde hraje roli i expertíza operatéra. Preferované operační výkony jsou dvoudutinová transtorakální Ivor Lewis ezofagektomie s náhradou jícnu žaludečním konduitem a s konstrukcí anastomozy v hrudníku (indikovaná u nádorů EGJ a distálního jícnu) a transtorakální McKeown ezofagektomie, při které je anastomóza na žaludek lokalizovaná na krku (indikovaná u nádorů středního a horního hrudního jícnu, alternativně i distálního jícnu a EGJ). Další možné operační přístupy zahrnují levou torako-abdominální ezofagektomii (solitární operační přístup z levé torakofrenolaparotomie, vhodný zejména u objemných tumorů EGJ vyžadující gastrektomii a resekci distálního jícnu) a transhiatální ezofagektomii s krční anastomózou, která vynechává torakotomii a je spojena s nižší respirační pooperační morbiditou, ale taky nižší onkologickou radikalitou. V případě karcinomu EGJ kardie je indikace ezofagektomie jednoznačná u nádoru typu Siewert I, a u nádorů Siewert II, kde orální konec nádorů zasahuje více jak 3 cm nad ezofagogastrickou junkci. U nádorů Siewert II invadujících <3 cm jícnu není optimální postup vyjasněn (je možná ezofagektomie i proximálně extendovaná gastrektomie). Nádory typu Siewert III jsou léčeny jako primární nádory žaludku, tedy gastrektomií s rozšířením resekce na distální jícen transhiatálně. Ve výjimečných případech rozsáhlých nádorů postihujících žaludek i jícen bez významného postižení uzlin je možná ezofagogastrektomie. První volbou náhrady jícnu je žaludek (ve formě tubulizovaného konduitu), při nemožnosti jeho použití (stavy po resekci žaludku či prorůstání nádoru) může být použito jejunum nebo tlusté střevo, a to v původní lokalizaci v zadním mediastinu či retrosternálně. Technika konstrukce anastomózy je záležitostí preference chirurga, může být ručně šita, polomechanická s použitím lineárního stapleru či kompletně mechanická pomocí cirkulárního stapleru. Lokalizace anastomózy (hrudník vs krk) závisí na lokalizaci tumoru a preferenci chirurga. Krční anastomózy jsou spojeny s častějším, ale méně závažným anastomotickým leakem a častější parézou levého zvratného nervu. Nedílnou součástí operačního výkonu je lymfadenektomie. Standardní lymfadenektomie vždy zahrnuje disekci spádových abdominální uzlin v rozsahu D1+ a periezofageálních uzlin dolního mediastina včetně bifurkačních uzlin. Rozšířená lymfadenektomie zahrnuje disekci i horních mediastinálních uzlin vpravo nebo i vlevo podle lokalizace tumoru (střední a horní hrudní nádory) a klinické suspekce na lymfadenopatii. V indikovaných případech se může jednat o tzv. lymfadenektomii 3 polí, tj. včetně disekce krčních uzlin. Za adekvátní se považuje odstranění nejméně 15 lymfatických uzlin, u lokálně pokročilých tumoru T3-T4a optimálně i víc jak 20. U části pacientů lze jícen resekovat miniinvazivně (MIE), jedná se buď o čistě totálně miniinvazivní (laparoskopie + torakoskopie) či kombinovanované (hybridní) výkony, kdy část operace je provedena miniinvazivně (typicky abdominální fáze laparoskopicky) a část otevřeně (torakotomie). Nejnovějším trendem je robotická ezofagektomie (RAMIE), jejíž podíl celosvětově narůstá. Miniinvazivní výkony jsou ve srovnání s otevřenými operacemi spojeny s nižší perioperační morbiditou, kratší délkou hospitalizace, lepší krátkodobou a střednědobou kvalitou života, při stejné onkologické radikalitě a srovnatelném dlouhodobém přežívání pacientů. Za předpokladu dostupné expertízy jsou preferovaným operačním přístupem. RAMIE je ve srovnání s MIE spojena s delším operačním časem, ale preciznější lymfadenektomií, zejména v horním mediastinu. Chirurgická léčba karcinomu jícnu a EGJ má být centralizovaná do velkoobjemových pracovišť provádějících alespoň 20 ezofagektomií ročně.
Limitované onemocnění (cT1-T2cN0M0)
Doporučení pro endoskopickou léčbu premaligních a časných maligních lézí jícnu jsou zpracovány a dostupné na www.endoskopiste.cz/wp-content/uploads/2021/06/barrett-guidelines.pdf.
U pacientů s T1a adenokarcinomem je preferována endoskopická resekce. U pacientů s nádorem T1/T2N0 je primární léčba chirurgická, bez neoadjuvantní léčby. Není-li operace možná z důvodu komorbidit nebo nesouhlasu pacienta, je preferována kombinovaná chemoradioterapie, která má lepší výsledky než radioterapie samotná (u obou histologických typů). Význam perioperační nebo adjuvantní chemoterapie u pacientů s karcinomy T1b není prokázán, bez ohledu na postižení lymfatických uzlin. U pacientů s adenokarcinomem může být endoskopická resekce léčbou volby pro nádory v kategorii T1b, a to i přes zvýšené riziko recidivy.
V případě nádoru T2 je možné zvolit multimodální léčbu jako u lokálně pokročilého onemocnění. V této podskupině dosud nebyl prokázán významný přínos pro přežití a proto by doporučení multimodální léčby mělo být projednáno v multidisciplinárním týmu a výhody a nevýhody by měly být prodiskutovány s pacientem.
Lokálně pokročilé onemocnění (cT3-T4 nebo cN1-3 M0)
Neoadjuvantní léčba je indikována u operabilních pacientů.
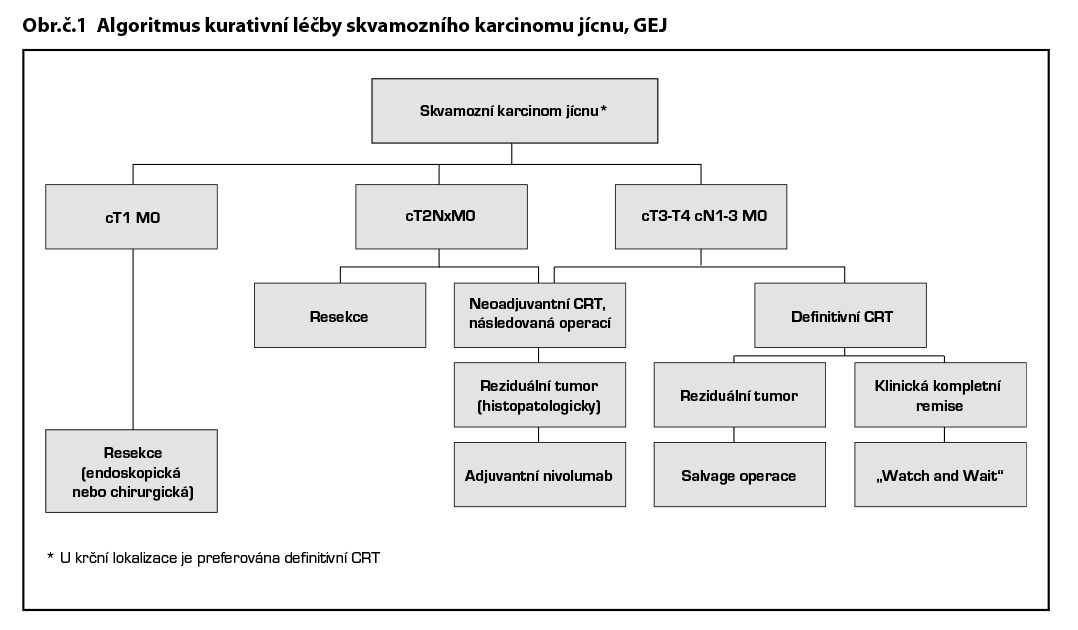
Skvamozní karcinom
Neoadjuvantní chemoradioterapie následovaná operací a adjuvantní imunoterapií nivolumab v případě reziduální choroby (hodnoceno jako T+ a N+) v resekátu je standardem léčby u skvamozního karcinomu jícnu.
Preferovaným chemoterapeutickým režimem je režim studie CROSS (paklitaxel/karboplatina podávaný 1× týdně s radioterapií o dávce 41,4 Gy aplikované ve 23 frakcích), následovaný operací a nivolumabem v případě nedosažené patologické kompletní remise (CheckMate 577); mOS pro skvamozní karcinom byl signifikantně delší v rameni s nivolumabem.
Definitivní kurativní chemoradioterapie se doporučuje v případě krční lokalizace nádoru a je volbou u pacientů bez možnosti chirurgické léčby (T4b, neresekabilní nádor, komorbidity, odmítnutí pacientem). Po definitivní chemoradioterapii je indikováno sledování. V případě perzistence tumoru či lokální progrese může následovat elektivní chirurgický výkon. Tradičním standardním režimem definitivní chemoradioterapie jsou čtyři série chemoterapie založené na fluorouracilu (kapecitabinu) a cisplatině v kombinaci s radioterapií o dávce 50,4 Gy v 28 frakcích (nebo 50 Gy ve 25 frakcích). Dávka radioterapie >50,4 Gy nepřinesla lepší lokální kontrolu ani delší přežití, navíc dávky nad >55 Gy zvyšovaly postoperační mortalitu a morbiditu v případě salvage ezofagektomie. Alternativním chemoterapeutickým režimem je 6× FOLFOX nebo režim studie CROSS (týdenní paklitaxel s karboplatinou ale 6×). Tento režim je lépe tolerován a akceptován jako standard i v rámci definitivní chemoradioterapie.
Dle studie SKYSCAPER-07 publikované abstraktem na ESMO 2025 prodloužila udržovací terapie atezolizumabem celkovou dobu do progrese onemocnění. Byl rovněž pozorován benefit v OS, medián v rameni s atezolizumabem* zatím nebyl dosažen.
Tyto výsledky byly statisticky signifikantní a podporují použití udržovací imunoterapie po definitivní CRT, i když se jednalo pouze o deskriptivní analýzu. V této indikaci není úhrada ze zdravotního pojištění schválena.
Ve výjimečných případech (komorbidity, věk, snaha o rychlou lokální kontrolu u křehkého pacienta) lze neoperativní režim definitivní chemoradioterapie zvážit i u adenokarcinomu.
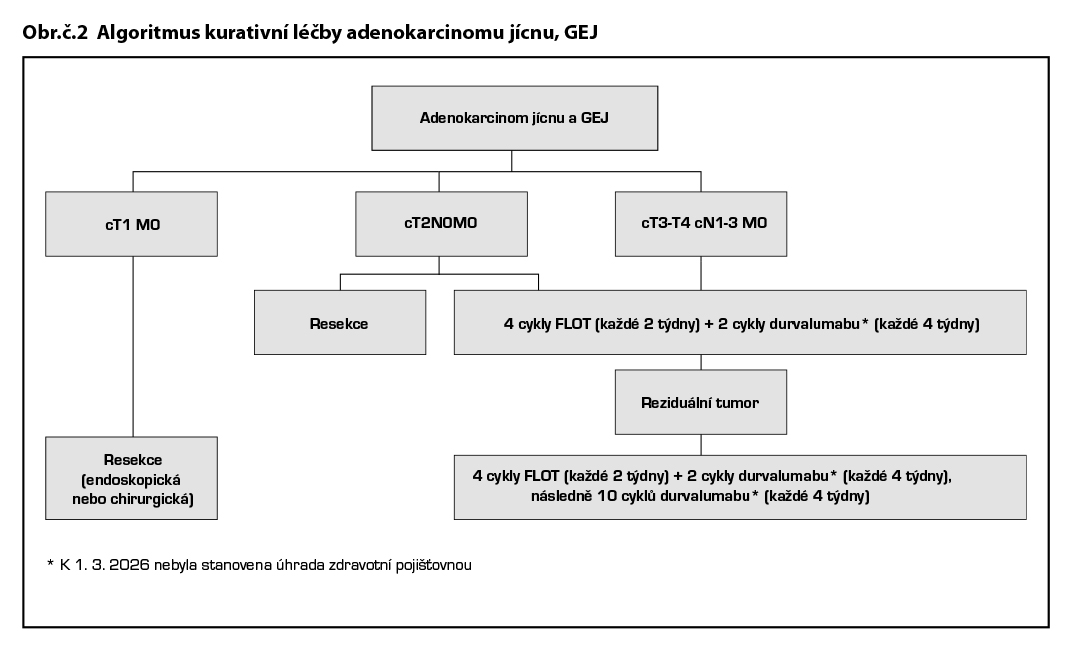
Adenokarcinom
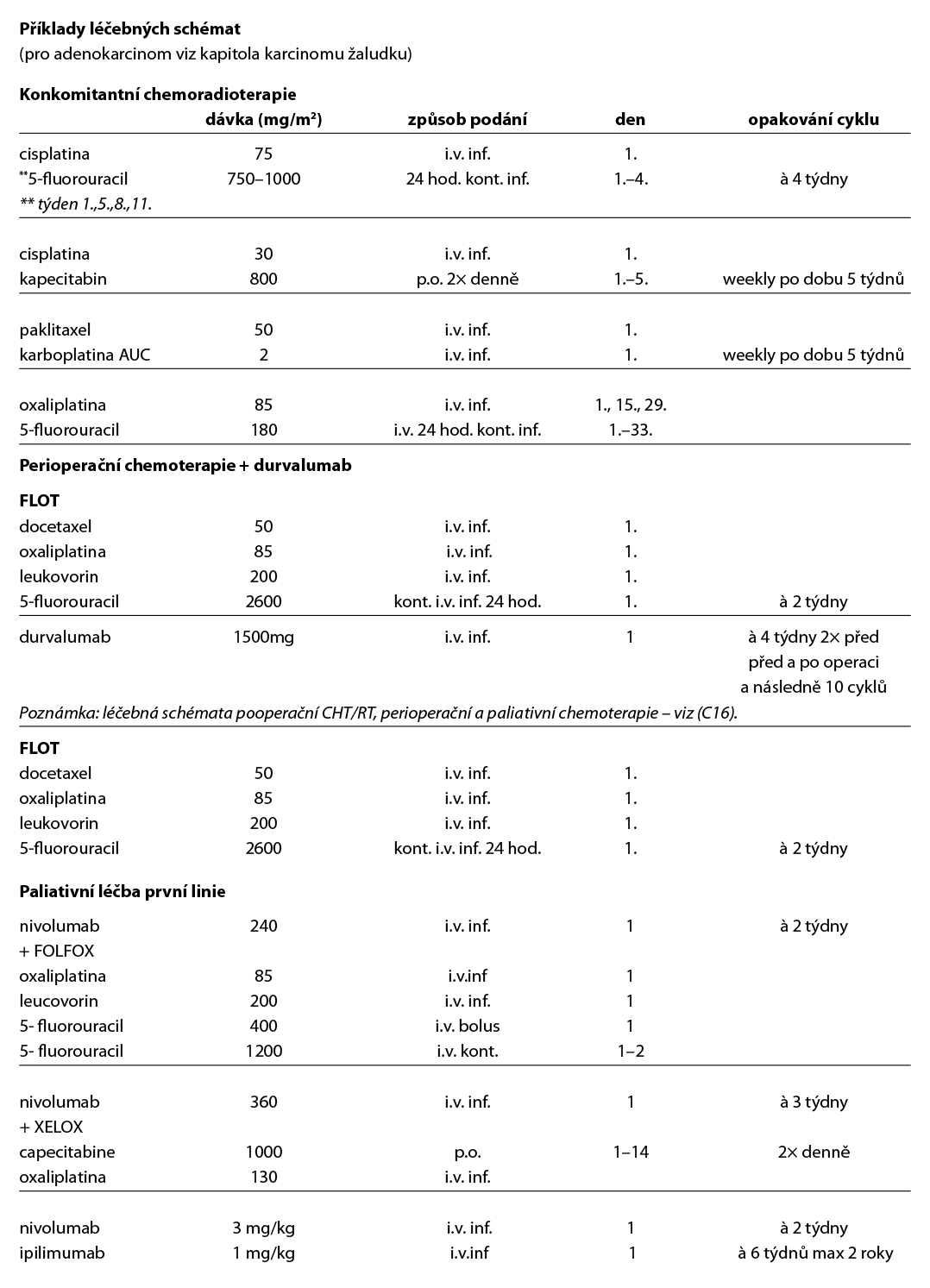
Pro adenokarcinomy jícnu a gastroezofageální junkce je indikována perioperační chemoterapie režimem FLOT (4 cykly před a 4 cykly po operaci).
Recentně bylo prokázáno, že FLOT v kombinaci s imunoterapií durvalumab* signifikantně prodloužuje EFS, OS a zlepšuje patologickou kompletní odpověď ve srovnání se samotnou chemoterapií (studie fáze III MATTERHORN) – nutné žádat schválení durvalumabu zdravotní pojišťovnou.
Role chemoradioterapie (CRT) v léčbě operabilního adenokarcinomu jícnu a GEJ
Data ze studie fáze III ESOPEC srovnávající perioperační FLOT s CRT (režim CROSS) u adenokarcinomu jícnu a GEJ favorizují jako léčebný standard perioperační chemoterapii. FLOT ve srovnání s CROSS zlepšuje 3leté OS a přežití bez progrese. Více lokoregionálních selhání bylo zaznamenáno v rameni s chemoterapií, naopak vzdálené recidivy se vyskytovaly u podstatně vyššího počtu pacientů ve skupině s předoperační CRT. Procento pacientů s R0 resekcí bylo téměř shodné v obou skupinách (přibližně 95 %). Výskyt pooperačních komplikací a úmrtnost po 90 dnech od operace byla v obou případech podobná.
Data z ESOPEC jsou podpořeny randomizovanou studií fáze III TOPGEAR , která ukázala, že přidání předoperační CRT k perioperační chemoterapii nezlepšilo OS u pacientů s resekabilními adenokarcinomy GEJ a žaludku.
Adjuvantní imunoterapie u lokálně pokročilého karcinomu jícnu a GEJ: ve studii CheckMate 577 prodloužila adjuvantní imunoterapie nivolumabem dobu do relapsu onemocnění pacientů (DFS) s karcinomem jícnu a GEJ, kteří byli léčeni neoadjuvantní konkomitantní chemoradioterapií s následnou operací a nedosáhli kompletní remise . Recentně byla na ASCO 2025 prezentována data o OS, přínos v případě adenokarcinomu byl patrný pouze u pacientů s PD-L1 CPS ≥ 1.
Adjuvantní léčba po absenci předoperační léčby
Pacienti s lokálně pokročilým karcinomem GEJ, kteří podstoupili resekci bez předchozí léčby (např. v případě podhodnoceného stagingu), mohou být léčeni adjuvantní terapií v případě vysokého rizika relapsu při rozsáhlém postižení lymfatických uzlin (pN2-3). V současné době není jasné, zda je vhodnější adjuvantní chemoterapie nebo chemoradioterapie. Podle údajů z asijské studie fáze III však kombinovaná chemoradioterapie (45 Gy + cisplatina/kapecitabin) nevede k (dalšímu) zlepšení přežití bez recidivy ve srovnání s kombinovanou chemoterapií samotnou (cisplatina/kapecitabin) (studie ARTIST2).
Po resekcích R1 se doporučuje adjuvantní chemoradioterapie z důvodu vysokého rizika lokální recidivy. Po neoadjuvantní chemoradioterapii a resekci R+ je ke zvážení adjuvantní podávání nivolumabu (ačkoli není zahrnuto v CheckMate 577).
Lokálně neoperovatelné adenokarcinomy jícnu/GEJ
U pacientů s adenokarcinomem jícnu, kteří jsou funkčně neoperovatelní nebo jejichž nádory jsou technicky neoperovatelné, se zdá, že definitivní chemoradioterapie dosahuje výsledků srovnatelných s výsledky u spinocelulárního karcinomu. Pro definitivní chemoradioterapii by měla být stanovena dávka radioterapie 50,4 Gy. Pro konkomitantní CRT jsou vhodné režimy s kombinací platiny a fluoropyrimidinu nebo karboplatiny a paklitaxelu.
Perioperační léčba u dMMR/MSI-H adenokarcinomů:
Dle retrospektivní metaanalýzy dat z pěti randomizovaných studií fáze III vedla perioperační chemoterapie založená na dvojkombinaci 5-fluorouracilu a platinovém derivátu u skupiny s MSI-H/MMR-D k horším výsledkům než samostatná chirurgie, a proto by tato skupina pacientů neměla být léčena perioperační dvojkombinací fluoropyrimidinu a platinového derivátu.
Prospektivní studie fáze II, a to francouzská NEONIPIGA (ipilimumab/nivolumab), a italská INFINITY (tremelimumab/ durvalumab), dokladovaly u pacientů s lokálně pokročilým primárně operabilním dMMR/MSI-H adenokarcinomem GEJ/ žaludku léčených samotnou neoadjuvantní imunoterapií dosažení patologické kompletní remise (pCR) až v 60 % případů (pT0N0). Podobně data ze studie fáze II DANTE ověřila přínos kombinace FLOT a atezolizumab. V současné době by v případech potvrzeného stavu MSI-high/dMMR měla být podávána perioperační imunoterapie – nejspíše durvalumabem v kombinaci s chemoterapií FLOT* – dle randomizované studie Matterhorn. Je otázkou, v jakých případech budou moci být pacienti léčeni pouze imunoterapií. Všichni pacienti s lokálně pokročilým adenokarcinomem by tedy měli být testováni na dMMR/MSI-H stav a v případě deficitu/instability konzultováni cestou multidisciplinárního týmu. V případě operabilního onemocnění může být zvážena primární chirurgická léčba. Je-li nutné docílit downstagingu, lze zvážit kombinaci FLOT s imunoterapií. Léčba checkpoint inhibitory v této indikaci však není hrazena a postup by měl být individuální.
Lokálně pokročilé neresekabilní či metastatické onemocnění
Systémová léčba
Výběr chemoterapeutického režimu v první linii závisí na celkovém stavu pacienta, komorbiditách, profilu nežádoucích účinků léčby. Systémová chemoterapie adenokarcinomu jícnu a GEJ je analogická léčbě adenokarcinomu žaludku. U skvamozního karcinomu je preferována kombinace na bázi fluorouracilu a platinového derivátu. Většina režimů u skvamozního karcinomu je přejata ze studií s adenokarcinomem, nicméně studie fáze II potvrdily standard kombinace cisplatiny a 5-FU. Infuzní fluorouracil a kapecitabin jsou volně zaměnitelné, stejně jako cisplatina a oxaliplatina. Starší a křehcí pacienti mohou být na základě dat ze studie fáze III GO2 léčeni režimem XELOX, případně FOLFOX, s redukcí dávky na 60 %. Tento režim prokázal stejnou účinnost s nižší toxicitou. Podobně, stejná studie prokázala benefit pro skupinu pacientů, u nichž byla zvažována pouze symptomatická terapie, OS byl nesignifikantně delší při použití chemoterapie versus BSC. Efektivita a dobrá tolerance irinotekanu byla prokázána ve francouzské studii f. III (French Intergroup Study). FOLFIRI je léčebnou alternativou k platinovému režimu v první linii metastatického onemocnění.
První linie léčby:
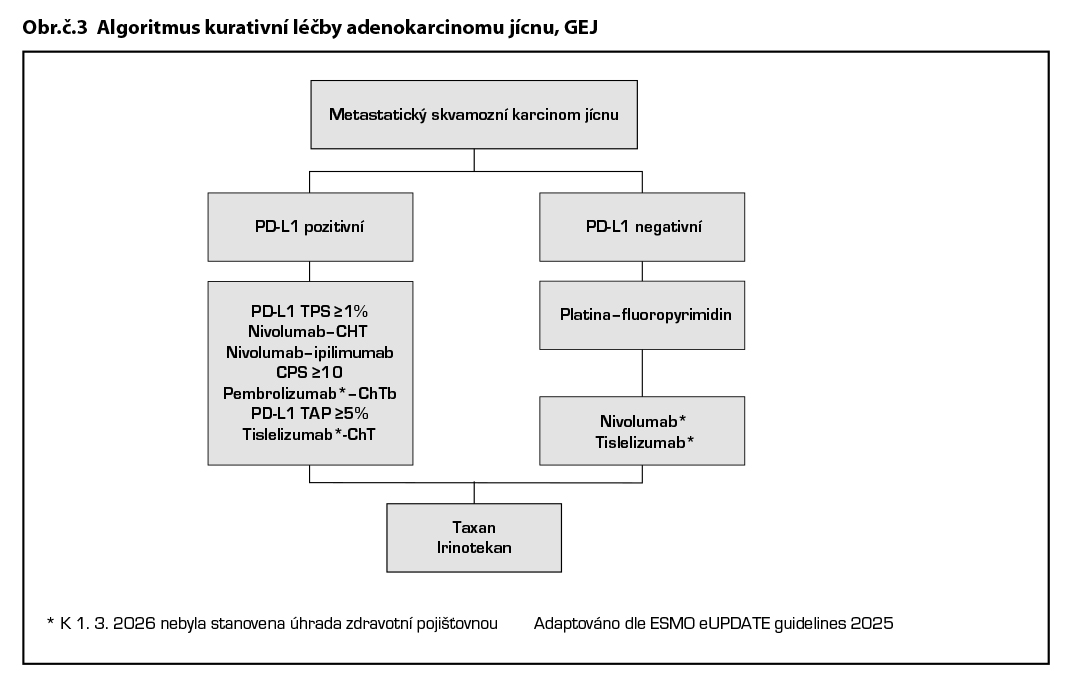
Skvamozní karcinom
Imunoterapie je v první linii účinná u obou histologických typů s lehce lepším efektem u skvamózního karcinomu. Studie fáze III CheckMate 648 randomizovala pacienty s lokálně pokročilým inoperabilním či metastatickým skvamozním karcinomem do ramene s nivolumabem, 5-fluorouracilem a cisplatinou nebo nivolumabem plus anti-CTLA-4 protilátkou ipilimumabem nebo chemoterapií samotnou. Pacienti léčeni nivolumabem, 5-fluorouracilem a cisplatinou měli prodloužený OS ve srovnání s chemoterapií samotnou, s maximem účinku ve skupině exprimující PD-L1 (hodnoceno dle TPS≥1%).
Nivolumab–ipilimumab také prodlužuje OS ve srovnání s chemoterapií (TPS≥1), avšak nikoliv dobu bez příznaků onemocnění (PFS), navíc bylo v rameni s kombinovanou imunoterapií zaznamenáno více časných úmrtí.
Na základě této studie je kombinace nivolumab s fluorouracilem a platinou či nivolumab/ipilimumab standardem první linie léčby u pacientů s TPS≥1 %. S ohledem na časná úmrtí v prvních měsících léčby samostatnou imunoterapií a nesignifikantní PFS je preferovaným režimem kombinace nivolumabu s chemoterapií.
Podobně pembrolizumab* a ostatní checkpoint inhibitory* (camrelizumab, tislelizumab, toripalimab, sintilimab etc.) mají data o účinnosti ze studií f. III. Tyto checkpoint inhibitory však nejsou v indikaci léčby první linie u skvamozního karcinomu v ČR hrazeny, tislelizumab a toripalimab mají registraci EMA.
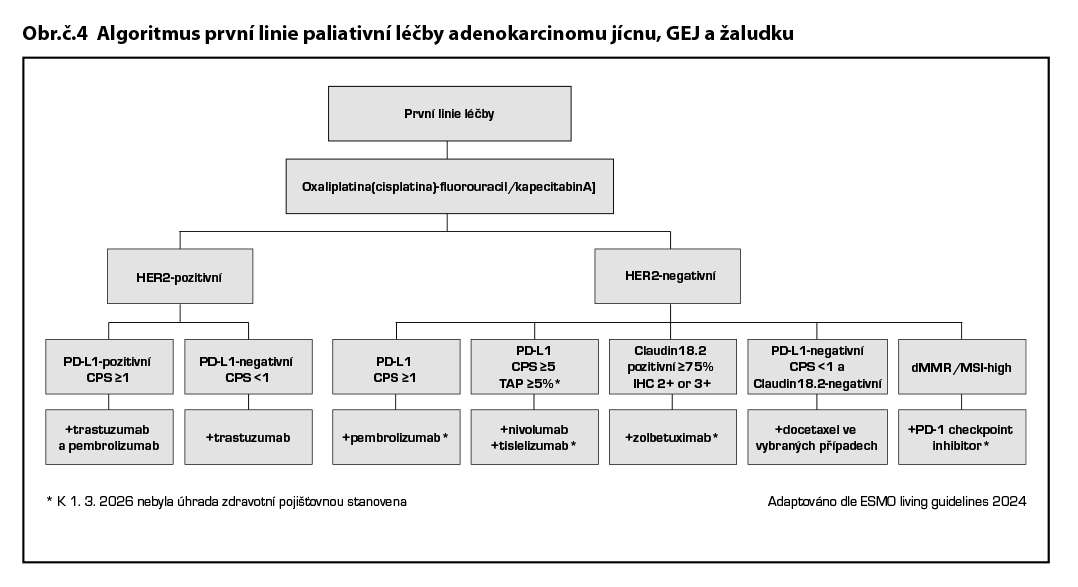
Adenokarcinom
Léčba HER2 negativního a PD-L1 CPS≥5 neresekabilního nebo metastatického adenokarcinomu GEJ a žaludku
V podmínkách ČR je v případě HER2 negativního onemocnění a PD-L1 exprese vyjádřené CPS≥5 indikována v první linii kombinace 5-fluorouracilu a platinového derivátu s nivolumabem (studie Checkmate 649).
Podobně pembrolizumab*, tislelizumab* a ostatní checkpoint inhibitory mají data o účinnosti ze studií f. III. Tyto checkpoint inhibitory však nejsou v indikaci léčby první linie v ČR hrazeny.
Léčba HER2 pozitivního neresekabilního nebo metastatického adenokarcinomu karcinomu GEJ a žaludku
Dle evropských standardů (EMA) je HER2 pozitivita u karcinomu GEJ/žaludku definována jako přítomnost exprese proteinu s imunohistochemickým (IHC) skóre 3+ nebo IHC 2+ a současná genová amplifikace v in situ hybridizaci (ISH) s poměrem HER2/CEP17 ≥2,0. Diagnostika HER2 by měla být zhodnocena s centrální/certifikované laboratoři).
Léčba HER2 pozitivního a PD-L1 CPS <1 neresekabilního nebo metastatického adenokarcinomu GEJ a žaludku
Trastuzumab by měl být přidán k chemoterapii na bázi 5-fluorouracilu a platinového derivátu (např. CAPOX, FOLFOX nebo FLO) u pacientů s HER2-pozitivním pokročilým karcinomem žaludku. Doporučení vychází z údajů studie fáze III ToGA, která prokázala vyšší míru léčebných odpovědí a prodloužené přežití u chemoterapie trastuzumabem, cisplatinou a fluoropyrimidinem ve srovnání s chemoterapií samotnou u pacientů splňujících výše uvedená výběrová kritéria. Kombinace trastuzumabu a oxaliplatiny plus fluoropyrimidinu vedou k výsledkům srovnatelným s historickým režimem ToGA obsahujícím cisplatinu.
Léčba HER2 pozitivního a PD-L1 CPS≥1 neresekabilního nebo metastatického adenokarcinomu GEJ a žaludku
Ve studii fáze III KEYNOTE-811 vedlo přidání pembrolizumabu k trastuzumabu a chemoterapii k zlepšení celkové odpo vědi na léčbu ORR, PFS a OS ve srovnání se samotným trastuzumabem-CHT. Pacienti s PD-L1 negativními nádory neměli z přidání pembrolizumabu žádný prospěch. Režim chemoterapie + trastuzumab a pembrolizumab je léčebným standardem u HER2 pozitivního PD-L1 CPS≥1 pozitivního neresekabilního nebo metastatického adenokarcinomu GEJ a žaludku.
Dle podmínek úhrady v ČR je chemoterapie s trastuzumabem s pembrolizumabem hrazena u IHC 3+ a PD-L1 CPS ≥ 1 pacientů s PS 0-1 do progrese nebo vyčerpání 35 cyklů.
Dle EMA a je stejná kombinace hrazena i u pacientů s IHC 2+/ISH amplifikací*(ISH; HER2/CEP17 poměr ≥2.0), v této indikaci je nutno o evropský standard žádat zdravotní pojišťovnu.
Léčba Claudin 18-2 pozitivního (CLDN 18.2 IHC 2+/3+ ≥ 75 % nádorových buněk) karcinomu GEJ a žaludku U pacientů s pokročilým neoperovatelným karcinomem žaludku/GEJ a expresí Claudin18.2 v ≥ 75 % nádorových buněk prodlužuje zolbetuximab* , chimérická monoklonální protilátka IgG1 cílená proti Claudin18.2, v kombinaci s chemoterapií FOLFOX prodlužuje OS (studie fáze III SPOTLIGHT). Výsledky studie SPOTLIGHT jsou do značné míry potvrzeny multinárodní studií fáze III GLOW a rovněž souhrnné údaje z obou studií prokázaly zlepšení PFS a OS. Hlavními vedlejšími účinky zolbetuximabu jsou nevolnost a zvracení, zejména během prvních několika aplikací (informace o managementu nauzey a zvracení v kapitole 29).
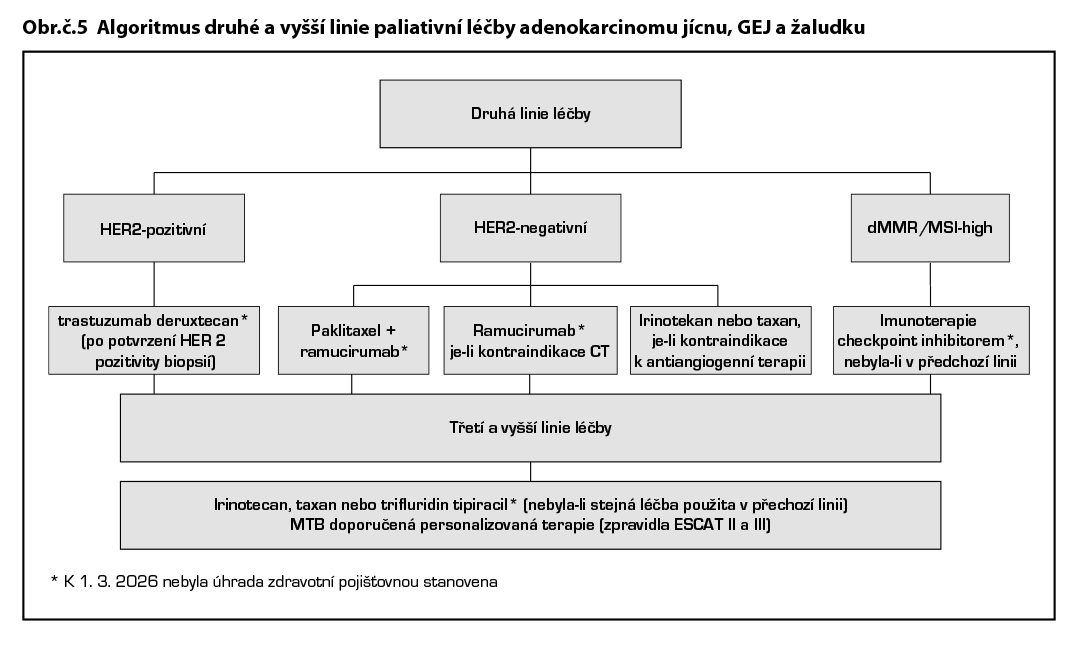
Druhá linie léčby
Skvamozní karcinom
U skvamozního karcinomu prokázal nivolumab* v druhé linii po předléčení fluoropyrimidinem a platinovým derivátem prodloužení celkového přežití a trvání léčebné odpovědi ve srovnání s paklitaxelem či docetaxelem. Podobně EMA schválila i použití tislelizumabu*. Z cytostatik je možno použít kombinaci FOLFIRI, nebyla-li použita v první linii, či monoterapii irinotekanem nebo taxanem.
Adenokarcinom
Chemoterapie dalších linií závisí na celkovém stavu pacienta a předchozí chemoterapii. Studie REGARD a RAINBOW zavedly standardní léčbu 2. linie – na základě těchto studií je ramucirumab* (CYRAMZA) od 12/2014 registrován EMA v této indikaci samostatně nebo v kombinaci s paklitaxelem*. Cytostatika s prokázanou aktivitou jsou taxany, irinotekan.
U HER2 pozitivních adenokarcinomů GEJ a žaludku je po progresi po předchozí léčbě režimem založeném na trastuzumabu indikován trastuzumab deruxtekan* (podrobněji viz adenokarcinom žaludku).
Třetí a vyšší linie
.Trifluridine/tipiracil* je cytostatická kombinace antimetabolitu trifluridinu a inhibitoru thymidinfosforylázy tipiracilu, jehož účinnost a bezpečnost byla zhodnocena studií III. fáze (TAGS) u pacientů s metastazujícím karcinomem žaludku (včetně adenokarcinomu gastroesofageální junkce), kteří byli dříve léčeni alespoň dvěma režimy systémové terapie pro pokročilé stádium onemocnění zahrnující chemoterapii založenou na fluoropyrimidinu, platině a buď taxanu nebo irinotekanu, spolu s odpovídající terapií anti HER2. Trifluridine/tipiracil vedl ke statisticky signifikantnímu zlepšení OS .
MSI-H/dMMR adenokarcinom GEJ a žaludku
Vzhledem k přesvědčivé účinnosti inhibitorů PD-1/PD-L1 by všem pacientům s MSI-HIGH/dMMR adenokarcinomy žaludku a GEJ měl být podáván jeden ze schválených checkpoint inhibitorů jako první linie léčby. Analýzy podskupin jsou pozitivní pro podávání inhibitoru imunitního kontrolního bodu v kombinaci s chemoterapií ve všech studiích relevantních pro schválení EMA (CheckMate 649, KEYNOTE-859) a také ve studiích, které nemohly být použity pro schválení (včetně KEYNOTE-062). Rovněž data z prospektivní studie Keynote 158 (pembrolizumab*) a ze studie NO LIMIT (ipilimumab/ nivolumab*) nebo GARNET (dostarlimab-gxly) potvrdila účinnost a možnost dosažení dlouhodobé remise při použití imunoterapie u metastatického onemocnění.
Pacienti, u nichž byla diagnostikována fúze NTRK genu, jsou kandidáty terapie NTRK inhibitory *entrektinibem a *larotrektinibem . Dále by měla být pacientům v dobrém výkonostním stavu ECOG PS 0,1 nabídnuta možnost NGS testování a konzultace Molekulárním tumour boardem, v případě targetabilní alterace je ke zvážení terapie cílenou léčbou zpravidla pro ESCAT I a II.
Prediktivní vyšetření
Pro skvamozní karcinom je podmínkou léčby první linií chemoterapie a nivolumabu, případně kombinací nivolumab/ ipilimumab hodnota TPS≥1%, pro léčbu *pembrolizumabem hodnota PD-L1 exprese vyjádřena CPS≥10.
U všech pacientů s adenokarcinomem GEJ a žaludku je doporučeno vyšetřit HER2 a MSI-H/MMR-D před stanovením strategie léčby, v (neo)adjuvantním záměru před zahájením chemoterapie.
Ve IV. klinickém stadiu je doporučeno před zahájením 1. linie systémové léčby vyšetřit i PD-L1 expresi a expresi Claudin 18. 2
Hodnocení PD-L1 exprese se liší dle histologického typu a použitého checkpoint inhibitoru. U adenokarcinomu je indikací k léčbě nivolumabem CPS≥5. Indikací k léčbě zolbetuximabem je hodnota Claudinu 18.2: střední či vysoká exprese v více než 75% nádorových buněk (CLDN 18.2 IHC 2+/3+ ≥ 75 % nádorových buněk)
V individuálních případech lze u pacientů ve IV. klinickém stadiu vyšetřit fúze NTRK (možnost terapie larotrektinibem a entrektinibem) a u pacientů v dobrém stavu při vyčerpání možností standartní léčby testování NGS a vyšetření TMB. Dále je doporučováno vyšetření DPYD k predikci toxicity chemoterapie fluoropyrimidiny.
*O úhradě přípravku ze zdravotního pojištění nebylo v této indikaci k 1. 3. 2026 rozhodnuto.
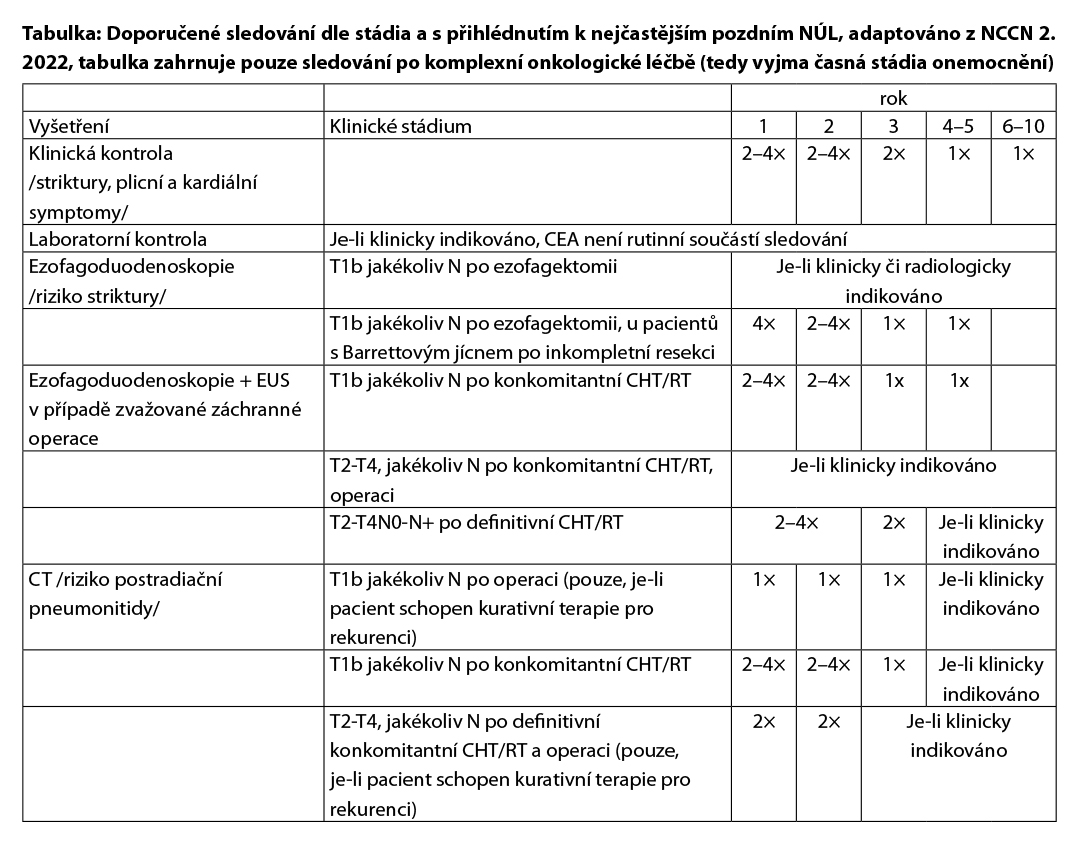
Karcinom jícnu – follow up po kurativní léčbě
Všichni pacienti by měli být sledováni systematicky, nicméně konsensus pro standardní follow-up neexistuje. Naše doporučení vychází z evropských (ESMO) a amerických (NCCN) guidelines.
PET/CT a ezofagoduodenoskopie může být součástí follow-up, je-li klinické podezření na recidivu/relaps onemocnění.
U všech pacientů doporučujeme zvážit nutnost nutriční podpory.
Literatura:
- Guo H-M, Zhang X-Q, Chen M, Huang S-L, Zou X-P. Endoscopic submucosal dissection vs endoscopic mucosal resection for superficial esophageal cancer. World J Gastroenterol 2014;20:5540-5547. DOI: 10.3748/wjg.v20.i18.5540
- Thuss-Patience P, Vecchione L, Keilholz U. Should cT2 esophageal cancer get neoadjuvant treatment before surgery? J Thorac Dis 2017;9:2819-2823. DOI: 10.21037/jtd.2017.08.143
- Al-Batran S, Homann N, Pauligk C et al. Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4): a randomized, phase 2/3 trial. Lancet 2019;393:1948-1957. DOI: 10.1016/S0140-6736(18)32557-1
- van Hagen P, Hulshof MCCM, van Lanschot JJB et al. Preoperative chemoradiotherapy for esophageal or junctional cancer. N Engl J Med 2012;366:2074-2084. DOI: 10.1056/NEJMoa1112088
- Eyck B, van Lanschot J, Maarten M et al. Ten-year outcome of neoadjuvant chemoradiotherapy plus surgery for esophageal cancer: the randomized controlled CROSS trial. J Clin Oncol 2021;39:1995-2004. DOI: 10.1200/JCO.20.03614
- Kelly RJ, Ajani JA, Kuzdzal J et al. Adjuvant nivolumab in resected esophageal or gastroesophageal junction cancer. N Engl J Med 2021;384:1191-1203. DOI: 10.1056/NEJMoa2032125
- Conroy T, Galais MP, Raoul JL et al. Definitive chemoradiotherapy with FOLFOX versus fluorouracil and cisplatin in patients with esophageal cancer (PRODIGE5/ACCORD17): final results of a randomized, phase 2/3 trial. Lancet Oncol 2014;15:305-314. DOI: 10.1016/S1470-2045(14)70028-2
- Doki Y, Ajani J, Kato K et al. Nivolumab combination therapy in advanced esophageal squamous-cell cancer. N Engl J Med 2022;368:449-462. DOI:10.1056/ NEJMoa2111380
- Janjigian Y, Shitara K, Moehler M et al. First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649): a randomised, open-label, phase 3 trial. Lancet 2021;398:27-40. DOI: 10.1016/S0140-6736(21)00797-2
- Hall PS, Swinson D, Cairns DA et al. Efficacy of reduced-intensity chemotherapy with oxaliplatin and capecitabine on quality of life and cancer control among older and frail patients with advanced gastroesophageal cancer. The GO2 phase 3 randomized clinical trial. JAMA Oncol 2021;7:869-877. DOI:10.1001/ jamaoncol.2021.0848
- Shitara K, Doi T, Dvorkin M et al. Trifluridine/Tipiracil versus placebo in heavily pretreated gastric cancer (TAGS): a randomized, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol 2018;19:1437-1448. DOI: 10.1016/S1470-2045(18)30739-3
- Shitara K, Bang YJ, Iwasa S et al. Trastuzumab deruxtecan in previously treated HER2-positive gastric cancer. N Engl J Med 2020;382:2419-2430. DOI:10.1056/ NEJMoa2004413
- Shitara K, Shah MA, Lordick F et al. Zolbetuximab in gastric or gastroesophageal junction adenocarcinoma. N Engl J Med 2024;391:1159-1162. DOI:10.1056/ NEJMc2409512
- Wilke H, Muro K, Van Cutsem E et al. Ramucirumab plus paclitaxel versus placebo plus paclitaxel in patients with previously treated advanced gastric or gastro-oesophageal junction adenocarcinoma (RAINBOW): a double-blind, randomized phase 3 trial. Lancet Oncol 2014;15:1224-1235. DOI:10.1016/ S1470-2045(14)70420-6
- Fuchs CS, Tomasek J, Yong CJ et al. Ramucirumab monotherapy for previously treated advanced gastric or gastro-oesophageal junction adenocarcinoma (REGARD): an international, randomized, multicenter, placebo-controlled, phase 3 trial. Lancet 2014;383:31-39. DOI: 10.1016/S0140-6736(13)61719-5
- Marabelle A, Fakih M, Lopez J et al. Association of tumor mutational burden with outcomes in patients with advanced solid tumors treated with pembrolizumab: prospective biomarker analysis of the multicohort, open-label, phase 2 KEYNOTE-158 study. Lancet Oncol 2020;21:1353-1365. DOI:10.1016/ S1470-2045(20)30445-9
- Hoeppner J, Brunner T, Schmoor C et al. Perioperative chemotherapy or preoperative chemoradiotherapy in esophageal cancer. N Engl J Med 2025;392:323335. doi: 10.1056/NEJMoa2409408.
- Shitara K, Lordick F, Bang YJ et al. Zolbetuximab plus mFOLFOX6 in patients with CLDN18.2-positive, HER2-negative, untreated, locally advanced unresectable or metastatic gastric or gastro-oesophageal junction adenocarcinoma (SPOTLIGHT): a multicenter, randomized, double-blind, phase 3 trial. Lancet 2023;401:1655-1668. DOI: 10.1016/S0140-6736(23)00620-7
- André T, Tougeron D, Piessen G et al. Neoadjuvant nivolumab plus ipilimumab and adjuvant nivolumab in localized deficient mismatch repair/microsatellite instability-high gastric or esophagogastric junction adenocarcinoma: the GERCOR NEONIPIGA phase II study. J Clin Oncol 2023;41:255-265. DOI:10.1200/ JCO.22.00686
- Janjigian YY, Al-Batran SE, Wainberg ZA et al; MATTERHORN Investigators. Perioperative durvalumab in gastric and gastroesophageal junction cancer. N Engl J Med 2025;393:217-230. DOI: 10.1056/NEJMoa2503701
- Hoeppner J, Schmoor C, Brunner T et al. Recurrence patterns of esophageal adenocarcinoma in the phase III ESOPEC Trial comparing perioperative chemotherapy with preoperative chemoradiotherapy. J Clin Oncol 2025 Jul 9:JCO2500948. doi: 10.1200/JCO-25-00948.
- Hall PS, Swinson D, Cairns DA et al. Efficacy of reduced-intensity chemotherapy with oxaliplatin and capecitabine on quality of life and cancer control among older and frail patients with advanced gastroesophageal cancer: the GO2 phase 3 randomized clinical trial. JAMA Oncol 2021;7:869-877. DOI:10.1001/ jamaoncol.2021.0848
- Kelly R, Ajani J, Kuzdzal J et al. Adjuvant nivolumab in resected esophageal or gastroesophageal junction cancer (EC/GEJC) following neoadjuvant chemoradiotherapy (CRT): First results of overall survival (OS) from CheckMate
- J Clin Oncol 2025;43(16suppl). DOI: 10.1200/JCO.2025.43.16_suppl.4000
- Shitara K, Van Cutsem E, Gümüş M et al; DESTINY-Gastric04 Trial Investigators. Trastuzumab deruxtecan or ramucirumab plus paclitaxel in gastric cancer. N Engl J Med 2025;393:336-348. DOI: 10.1056/NEJMoa2503119
- Tabernero J, Shitara K, Zaanan A et al. Trifluridine/tipiracil versus placebo for third or later lines of treatment in metastatic gastric cancer: an exploratory subgroup analysis from the TAGS study. ESMO Open 2021;6:100200. DOI: 10.1016/j.esmoop.2021.100200
- Obermannova R et al. ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Annals of Oncology 2022, S0923-7534(22)01850-6.
