24.1 Indikační kritéria pro prezentaci pacienta na multidisciplinárním týmu a molekulární prediktivní vyšetření u nádorů CNS
U každého pacienta s primárním nádorem mozku bychom měli zvážit možnosti multioborového přístupu. Níže jsou uvedena indikační kritéria pro prezentaci pacienta na multidisciplinárním týmu:
- všichni pacienti v době diagnózy a/nebo po operaci
- všichni pacienti v době recidivy nádoru
Molekulární diagnostické a prediktivní vyšetření u primárních nádorů CNS
Standardem v diagnosticky relevantních případech by dnes mělo být vyšetřování molekulárních markerů – kodelece 1p/19q, mutace IDH, mutace ATRX, metylace promotoru genu pro MGMT a homozygotní delece CDKN2A/B, která je molekulárním markerem pro astrocytom WHO grade 4 IDH.
U středočarových WHO G4 gliomů vyšetřovat expresi H3 K27me3 a v případě průkazné ztráty exprese H3 K27me3 je nutné došetření genetických alterací definující difúzní středočarový gliom H3 K27-alterovaný (mutace H3-K27M, mutace nebo amplifikace EGFR anebo zvýšená exprese EZHIP). U intrakraniálního supratentoriálního ependymomu (G1-3) vyšetřovat ZFTA a YAP1 fúzní gen, definující samostatné jednotky supratentoriálního ependymomu a v případě ZFTA-fúze pozitivního supratentoriálního ependymomu i vyšetření CDKN2A/B (prognostický faktor).
Mutaci genu BRAF V600 je doporučeno vyšetřovat u pilocytického astrocytomu, pleomorfního xantoastrocytomu, gangliogliomu (prediktivní marker pro léčbu BRAF a MEK inhibitory). Individuálně zvažovat vyšetření NTRK fúze (prediktivní marker pro NTRK inhibitory). V indikovaných případech cestou multidisciplinárního týmu je možno doporučit NGS testování.
Prediktivní vyšetření pro systémovou léčbu u mozkových metastáz je určeno primárním nádorem a je uvedeno v jednotlivých kapitolách.
24.2 Chirurgická léčba
Základním léčebným přístupem u většiny mozkových nádorů je neurochirurgický zákrok. Cílem je provést maximální bezpečnou resekci bez poškození funkčně důležitých oblastí mozku a získání nádorové tkáně pro histologické a molekulárně genetické vyšetření. Rozsah resekce a velikost reziduálního nádorového objemu je považován za významný prognostický faktor, který ovlivňuje celkové přežití u gliomů všech typů a stupňů. Spíše než procentuální rozsah resekce je důležitý absolutní objem nádorového rezidua. Rozsah resekce by měl být posouzen dle RANO resect kriterií během 24–48 hodin po operaci pomocí MR. Inoperabilní mozkový nádor je nutno alespoň histologicky verifikovat, minimálně stereotaktickou biopsií. K dosažení co největší radikality výkonu může být využito intraoperačních zobrazovacích metod jako UZ, intraoperační MR, operace po aplikaci kyseliny 5-aminolevulinové (5-ALA), nebo jejich kombinace. Pokud chirurgický výkon nemá kurativní potenciál a musí následovat brzká pooperační léčba (např. u gliomů), nemělo by při snaze o maximální resekci dojít k významnému poškození neurologických funkcí, zvýšení rizika dalších komplikací, snížení kvality života. Prevence nových trvalých neurologických deficitů je tak důležitější než rozsah resekce. Pooperační stav může zásadně ovlivnit další léčebné možnosti, a tím i celkový osud pacienta. K minimalizaci rizika neurologického deficitu po operaci slouží předoperační plánování (funkční MR a traktografie), intraoperační zobrazení tumoru a intraoperační elektrofyziologické mapování elokventních oblastí. Pokud je nutno při operaci monitorovat řeč, tak se výkon provádí v bdělém stavu (tzv. awake kraniotomie).
Role neurochirurga je důležitá také při řešení recidiv primárních mozkových nádorů. Indikace reoperace je vždy posuzována individuálně z pohledu možného benefitu a rizika.
Následující část bude věnována především gliomům, nejčastějším primárním nádorům CNS v dospělém věku.
24.3 Low-grade gliomy (oligodendrogliom G2, astrocytom G2, low-grade gliomy pediatrického typu)
24.3.1 Adjuvantní léčba
Pro indikaci pooperační léčby je vhodné kromě radikality výkonu zhodnocení dalších rizikových faktorů (věk > 40 let, KPS < 70 %, nádor > 6 cm, přechod přes střední čáru a neurologický deficit před operací). Přítomnost 0–2 faktorů řadí pacienta do skupiny nízkého rizika (low-risk), 3 a více faktorů do skupiny vysokého rizika (high-risk). Toto historické dělení na low-risk a high-risk skupinu podle prognostických faktorů bude nutno brát v budoucnu jen velmi orientačně. S příchodem cílené léčby (IDH inhibitor - vorasidenib) se nově vyčlení medium-risk skupina pacientů.
Éra zavedení molekulárních charakteristik postupně vede k přehodnocování rizikových faktorů u IDH mutovaných gliomů, které často vycházejí ze starších studií. Novější důkazy například zpochybňují tradičně uváděnou věkovou hranici 40 let. Přitom se jedná o obecnou vlastnost interpretace studií LGG, kdy jsou výsledky často k dispozici po víc jak 10 letech od zahájení studie. Diskutabilní je posouzení reziduálního onemocnění po operaci v kontextu prostředí mikroskopického infiltrativního onemocnění přítomného nad rámec zobrazovacích abnormalit prakticky u všech pacientů s gliomy. Z tradičních rizikových faktorů pak zůstává nejrelevantnější objem a rychlost růstu nádoru/rezidua a přítomnost neurologických symptomů.
U low-risk pacientů po makroskopicky totální resekci tumoru, případně mladých (< 40 let) s drobným pooperačním reziduem, kteří jsou asymptomatiční a pacientů s WHO G1 difúzním gliomem pediatrického typu (polymorfní low-grade neuroepiteliální tumor mladých, angiocentrický gliom, difúzní astrocytom, MYB-, MYBL-alterovaný a difúzní low-grade gliom s alterací MAPK kaskády) lze doporučit samotné sledování (watch and wait strategie).
Pro medium-risk pacienty bude zvažována léčba IDH 1/2 inhibitorem vorasidenibem na základě výsledků randomizované klinické studie fáze 3 INDIGO (NCT04164901) a v souladu se schválenou indikací přípravku.
Vorasidenib je indikován jako monoterapie k léčbě převážně postkontrastně se nesytícího (non-enhancing) astrocytomu nebo oligodendrogliomu 2. stupně s mutací IDH1 R132 nebo IDH2 R172 u dospělých a dospívajících pacientů ve věku ≥12 let a s tělesnou hmotností ≥40 kg, kteří podstoupili pouze chirurgický zákrok (včetně biopsie, subtotální nebo totální resekce) a bezprostředně nevyžadují radioterapii ani chemoterapii.
Do studie INDIGO byli zařazeni pacienti s měřitelným, převážně nesytícím onemocněním na MRI. Pacienti s minimálním, nenodulárním a neměřitelným sycením mohli být zařazeni za předpokladu stability nálezu na kontrolním MRI. Pacienti byli léčeni vorasidenibem v dávce 40 mg perorálně jednou denně nebo placebem až do radiografické progrese onemocnění nebo nepřijatelné toxicity. Primárním cílovým ukazatelem bylo přežití bez radiografické progrese (PFS) podle kritérií RANO pro low-grade gliomy. Aktualizovaná analýza potvrdila signifikantní prodloužení PFS při léčbě vorasidenibem (HR 0,35; 95% CI 0,25–0,49). Po 24 měsících činila míra PFS 59 % v rameni s vorasidenibem oproti 26 % u placeba. Medián PFS nebyl v rameni s vorasidenibem dosažen, zatímco u placeba činil 11,4 měsíce. Součástí klinického přínosu bylo rovněž oddálení nutnosti zahájení další onkologické léčby (radioterapie nebo chemoterapie) a lepší kontrola nádorem asociované epilepsie.
Vzhledem k dosud omezeným zkušenostem s touto cílenou terapií nelze v současnosti jednoznačně definovat relativní význam jednotlivých prognostických faktorů pro výběr nemocných do medium-risk skupiny. Indikace pooperační léčby vorasidenibem by proto měla být vždy stanovena v rámci multidisciplinárního týmu.
K 1. 3. 2026 nemá vorasidenib stanovenu úhradu ze systému veřejného zdravotního pojištění a je nutno postupovat cestou žádosti o individuální schválení léčby (RL).
U high-risk dospělých pacientů je na základě výsledků studie 3. fáze RTOG 9802 doporučena pooperační radioterapie s následnou chemoterapií (6× PCV). Pokud není možno nebo není vhodné podat režim PCV (vysoké riziko toxicity, nedostupnost cytostatik), lze jako alternativu použít temozolomid. U high-risk pacientů nevhodných nebo odmítajících chemoterapii volíme jen radioterapii. Samotná chemoterapie (temozolomid) je možnou variantou pro situace, kdy radioterapie není vhodná (např. objemný nádor, odmítnutí pacientem). Její výsledky jsou ale z pohledu dlouhodobé kontroly onemocnění pravděpodobně horší než u radioterapie.
Pooperační možnosti léčby low-grade gliomů (LGG)
- sledování (low-risk) (2A)*,
- vorasidenib (medium-risk) (2A)
- adjuvantní radioterapie + chemoterapie (6× PCV, high-risk) (1),
- konkomitantní chemoradioterapie + adjuvantní chemoterapie s temozolomidem (2A) u high-risk oligodendrogliomů
- adjuvantní radioterapie + chemoterapie (temozolomid, high-risk) (2A),
- adjuvantní radioterapie (high-risk) (2A),
- adjuvantní chemoterapie (temozolomid, high-risk) (2B).
*Sledování jen u pacienta po sub/totální resekci, < 40 let, neurologicky stabilního nebo asymptomatického a u pacientů s WHO G1 difúzním gliomem pediatrického typu. Difúzní gliomy pediatrického typu jsou všechny IDH-wildtype a dělí se na low-grade a high-grade gliomy. Low-grade difúzní gliomy pediatrického typu mají lepší prognózu než IDH-mutované gliomy adultní.
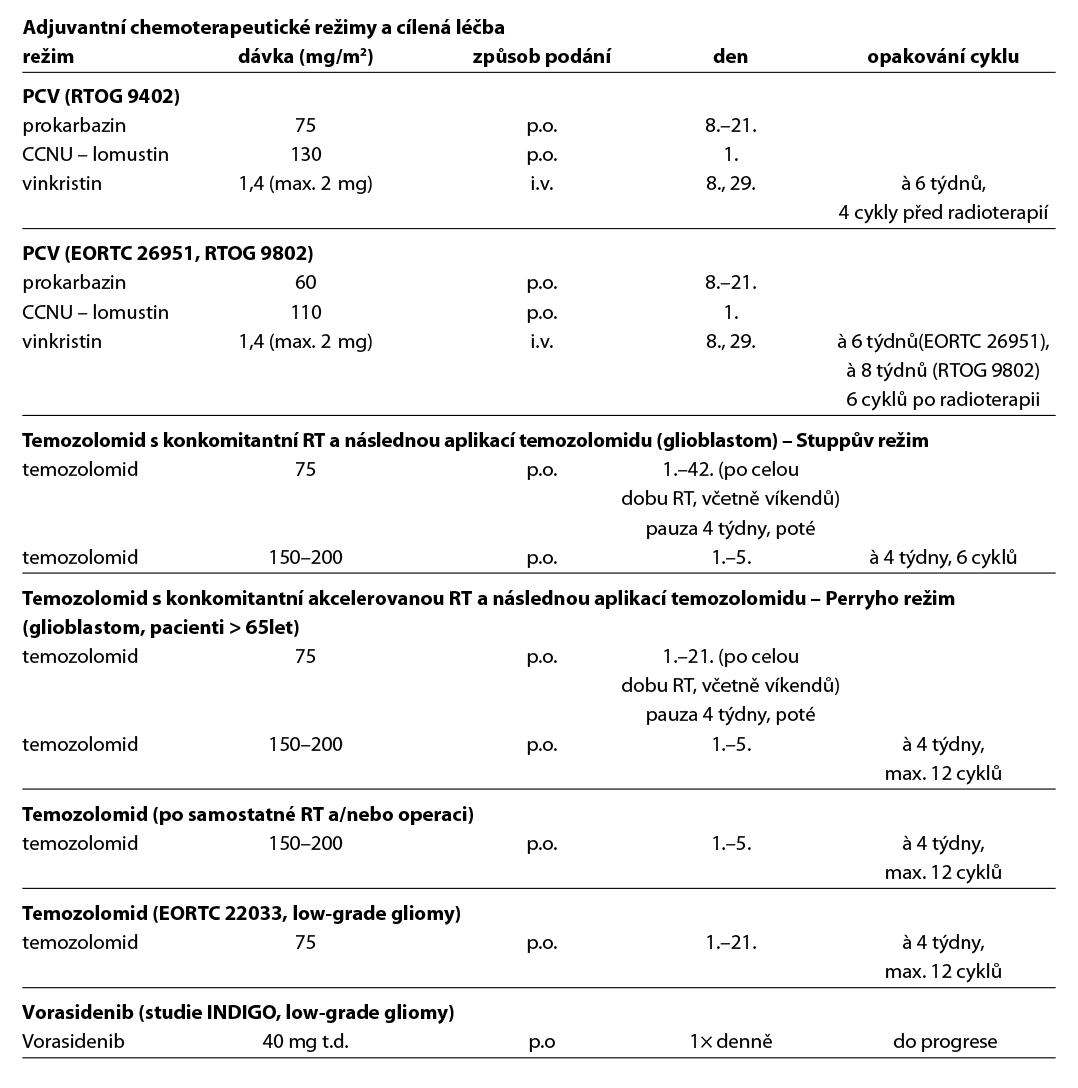
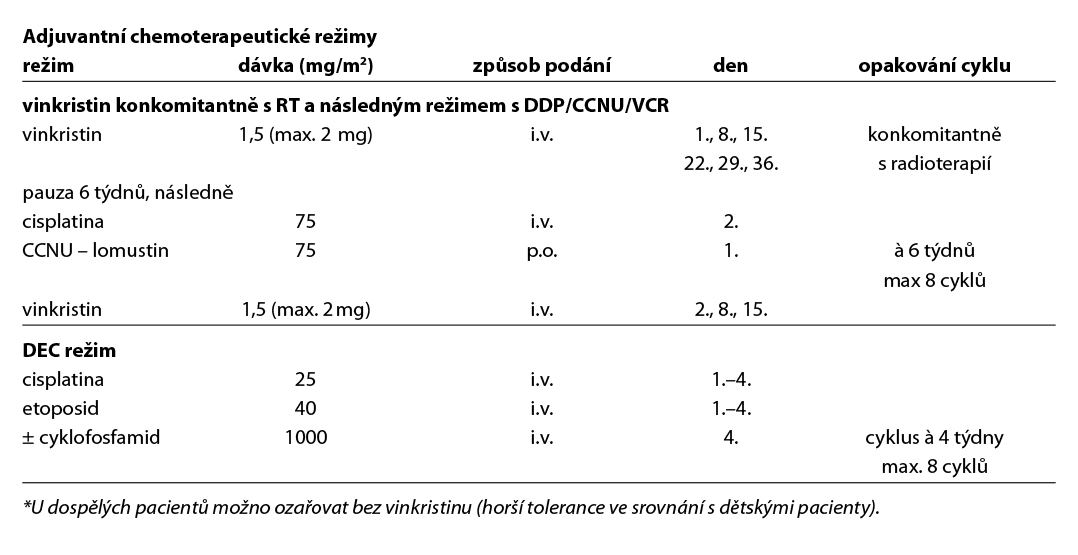
Režimy pro adjuvantní chemoterapii
- PCV (prokarbazin, CCNU, vinkristin),
- temozolomid v monoterapii.
Pozn.: Indikace adjuvantní radioterapie je specifikována v Národních radiologických standardech – radiační onkologie, Věstník MZ ČR, částka 2, 26. 1. 2016 (www.srobf.cz).
24.3.2 Léčba recidivy/progrese
Vyčerpat možnosti chirurgie a radioterapie.
Paliativní chemoterapii zvažovat u symptomatických onemocnění nebo při známkách progrese v high-grade gliom.
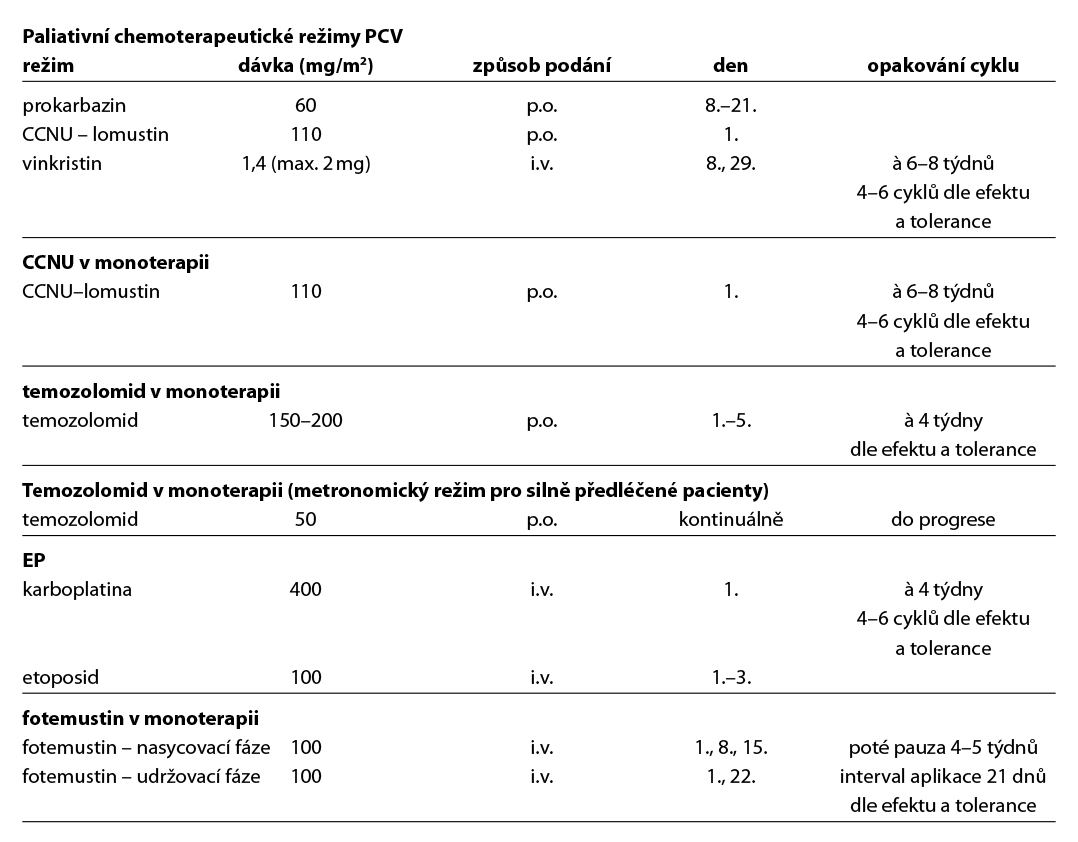
Režimy pro paliativní chemoterapii
- PCV (prokarbazin, CCNU, vinkristin), nebo nitrosourea v monoterapii,
- temozolomid v monoterapii,
- ostatní režimy paliativní chemoterapie (viz níže).
24.4 High-grade gliomy (oligodendrogliom G3, astrocytom G3 a G4, glioblastom)
24.4.1 Adjuvantní léčba
24.4.1.1 Oligodendrogliom IDH mutovaný s kodelecí 1p/19q, WHO G3
- radioterapie + (neo)adjuvantní chemoterapie s PCV (1),
- konkomitantní chemoradioterapie a adjuvantní chemoterapie s temozolomidem (2A),
- radioterapie (KI < 60%) (2A).
Režim PCV (prokarbazin, CCNU, vinkristin) – možno zvážit 4× před nebo 6× po radioterapii u oligodendrogliomů G3. Dle randomizovaných klinických studií RTOG 9402 a EORTC 26951 byl u této skupiny pacientů potvrzen signifikantní vliv (neo)adjuvantní chemoterapie na prodloužení celkového přežití ve srovnání se samotnou radioterapií. Zda je lepší konkomitantní chemoradioterapie a adjuvantní chemoterapie s temozolomidem vs. radioterapie následovaná režimem PCV řeší studie CODEL. Režim s adjuvantním temozolomidem (s/bez konkomitantního podání s radioterapií) je dnes akceptovanou variantou pro pacienty nevhodné pro režim PCV nebo při jeho nedostupnosti. Samotná radioterapie je vhodná jen u pacientů neschopných následné chemoterapie (KI < 60 %).
24.4.1.2 Astrocytom IDH mutovaný, WHO G3/4 (non-kodelece 1p/19q)
- radioterapie + adjuvantní temozolomid (12×) (1)*,
- konkomitantní chemoradioterapie a adjuvantní chemoterapie s temozolomidem (2A)**,
- radioterapie (KI < 60 %) (2A),
- chemoterapie temozolomid při metylaci MGMT (KI < 60 %) (2B).
*Dle finálních výsledků studie 3. fáze CATNON bylo potvrzeno prodloužení celkového přežití v rameni s adjuvantní chemoterapií (12 cyklů TMZ) po provedené radioterapii u anaplastických astrocytomů WHO G3. Vliv konkomitantní chemoterapie s temozolomidem v průběhu radioterapie na celkové přežití nebyl potvrzen.
**Indikaci Stuppova režimu zvážit u astrocytomu G4 (dříve označovaný jako sekundární glioblastom).
24.4.1.3 Glioblastom IDH wildtype, WHO G4
- konkomitantní chemoradioterapie a adjuvantní chemoterapie s temozolomidem (Stuppův režim) (1),
- konkomitantní chemoradioterapie a adjuvantní chemoterapie s temozolomidem (Stuppův režim) + TTF* (1),
- akcerlerovaná radioterapie s konkomitantním a adjuvantním temozolomidem u pacientů > 65 let (Perryho režim) (1), indikace při předpokladu obtížného zvládání dlouhého šestitýdenního Stuppova režimu,
- akcelerovaná radioterapie (preference u pacientů > 70 let bez průkazu metylace MGMT nebo u pacientů s KI < 60 %) (2A),
- chemoterapie s temozolomidem při metylaci MGMT (možnost u pacientů > 70 let) nebo pacientů s KI < 60 %) (2A).
Stav metylace promotoru MGMT by měl být stanoven u všech glioblastomů jako prognostický a prediktivní faktor, pacienti starší (> 70 let) nebo křehčí by pak měli být léčeni temozolomidem na základě stavu metylace.
*Léčbu s TTF (Tumor Treating Fields - systém Optune) v kombinaci s adjuvantní chemoterapií s temozolomidem lze zvážit u dospělých pacientů s nově diagnostikovaným supratentoriálním glioblastomem, kteří jsou po provedené konkomitantní chemoradioterapii bez známek progrese nebo recidivy nádoru. Léčba v ČR je možná ve vybraných onkologických centrech (Nemocnice Na Homolce, ÚVN Praha, Masarykův onkologický ústav Brno, FN Olomouc) a její úhrada musí být schválena revizním lékařem pojišťovny.
24.4.1.4 High-grade gliomy pediatrického typu (Difúzní středočarový gliom, H3 K27M-alterovaný, Difúzní hemisférický gliom, H3 G34-mutovaný, Difúzní high-grade gliom pediatrického typu, H3-wildtype, IDH-wildtype, Hemisferický gliom infantilního typu)
Léčebný postup u výše uvedených jednotek odpovídá léčbě glioblastomu. Vždy je vhodná konzultace s dětskými onkology.
24.4.2 Léčba recidivy/progrese
Vyčerpat možnosti chirurgie a radioterapie. Individuálně po resekci recidivy glioblastomu, v závislosti na předchozím ozáření, opětovně zvážit pooperační konkomitantní chemoradioterapii následovanou samotnou chemoterapií (3). Standard léčby recidivy bude definován probíhající studií EORTC 2227 LEGATO, která randomizuje pacienty k paliativnímu podávání lomustinu +- v kombinaci s opakovanou radioterapií.
24.4.2.1 U pacientů s progresí po předchozí chirurgické a radiační terapii
- preference režimů temozolomid monoterapie, lomustin monoterapie, PCV.
24.4.2.2 U pacientů s progresí po 1. linii chemoterapie, v celkově dobrém stavu
- 2. linie chemoterapie – volba odlišného režimu od režimů podaných v adjuvanci nebo 1. linii paliativní chemoterapie:
- temozolomid v monoterapii,
- PCV,
- lomustin (CCNU) v monoterapii,
- režim PEI (pro 3. a další linii),
- režim EP (pro 3. a další linii),
- fotemustin v monoterapii – indikovat u pacientů ve velmi dobrém stavu.
Léčebný algoritmus gliálních nádorů mozku dle molekulárních markerů (upraveno dle EANO guidelines 2021, WHO klasifikace 2021 a NCCN guidelines 2025)
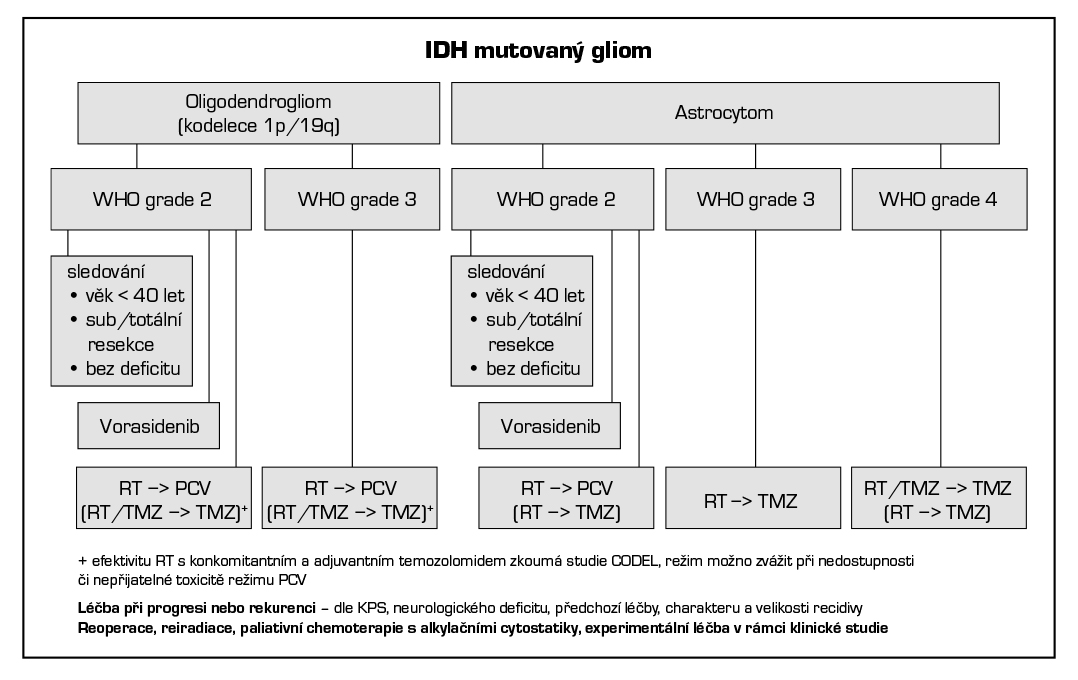
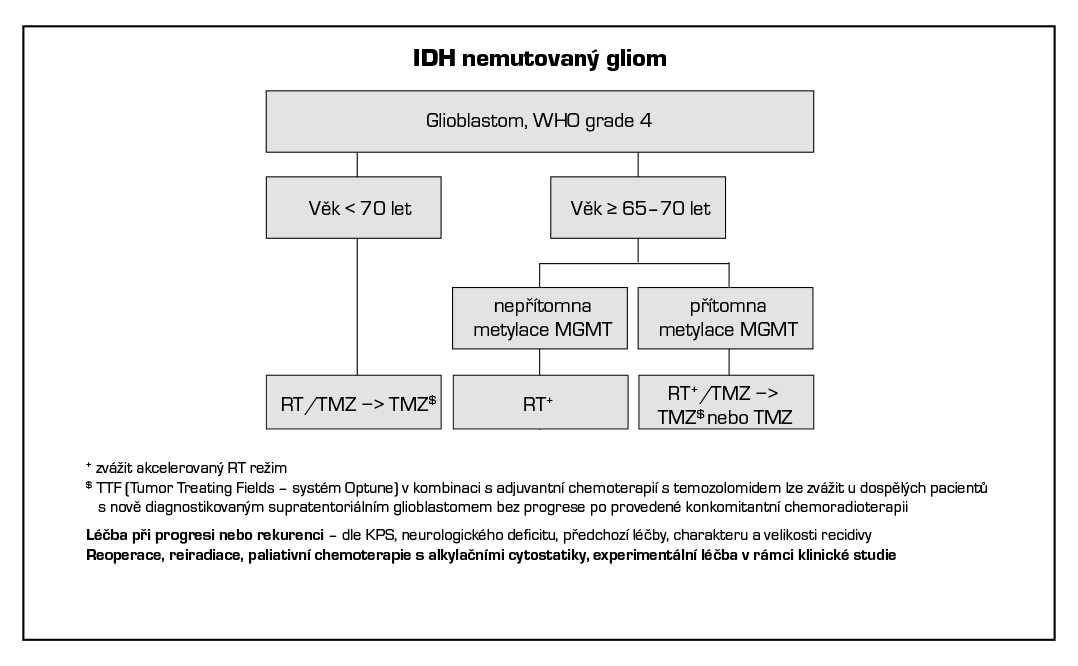
24.5 Ependymomy
Možno zvážit paliativní chemoterapii na basi derivátů nitrosourey, temozolomidu, platiny a etoposidu u pacientů s vyčerpanými možnostmi chirurgie a radioterapie. Adjuvantní chemoterapie není standardně indikována.
24.6 Embryonální tumory (meduloblastomy)
U skupiny s běžným rizikem rekurence (reziduální nádor < 1,5 cm2, bez metastáz v páteřním kanálu na MR, cytologicky negativní mozkomíšní mok, absence vzdálené diseminace) je indikována pooperační radioterapie kraniospinální osy (standardní nebo volitelně i redukovaná dávka) nebo konkomitantní chemoradioterapie kraniospinální osy s následnou chemoterapií.
U skupiny s vysokým rizikem rekurence (neresekabilní nebo reziduální nádor > 1,5 cm2 nebo metastázy v páteřním kanálu na MR nebo cytologicky pozitivní mozkomíšní mok nebo vzdálená diseminace nebo velkobuněčný meduloblastom nebo supratentoriální embryonální tumor nebo při nalezení mutace TP53) je indikována pooperační konkomitantní chemoradioterapie kraniospinální osy (standardní dávka ozáření) s následnou chemoterapií.
V případě recidivy zvažovat resekční výkon s následnou radioterapií a/nebo chemoterapií nebo high-dose chemoterapií s autologní transplantací PBSC.
Vzhledem k dětskému typu primárního nádoru mozku je vždy vhodná konzultace s dětskými onkology.
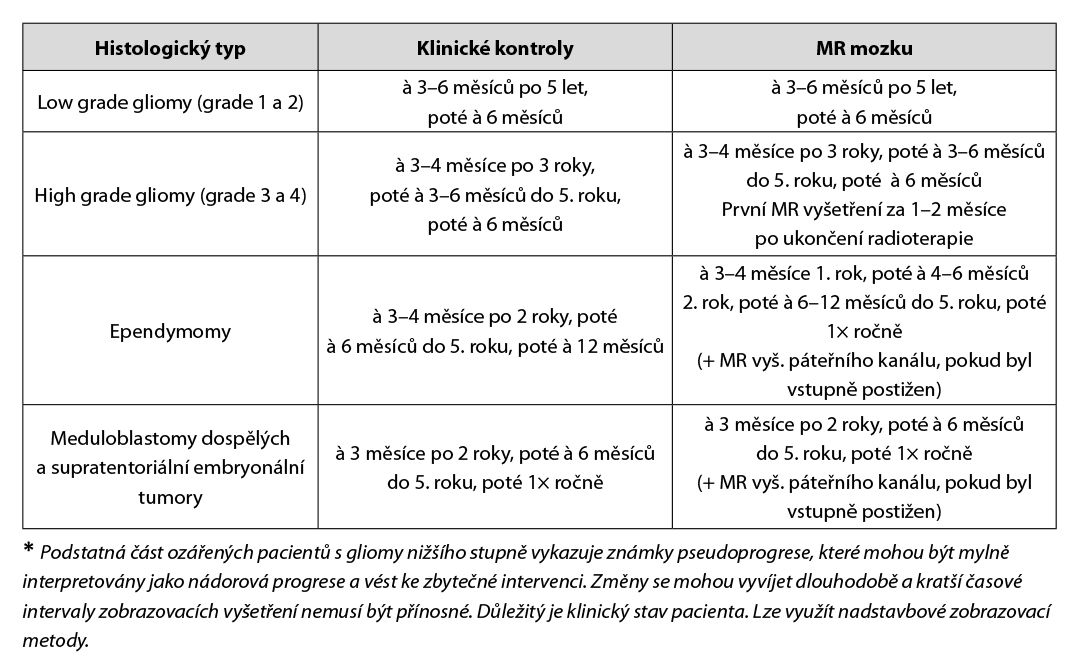
24.7 Dispenzarizace pacientů po léčbě (follow-up)
Dispenzarizaci provádí radiační a klinický onkolog, neurochirurg, případně praktický lékař. Klinické kontroly probíhají ve spolupráci s neurologem (EEG vyš., antiepileptická léčba).
Laboratorní vyšetření:
- standardně jen při chemoterapii, při kortikoterapii glykémie a kalémie
- při antiepileptické terapii dle indikace hladina antiepileptik v séru, dále KO+dif., jaterní testy.
Zdroj: NCCN guidelines v 3.2025, EANO guidelines 2021.
Změna je plně v kompetenci ošetřujícího lékaře!!!
Literatura:
- Weller M, van den Bent M, Preusser M. et al. EANO guidelines on the diagnosis and treatment of diffuse gliomas of adulthood. Nat Rev Clin Oncol. 2021 Mar;18(3):170-186.
- Capper D, Reifenberger G, French PJ, et al. EANO guideline on rational molecular testing of gliomas, glioneuronal, and neuronal tumors in adults for targeted therapy selection. Neuro Oncol. 2023 May 4;25(5):813-826. doi: 10.1093/neuonc/noad008.
- Baumert, Brigitta G. et al. ESTRO-EANO guideline on target delineation and radiotherapy for IDH-mutant WHO CNS grade 2 and 3 diffuse glioma. Radiotherapy and Oncology, Volume 202, 110594
- NCCN Clinical Practice Guidelines in Oncology, Central Nervous System Cancers, Version 3.2025.
- Šlampa P, a kol. Radiační onkologie. Maxdorf Jessenius, Praha, 2022, 772 s.
- Karschnia P, Young JS, Dono A, et al. Prognostic validation of a new classification system for extent of resection in glioblastoma: A report of the RANO resect group. Neuro Oncol. 2023 May 4;25(5):940-954.
- Miller JJ, Gonzalez Castro LN, McBrayer S, et al. Isocitrate dehydrogenase (IDH) mutant gliomas: A Society for Neuro-Oncology (SNO) consensus review on diagnosis, management, and future directions. Neuro Oncol. 2023 Jan 5;25(1):4-25.
- Cloughesy TF, van den Bent MJ, Touat M, et al. Vorasidenib in IDH1-mutant or IDH2-mutant low-grade glioma (INDIGO): secondary and exploratory endpoints from a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2025 Dec;26(12):1665-1675.
- van den Bent MJ, Ghisai SA, Wick W, et al. Concurrent and adjuvant temozolomide for 1p/19q non-co-deleted anaplastic glioma (CATNON; EORTC study 26053-22054): final and exploratory analyses of a randomised, open-label, phase 3 trial. Lancet Oncol. 2026 Jan;27(1):45-56.
