Rozhodnutí o terapeutickém postupu by mělo být provedeno multidisciplinárním týmem. Primární léčba je založena na lokalizaci a rozsahu nádoru, histologickém typu, komorbiditách/PS pacienta. Doporučené léčebné postupy jsou kategorie 1, není-li uvedeno jinak.
Kritéria ke konzultaci multidisciplinárního týmu:
- všichni noví pacienti
- oligometastatické postižení, je-li zvažována lokální léčba – definice oligometastatického onemocnění: DOI: 10.1016/j.ejca.2024.114062
- pacienti zvažovaní k indikaci HIPEC či PIPAC
Endoskopická léčba a radikální chirurgický výkon by měly probíhat ve specializovaných (high volume) centrech. Doporučení pro endoskopickou léčbu premaligních a časných maligních lézí jícnu jsou zpracovány a dostupné na www.endoskopiste.cz/wp-content/uploads/2021/06/barrett-guidelines.pdf.
Všem pacientům by mělo být poskytnuto komplexní nutriční poradenství, od běžné plnohodnotné stravy, přes enterální až po kompletní parenterální výživu. Všem pacientům by rovněž měla být nabídnuta rehabilitační a psychoonkologická péče.
Chirurgická léčba
Chirurgická resekční léčba má kurativní potenciál, tento se ale plně uplatňuje pouze ve velmi časných stadiích nemoci, většina pacientů relabuje, proto je chirurgie součástí multimodalitní léčby a chirurgický výkon je vždy konsultován v multidisciplinárním týmu. Chirurgická resekce (gastrektomie) může být parciální (distální, proximální, segmentální, lokální), subtotální či totální. O rozsahu resekce rozhoduje velikost nádoru, jeho lokalizace, stadium onemocnění, nádorová histopatologie, ale také celkový stav pacienta. Standardním typem resekčního výkonu je subtotální gastrektomie v případě distálního typu nádoru a totální gastrektomie u orálněji lokalizovaných karcinomů. U vybraných typů proximálních nádorů, resp. nádorů kardioezofageálního přechodu (Siewert 3 popřípadě 2) je možné zvážit proximální gastrektomii. U lokálně pokročilých nádorů žaludku a distálního jícnu je možná (výjimečně) ezofagogastrektomie. Dle posledních ESMO doporučení (ve shodě s poslední verzí Japonské asociace pro karcinom žaludku) by v případě expanzivního typu nádorového růstu (včetně intestinálních histotypů) měl být proximální okraj resekce lokalizován nejméně 3 cm od okraje nádoru, v případě infiltrativního růstu (špatně kohezivní/difuzní typ nádoru) nejméně 5 cm. Nelze-li tyto parametry naplnit, je doporučeno vyšetření resekční linie v celé tloušťce „na zmrzlo“ (k potvrzení R0 resekce).
Nedílnou součástí operačního výkonu je lymfadenektomie, standardním výkonem je D2 lymfadenektomie (v případě T1 nádorů je možná D1+), zvláště v lokálně pokročilejších stadiích přináší benefit v délce přežívání a přesnějším stagingu nádorového onemocnění ve srovnání s D1 resekcí. Ve speciálních případech (lokální šíření nádoru) je možné zvážit extenzi lymfadenektomie v některém z D3 kompartmentů, tento postup ale není standardem. U nádorů s lokálním šířením bez známek generalizace je možná přidružená orgánová resekce (slezina, slinivka, játra), morbidita rozšířených resekcí je ovšem vyšší proti standardnímu výkonu.
V určitých (symptomatických) případech může být po indukční léčbě indikována gastrektomie současně s oligometastatickým postižením, dlouhodobý efekt je však nejistý. Rovněž nadějně se jeví efekt gastrektomie, cytoredukční chirurgie a HIPEC u limitované formy peritoneálního metastatického postižení, jednoznačné důkazy pro dlouhodobý efekt uvedených postupů zatím nejsou k dispozici.
Standardem v operativě žaludku zatím zůstává operace z laparotomického přístupu, je však možný i laparoskopický přístup, častěji při distální resekci žaludku, v rukách zkušeného laparoskopického chirurga je možná i totální gastrektomie s D2 lymfadenektomií s dlouhodobými výsledky srovnatelnými s otevřenou operací. Velmi perspektivní se jeví robotická chirurgie gastrektomie, ve východní Asii je již plně etablována, je ale frekventována již i v EU, v ČR se začíná rozvíjet. Miniinvazivní výkony je možné kombinovat s částečně otevřeným přístupem (hybridní operace).
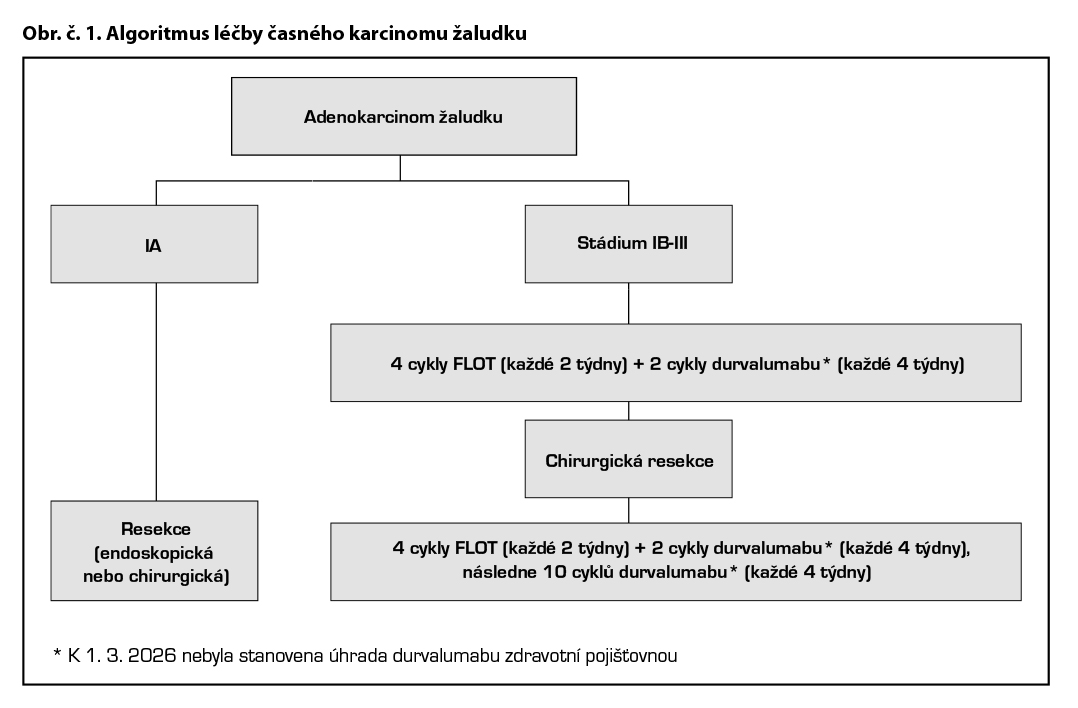
Tis, T1a
– primární léčba je endoskopická, případně chirurgická.
T1b N0, M0
– primární léčba je chirurgická.
Klinické stádium ≥IB-III (>T1, a/nebo ≥N0 M0), potenciálně resekabilní karcinom žaludku a gastroesofageální junkce
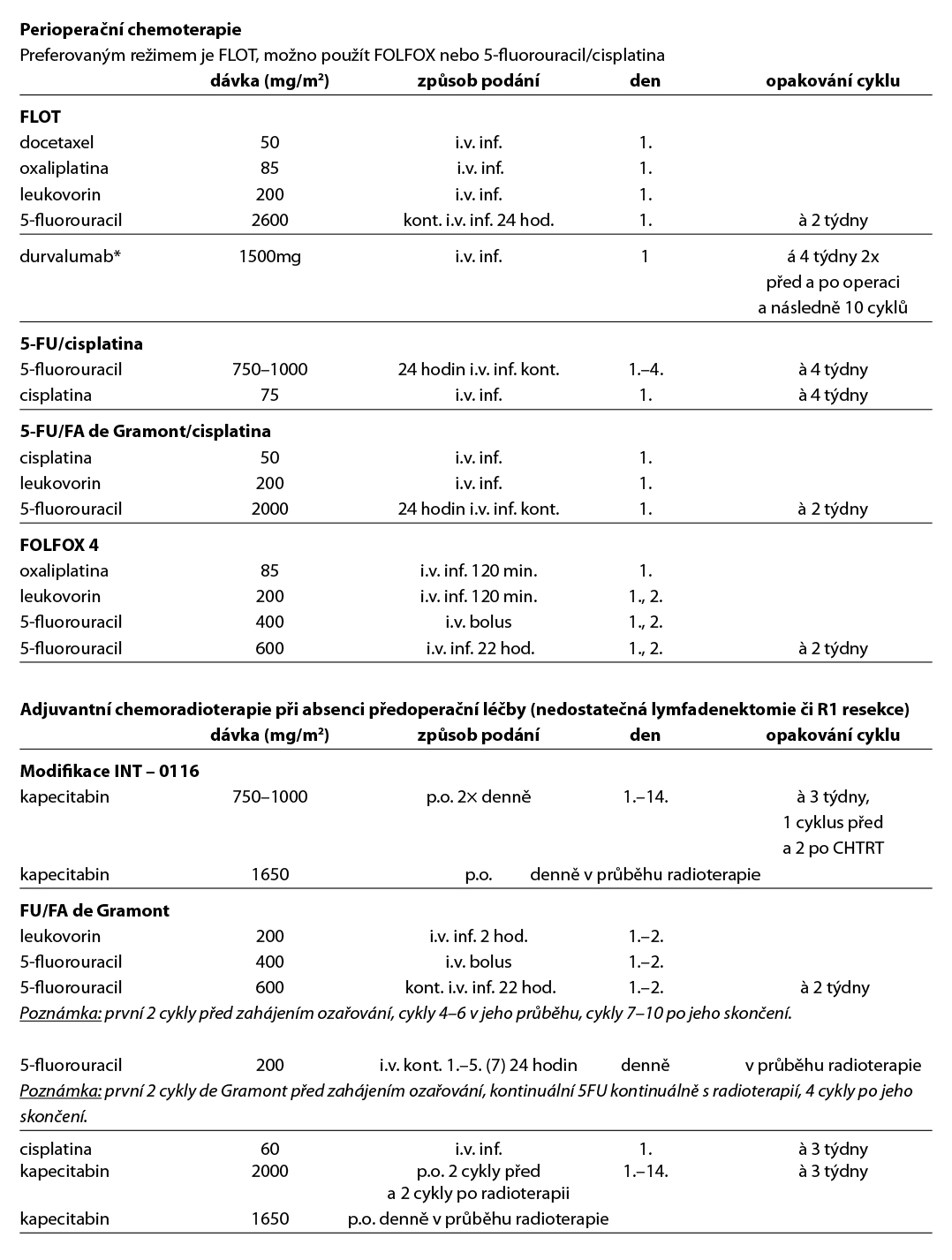
Perioperační léčba
Standardem léčby resekabilního karcinomu žaludku je perioperační chemoterapie FLOT v kombinaci s checkpoint inhibitorem durvalumabem*.
Racionále k perioperační chemoterapii (CHT)
- Prodlužuje celkové přežití pacientů a je standardním léčebným postupem.
- Efekt perioperační chemoterapie na bázi 5-fluorouracilu a cisplatiny/oxaliplatiny prokazují výsledky několika randomizovaných studií fáze III (studie MAGIC, EORTC 40954, ACCORD, FLOT4).
- Režim FLOT zlepšil ve studii AIO celkové přežití pacientů s lokálně pokročilým onemocněním a je preferovaným standardem perioperační léčby; pro starší pacienty s komorbiditami je alternativou dvojkombinace 5-fluorouracilu s oxaliplatinou.
- Infuzní fluorouracil a kapecitabin jsou v použití rovnocenné stejně jako cisplatina s oxaliplatinou. S ohledem na toxicitu bolusového fluorouracilu se doporučuje jeho náhrada infuzním fluorouracilem či kapecitabinem.
- Primární chirurgický výkon by měl být indikován jenom ve zvláštních případech jako je krvácející nádor a obstrukce způsobená tumorem.
Perioperační chemoterapie
Pro adenokarcinomy jícnu a gastroezofageální junkce je indikována perioperační chemoterapie režimem FLOT (4 cykly před a 4 cykly po operaci).
Perioperační chemoterapie + imunoterapie: FLOT plus durvalumab*
Recentně bylo prokázáno, že FLOT v kombinaci s imunoterapií durvalumab* signifikantně prodloužuje EFS a zlepšuje patologickou kompletní odpověď ve srovnání se samotnou chemoterapií (studie fáze III MATTERHORN) – nutné žádat schválení durvalumabu zdravotní pojišťovnou.
Perioperační léčba u HER2 pozitivních adenokarcinomů
U HER2-pozitivních nádorů nebyl dosud jednoznačně prokázán přínos kombinace perioperační chemoterapie a HER2 pro celkové přežití. Ve studii fáze II AIO-PETRARCA vedla kombinace FLOT a trastuzumab k vyšší míře histopatologické odpovědi a byl rovněž pozorován trend k lepšímu přežití bez progrese a celkovému přežití při kombinaci chemoterapie FLOT s trastuzumabem + pertuzumabem. Mezinárodní studie EORTC1203-INNOVATION dokladovala velmi slibnou míru odpovědí, zejména u kombinace FLOT + trastuzumab, zatímco FLOT + trastuzumab + pertuzumab neprokázal další přínos zejména pro zvýšenou toxicitu. Tyto údaje vyžadují ověření na větších a nezávislých kohortách. V individuálních případech a po projednání v multidisciplinární nádorové komisi lze však již nyní u pacientů s lokálně pokročilými HER2-pozitivními karcinomy žaludku nebo GEJ v případě sporné R0 resekability zvážit primární systémovou léčbu pomocí FLOT + trastuzumabu*.
Perioperační léčba u dMMR/MSI-H adenokarcinomů:
Dle retrospektivní metaanalýzy dat z pěti randomizovaných studií fáze III vedla perioperační chemoterapie založená na dvojkombinaci 5-fluorouracilu a platinovém derivátu u skupiny s MSI-H/MMR-D k horším výsledkům než samostatná chirurgie, a proto by tato skupina pacientů neměla být léčena perioperační dvojkombinací fluoropyrimidinu a platinového derivátu.
Prospektivní studie fáze II, a to francouzská NEONIPIGA (ipilimumab/nivolumab), a italská INFINITY (tremelimumab/durvalumab), dokladovaly u pacientů s lokálně pokročilým primárně operabilním dMMR/MSI-H adenokarcinomem GEJ/žaludku léčených samotnou neoadjuvantní imunoterapií dosažení patologické kompletní remise (pCR) až v 60 % případů (pT0N0). Podobně data ze studie fáze II DANTE ověřila přínos kombinace FLOT a atezolizumab. V současné době by v případech potvrzeného stavu MSI-high/dMMR měla být podávána perioperační imunoterapie – nejspíše durvalumabem v kombinaci s chemoterapií FLOT – dle randomizované studie MATTERHORN. Je otázkou, v jakých případech budou moci být pacienti léčeni pouze imunoterapií.
Všichni pacienti s lokálně pokročilým adenokarcinomem by tedy měli být testováni na dMMR/MSI-H stav a v případě deficitu/instability konzultováni cestou multidisciplinárního týmu. V případě operabilního onemocnění může být zvážena primární chirurgická léčba. Je-li nutné docílit downstagingu, lze zvážit kombinaci FLOT s imunoterapií. Léčba checkpoint inhibitory v této indikaci však není hrazena a postup by měl být individuální.
Adjuvantní chemoterapie při absenci předoperační léčby
Asijská studie fáze III CLASSIC prokázala u klinického stádia II-IIIB – po radikální resekci včetně D2 lymfadenektomie, že adjuvantní chemoterapie (oxaliplatina + kapecitabin XELOX 8 cyklů) signifikantně prodlužuje medián OS a DFS (2A), data u evropské populace jsou limitovaná, dle metaanalýzy z roku 2010 přináší adjuvantní chemoterapie benefit v OS 6 %.
Adjuvantní chemoradioterapie karcinomu žaludku
Prakticky jedinou pozitivní studií ve prospěch použití adjuvantní chemoradioterapie je americká studie z roku 2000 Intergroup INT0116 (prodloužení 3letého přežití bez progrese). Také update studie po 10 letech prokázal stejný benefit. Nicméně studii je vyčítáno, že radioterapie pouze kompenzovala nedostatečný chirurgický výkon, poněvadž 54 % pacientů podstoupilo D0 resekci a pouze 10 % D2 lymfadenektomii.
Ostatní studie fáze III (CRITICS a ARTIST) neprokázaly benefit v OS. Adjuvantní radioterapii lze zvážit při R1 resekci. I zde je však potřeba přihlédnout vyšší pravděpodobnosti vzdáleného relapsu onemocnění.
Předchozí negativní data doplňuje i recentně publikovaná studie fáze III TOPGEAR (2025): přidání předoperační chemoradioterapie (CRT) ke standardní perioperační chemoterapii zlepšilo patologickou odpověď, ale nezlepšilo celkové přežití (OS) ani přežití bez progrese (PFS) ve srovnání s perioperační chemoterapií samotnou.
Shora uvedené randomizované studie nepodporují použití adjuvantní radioterapie.
Perioperační chemoterapie a neoadjuvantní chemoradioterapie
Randomizovaná studie fáze III TOPGEAR ověřovala, zda přidání předoperační CRT k perioperační chemoterapii nezlepší OS u pacientů s resekabilními adenokarcinomy GEJ a žaludku; výsledky studie neprokázaly benefit radioterapie ve schématu perioperační chemoterapie.
Lokálně pokročilé neresekabilní či metastatické onemocnění
Paliativní chemoterapie
zlepšuje kvalitu života a OS ve srovnání s nejlepší podpůrnou léčbou (BSC).
Single agent chemoterapie nemá vliv na přežívání.
Základními cytostatiky u pokročilého a metastatického karcinomu žaludku jsou: 5-fluorouracil (často v kombinaci s leukovorinem), jeho perorální prodrug kapecitabin, případně kombinovaný perorální fluoropyrimidinový derivát Teysuno, dále deriváty platiny (cisplatina a oxaliplatina), taxany (paclitaxel, docetaxel), irinotekan. Cisplatina i oxaliplatina stejně jako infuzní 5-fluorouracil a kapecitabin jsou volně zaměnitelné. Režim s kontinuálním 5-fluorouracilem nebo perorální léčba kapecitabinem jsou preferovány před podáváním bolusového 5-fluorouracilu, který má vysokou toxicitu. Režimy s oxaliplatinou jsou preferovány u pacientů ve věku nad 65 let.
Základními cílenými (biologickými) léky, jež používáme v této indikaci, jsou trastuzumab a protilátkový konjugát trastuzumab deruxtecan*, předpokladem použití obou léčiv je přítomná pozitivita HER2 (asi 12 % případů karcinomu žaludku a GEJ). Dále je k dispozici zolbetuximab*, protilátka proti Claudinu 18.2 (cca 35 % karcinomů žaludku), ramucirumab*, protilátka proti receptoru vaskulárního endoteliálního růstového faktoru (VEGFR2).
Radioterapie je indikována ke kontrole symptomů (krvácení, bolest, obstrukce).
Paliativní endoskopické výkony zahrnují endoluminální laserovou terapii, zavedení endoluminálního stentu, gastrojejunostomii jako součást řešení nádorové obstrukce.
Paliativní chirurgické metody zahrnují paliativní resekci, která je indikována v případě nádorové obstrukce, krvácení či zavedení výživové jejunostomie, vysoce paliativním výkonem je zavedení derivační gastrostomie.
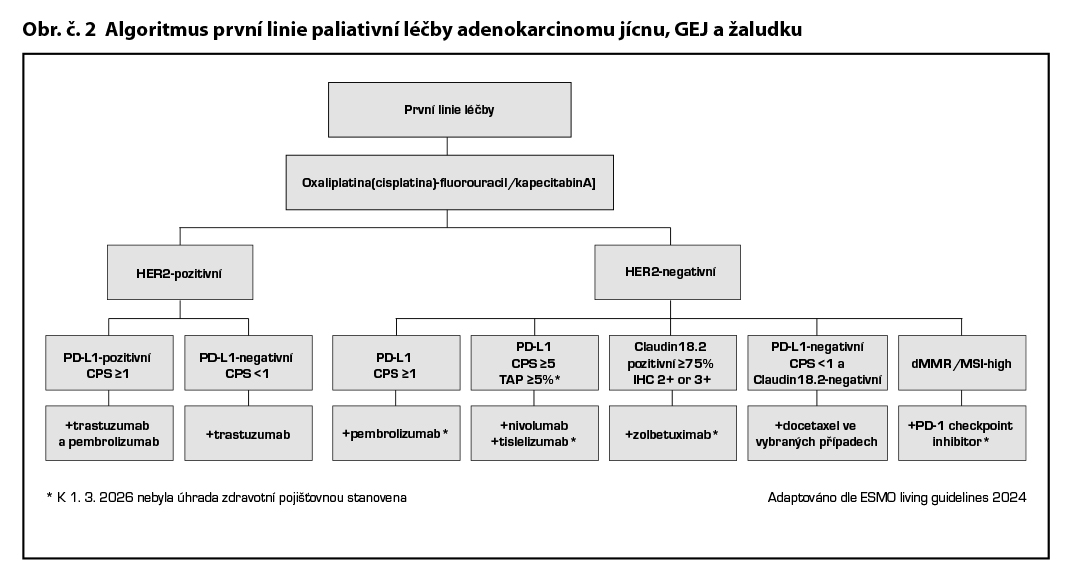
První linie metastatického onemocnění
Preferovaná je dvojkombinace na bázi fluorouracilu a platinového derivátu. Z režimů dvojkombinace používáme FOLFOX či FLO, 5-FU/cisplatina nebo kapecitabin/cisplatina nebo oxaliplatina a jejich modifikace (studie ML 17032). Trojkombinaci, zpravidla FLOT, indikujeme u mladých pacientů, u pacientů s cílem dosažení rychlé kontroly symptomů nebo u pacientů s oligometastatickým onemocněním, kde zvažujeme operabilitu.
Francouzská studie fáze III prokázala významně delší přežití bez progrese a významně delší celkové přežití u tripletu platina-fluoropyrimidin-docetaxel (modifikovaný FLOT, tzv. T-FOX) ve srovnání s dubletem FOLFOX. Je nutné zdůraznit, že všichni pacienti byli docetaxel-naivní a že benefit nebyl pozorován u pacientů starších 65 let, u pacientů s výkonnostním stavem dle ECOG > 0 a u karcinomů intestinálního typu. Vhodnou indikací modifikované trojkombinace chemoterapie FLOT/T-FOX jsou pacienti s velkým rozsahem onemocnění a snahou dosažení rychlého zmenšení nádorové masy a pacienti s nádory s absencí prediktivních markerů k cílené terapii nebo imunoterapii. Standardem zůstává platinovo-fluoropyrimidinový dublet.
Režim s redukovanou dávkou oxaliplatiny a kapecitabinu na 60 % byl ve skupině starších a křehkých pacientů léčených pro inoperabilní lokálně pokročilý či metastatický gastroezofageální karcinom lépe tolerován se srovnatelným dosaženým efektem – výsledky studie GO2.
S1 (Teysuno) je možno kombinovat s cisplatinou i oxaliplatinou, účinnost je srovnatelná, ale profil nežádoucích účinků se liší ve prospěch S1.
Irinotekan, zvlášť v kombinaci s fluorouracilem, je vhodný i do první linie léčby metastatického onemocnění, kdy je indikován v situaci, kdy není možno použít platinový derivát (studie fáze III FOLFIRI s režimem ECF). Medián TTF byl signifikantně delší v rameni s FOLFIRI, režim FOLFIRI byl také lépe tolerován, i když medián PFS a OS byl srovnatelný.
Léčba HER2 negativního a PD-L1 pozitivního neresekabilního nebo metastatického adenokarcinomu GEJ a žaludku
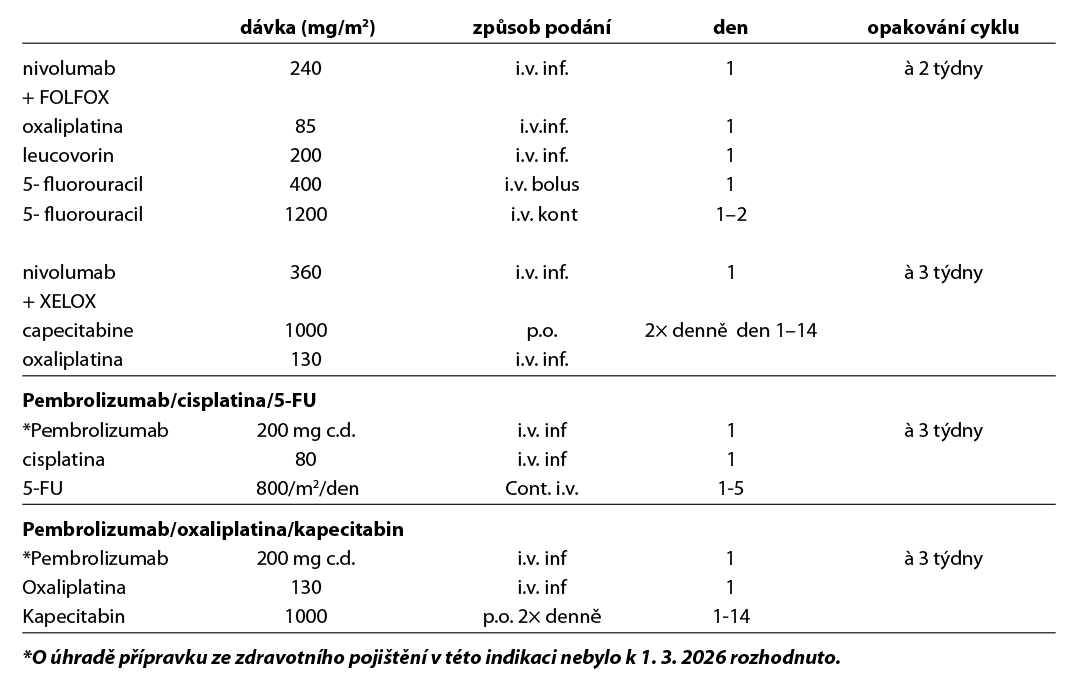
Kombinace fluoropyrimidinu a oxaliplatiny s nivolumabem je léčebným standardem pro pacienty s PD-L1 expresí CPS≥5 (studie fáze III CheckMate 649). Podobně i pembrolizumab* v kombinaci s chemoterapií zlepšuje celkové přežití pacientů s PD-L1 pozitivními nádory, benefit je vyšší dle míry CPS (CPS≥10 > CPS≥1; studie fáze III KEYNOTE-859). Tislelizumab* v kombinaci s chemoterapií je dalším checkpoint inhibitorem, který je doporučen EMA u populace pacientů s HER2 negativním PD-L1 TAP≥5 (tumor area positivity).
Léčba HER2 pozitivního neresekabilního nebo metastatického adenokarcinomu karcinomu GEJ a žaludku
Dle evropských standardů (EMA) je HER2 pozitivita u karcinomu GEJ/žaludku definována jako přítomnost exprese proteinu s imunohistochemickým (IHC) skóre 3+ nebo IHC 2+ a současná genová amplifikace v in situ hybridizaci (ISH) s poměrem HER2/CEP17 ≥2,0, v podmínkách ČR je však v indikaci IHC 2+/amplifikace nutno o evropský standard žádat zdravotní pojišťovnu. Diagnostika HER2 by měla bát zhodnocena s centrální/certifikované laboratoři).
Léčba HER2 pozitivního a PD-L1 CPS <1 neresekabilního nebo metastatického adenokarcinomu GEJ a žaludku
Trastuzumab by měl být přidán k chemoterapii na bázi 5-fluorouracilu a platinového derivátu (např. CAPOX, FOLFOX nebo FLO) u pacientů s HER2-pozitivním pokročilým karcinomem žaludku. Doporučení vychází z údajů studie fáze III ToGA, která prokázala vyšší míru léčebných odpovědí a prodloužené přežití u chemoterapie trastuzumabem, cisplatinou a fluoropyrimidinem ve srovnání s chemoterapií samotnou u pacientů splňujících výše uvedená výběrová kritéria. Kombinace trastuzumabu a oxaliplatiny plus fluoropyrimidinu vedou k výsledkům srovnatelným s historickým režimem ToGA obsahujícím cisplatinu.
Trastuzumab je indikován v nasycovací dávce 8 mg/kg a pokračující 6 mg/kg v případě třítýdenního podání, a v dávce 6 mg/kg a pokračující 4 mg/kg v případě 2týdenní aplikace. V případě průkazu amplifikace a nepředléčenosti trastuzumabem v 1. linii je možné trastuzumab aplikovat i v 2. linii*.
Léčba HER2 pozitivního a PD-L1 CPS≥1 neresekabilního nebo metastatického adenokarcinomu GEJ a žaludku
Ve studii fáze III KEYNOTE-811 vedlo přidání pembrolizumabu k trastuzumabu a chemoterapii ke zlepšení ORR, PFS a OS ve srovnání se samotným trastuzumabem-CHT. Pacienti s PD-L1 negativními nádory neměli z přidání pembrolizumabu žádný prospěch. Režim chemoterapie + trastuzumab a pembrolizumab je léčebným standardem u HER2 pozitivního PD-L1 CPS≥1 pozitivního neresekabilního nebo metastatického adenokarcinomu GEJ a žaludku.
Dle podmínek úhrady v ČR je chemoterapie s trastuzumabem s pembrolizumabem hrazena u IHC 3+ a PD-L1 CPS ≥ 1 pacientů s PS 0-1 do progrese nebo vyčerpání 35 cyklů.
Dle EMA je stejná kombinace hrazena i u pacientů s IHC 2+/ISH amplifikací* (ISH; HER2/CEP17 poměr ≥2.0), v této indikaci je nutno o evropský standard žádat zdravotní pojišťovnu.
Léčba Claudin 18-2 pozitivního (CLDN 18.2 IHC 2+/3+ ≥ 75 % nádorových buněk) karcinomu GEJ a žaludku
U pacientů s pokročilým neoperovatelným karcinomem žaludku/GEJ a expresí Claudin18.2 v ≥ 75 % nádorových buněk prodlužuje zolbetuximab*, chimérická monoklonální protilátka IgG1 cílená proti Claudin18.2, v kombinaci s chemoterapií FOLFOX, OS (studie fáze III SPOTLIGHT). Výsledky studie SPOTLIGHT jsou do značné míry potvrzeny multinárodní studií fáze III GLOW a rovněž souhrnné údaje z obou studií prokázaly zlepšení PFS a OS.
Hlavními vedlejšími účinky zolbetuximabu jsou nevolnost a zvracení, zejména během prvních několika aplikací. Pacienti by proto měli být zajištěni antiemetickou profylaxí, jak je doporučeno u vysoce emetogenní chemoterapie (viz kapitola 29), minimálně před a během prvních cyklů, a dále je důležité zpomalení rychlosti infuze zolbetuximabu, pokud se nevolnost a zvracení objeví.
*O úhradě přípravku ze zdravotního pojištění nebylo v této indikaci k 1. 3. 2026 rozhodnuto.
MSI-H/dMMR inoperabilní a metastatický adenokarcinom GEJ a žaludku
Vzhledem k přesvědčivé účinnosti inhibitorů PD-1/PD-L1 by všem pacientům s MSI-HIGH/dMMR adenokarcinomy žaludku a GEJ měl být podáván jeden ze schválených checkpoint inhibitorů jako první linie léčby. Analýzy podskupin jsou pozitivní pro podávání inhibitoru imunitního kontrolního bodu v kombinaci s chemoterapií ve všech studiích relevantních pro schválení EMA (CheckMate 649, KEYNOTE-859) a také ve studiích, které nemohly být použity pro schválení (včetně KEYNOTE-062). Rovněž data z prospektivní studie Keynote 158 (pembrolizumab*) a ze studie NO LIMIT (ipilimumab/nivolumab*) nebo GARNET (dostarlimab-gxly) potvrdila účinnost a možnost dosažení dlouhodobé remise při použití imunoterapie u metastatického onemocnění.
*O úhradě přípravku ze zdravotního pojištění nebylo v této indikaci k 1. 3. 2026 rozhodnuto.
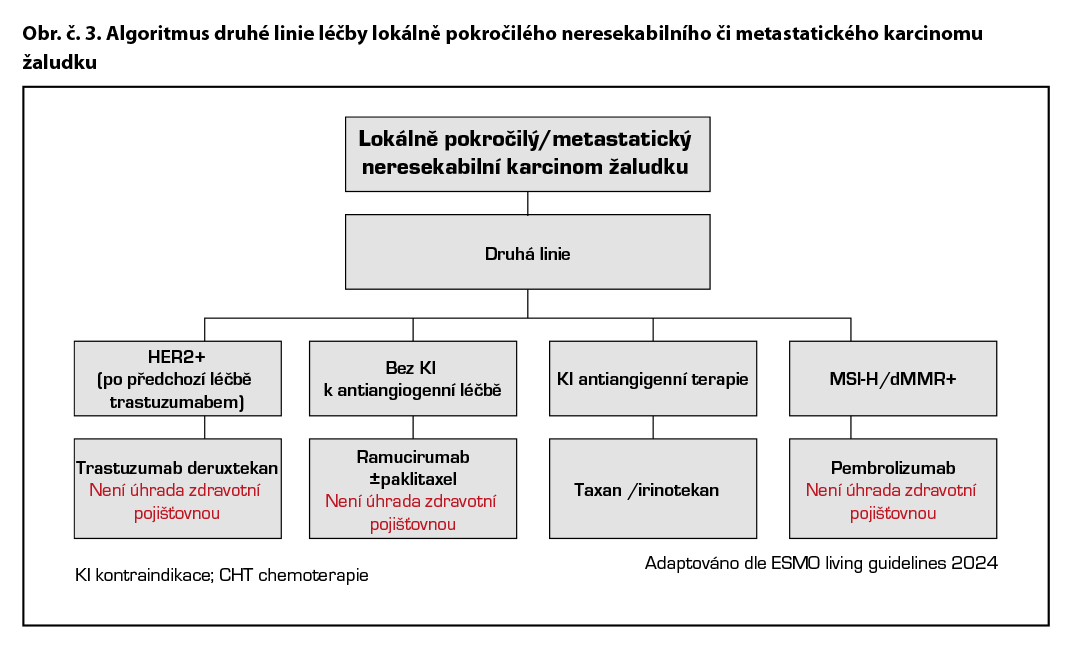
Chemoterapie 2. linie
Standardem je terapie irinotekanem, paklitaxelem či docetaxelem. Režim FOLFIRI je možno použít u pacientů v dobrém stavu – data jsou extrapolována z první linie.
Druhá linie léčby HER2 pozitivního onemocnění
U HER2 pozitivních adenokarcinomů GEJ a žaludku je po progresi po předchozí léčbě režimem založeném na trastuzumabu indikován trastuzumab deruxtekan* (T-DXd). Ve studii DESTINY-Gastric01 u asijské populace bylo celkové přežití delší s trastuzumab deruxtekanem než s chemoterapií. Podobně i u západní populace prokázal T-DXd klinickou účinnost a zvládnutelný bezpečnostní profil u HER2+ neresekovatelného/metastatického onemocnění po selhání na předchozí léčbě trastuzumabem a v neposlední řadě jsou k dispozici data z přímého srovnání ramucirumabu a paclitaxelu versus trastuzumab deruxtecan (studie DESTINY-Gastric04), která jednoznačně favorizují použití trastuzumabu deruxtecanu* po selhání režimu s trastuzumabem.
Druhá linie léčby HER2 negativního onemocnění
Ve studiích fáze II a III prokázala účinnost cytostatika irinotekan (v monoterapii či v kombinaci s fluoropyrimidinem), paklitaxel a docetaxel. Jejich zařazení do druhé linie vedlo k prodloužení přežití pacientů s metastatickým onemocněním o 1,5 měsíce.
Ramucirumab* je lidská monoklonální protilátka proti receptoru pro vaskulární endoteliální růstový faktor VEGFR2, jejíž podávání vede k blokádě vazby ligandů VEGF A, VEGF B. Účinnost ramucirumabu v léčbě karcinomu žaludku dosud testovaly dvě studie – REGARD a RAINBOW.
Ramucirumab v monoterapii mírně zlepšuje OS ve srovnání s placebem (studie fáze III REGARD).
Kombinace ramucirumabu s paklitaxelem rovněž zlepšuje OS a je evropským standardem, v ČR není tato léčba schválena (studie fáze III RAINBOW).
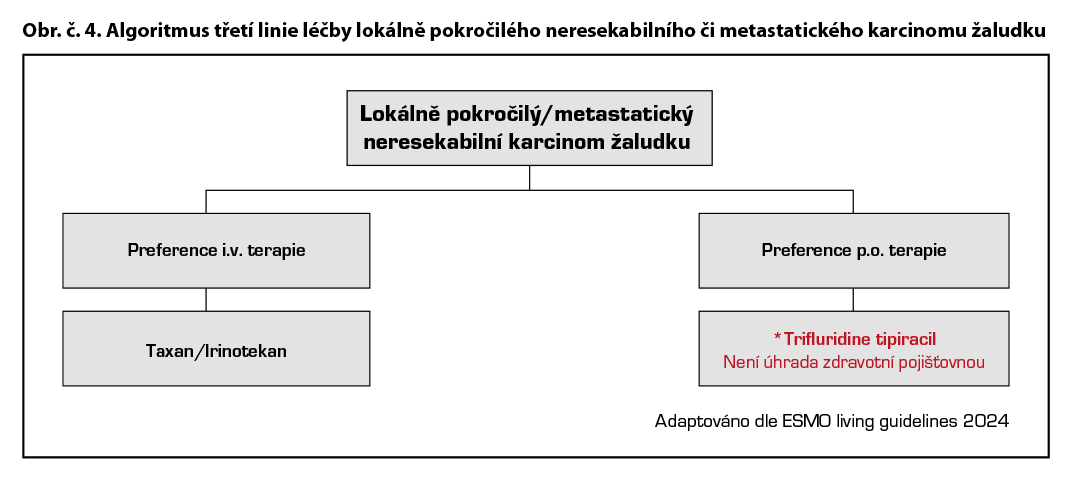
Třetí a další linie v léčbě metastatického onemocnění
Použití další linie by mělo být individualizováno dle celkového stavu pacienta a chemosenzitivity onemocnění. Délka léčby má vliv na celkové přežití pacientů. Trifluridine/tipiracil* je cytostatická kombinace antimetabolitu trifluridinu a inhibitoru thymidinfosforylázy tipiracilu, jehož účinnost a bezpečnost byla zhodnocena studií III. fáze (TAGS) u pacientů s metastazujícím karcinomem žaludku (včetně adenokarcinomu gastroesofageální junkce), kteří byli dříve léčeni alespoň dvěma režimy systémové terapie pro pokročilé stádium onemocnění zahrnující chemoterapii založenou na fluoropyrimidinu, platině a buď taxanu nebo irinotekanu, spolu s odpovídající terapií anti HER2. Trifluridine/tipiracil vedl ke statisticky signifikantnímu zlepšení OS.
Preferována je účast v klinických studiích, dále je možná léčba režimem s docetaxelem, paklitaxelem, irinotekanem, pokud tyto přípravky nebyly použity v předchozích liniích.
Pacienti, u nichž byla diagnostikována fúze NTRK genu, jsou kandidáty terapie NTRK inhibitory entrektinibem* a larotrektinibem*.
Na základě konzultace molekulární nádorové komise/tumor boardu (MTB) lze ve vybraných případech upřednostnit i dosud neschválenou léčebnou možnost, zejména pokud lze doporučení založit na stupnici ESMO pro klinickou účinnost molekulárních cílů (ESCAT) úrovně I nebo II.
*O úhradě přípravku ze zdravotního pojištění nebylo v této indikaci k 1. 3. 2026 rozhodnuto.
Prediktivní vyšetření
U všech pacientů s adenokarcinomem GEJ a žaludku je doporučeno vyšetřit HER2 a MSI-H/MMR-D před stanovením strategie léčby, v (neo)adjuvantním záměru před zahájením chemoterapie. Před zahájením paliativní terapie je dále nutno vyšetřit Claudin 18.2 a PD-L1 expresi. Indikací k léčbě zolbetuximabem* je exprese IHC 2+ nebo 3+ ve ≥ 75 % nádorových buněk. Hodnocení PD-L1 exprese se liší dle histologického typu a použitého checkpoint inhibitoru. U adenokarcinomu je indikací k léčbě nivolumabem CPS ≥ 5, k léčbě pembrolizumabem* CPS ≥ 1 a tislelizumabem* TAP ≥ 5 %.
V individuálních případech lze u pacientů ve IV. klinickém stadiu vyšetřit fúze NTRK (možnost terapie larotrektinibem a entrektinibem) a u pacientů v dobrém stavu při vyčerpání možností standardní léčby testování NGS a vyšetření TMB. Na základě konzultace molekulární nádorové komise/tumor boardu (MTB) lze ve vybraných případech upřednostnit i dosud neschválenou léčebnou možnost, zejména pokud lze doporučení založit na stupnici ESMO pro klinickou účinnost molekulárních cílů (ESCAT) úrovně I nebo II.
Dále je doporučováno vyšetření DPYD k predikci toxicity chemoterapie fluoropyrimidiny.

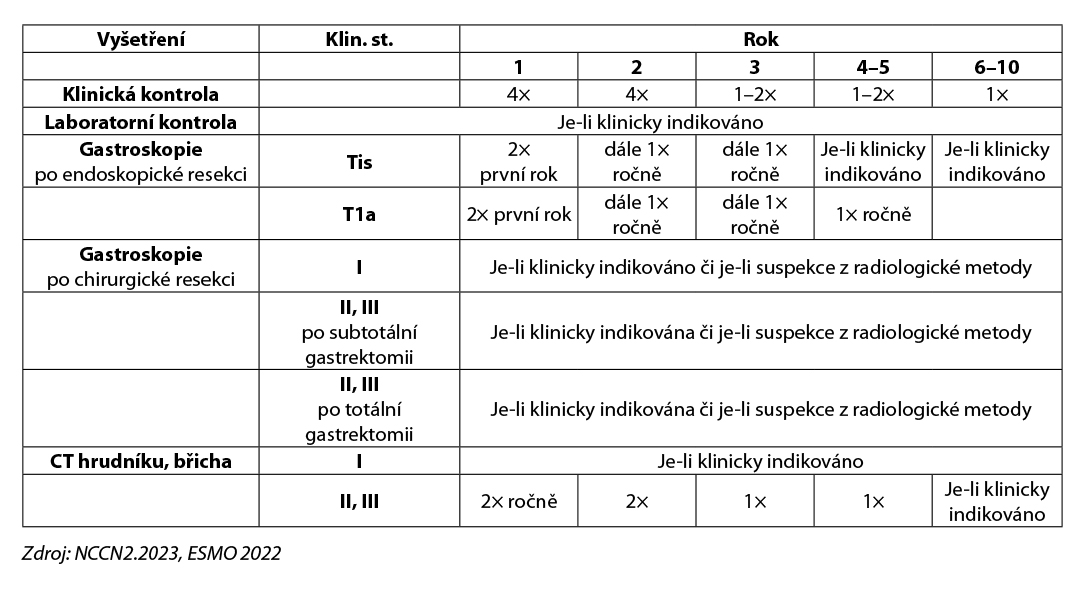
Karcinom žaludku – follow up po kurativní léčbě
Všichni pacienti by měli být sledováni systematicky, nicméně konsensus pro standardní follow-up neexistuje. Naše doporučení vychází z evropských (ESMO) a amerických (NCCN) guidelines.
PET/CT a gastroskopie po totální gastrektomii může být součástí follow-up, je-li klinické podezření na recidivu/relaps onemocnění.
- u všech pacientů zvážit nutnost nutriční podpory
- po totální gastrektomii, případně i po subtotálním výkonu je indikována monitorace hladiny B12 a železa a případná substituce, je-li diagnostikována nedostatečná hladina
Literatura:
- Hall PS, et al. Optimazing therapy for frail and elderly patients (pts) with advanced gastroesophageal cancer (GOAC): The GO2 phase III trial. J Clin Oncol 2019;37:4006.
- Janjigian YY, et al. First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649): a randomised, open-label, phase 3 trial. Lancet. 2021 Jul 3;398(10294):27-40.
- Janjigian YY, et al. The KEYNOTE-811 trial of dual PD-1 and HER2 blockade in HER2-positive gastric cancer. Nature 2021;600(7890):727-730. Janjigian YY et al. Pembrolizumab in HER2-Positive Gastric Cancer. N Engl J Med 2024 Oct 10;391(14):1360-1362.
- Japanese Gastric Cancer Association. Japanese gastric cancer treatment guidelines 2018 (5th edition). Gastric Cancer. 2021 Jan;24(1):1-21. DOI: 10.1007/s10120-020-01042-y.
- Lordick F, et al. ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2022 Oct;33(10):1005-1020. DOI: 10.1016/j.annonc.2022.07.004.
- NCCN Guidelines-v.1.6. Gastric Cancer.
- Shitara K, Shah MA, Lordick F, et al. Zolbetuximab in Gastric or Gastroesophageal Junction Adenocarcinoma. N Engl J Med. 2024 Sep 26;391(12):1159-1162.
- Zaanan A et al. 5-fluorouracil and oxaliplatin with or without docetaxel in the first-line treatment of HER2 negative locally advanced unresectable or metastatic gastric or gastro-esophageal junction adenocarcinoma (GASTFOX-PRODIGE 51): a randomized phase III trial sponsored by the FFCD. LBA77, ESMO 2023.
- André T, Tougeron D, Piessen G et al. Neoadjuvant nivolumab plus ipilimumab and adjuvant nivolumab in localized deficient mismatch repair/microsatellite instability-high gastric or esophagogastric junction adenocarcinoma: the GERCOR NEONIPIGA phase II study. J Clin Oncol 2023;41:255-265. DOI: 10.1200/JCO.22.00686.
- Janjigian YY, Al-Batran SE, Wainberg ZA et al; MATTERHORN Investigators. Perioperative durvalumab in gastric and gastroesophageal junction cancer. N Engl J Med 2025;393:217-230. DOI: 10.1056/NEJMoa2503701.
- Shitara K, Van Cutsem E, Gümüş M et al; DESTINY-Gastric04 Trial Investigators. Trastuzumab deruxtecan or ramucirumab plus paclitaxel in gastric cancer. N Engl J Med 2025;393:336-348. DOI: 10.1056/NEJMoa2503119.
- Tabernero J, Shitara K, Zaanan A et al. Trifluridine/tipiracil versus placebo for third or later lines of treatment in metastatic gastric cancer: an exploratory subgroup analysis from the TAGS study. ESMO Open 2021;6:100200. DOI: 10.1016/j.esmoop.2021.100200.
- Obermannova R et al. ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Annals of Oncology 2022, S0923-7534(22)01850-6.
- TNM klasifikace zhoubných novotvarů, 8. vydání, 2017.
