Úvod
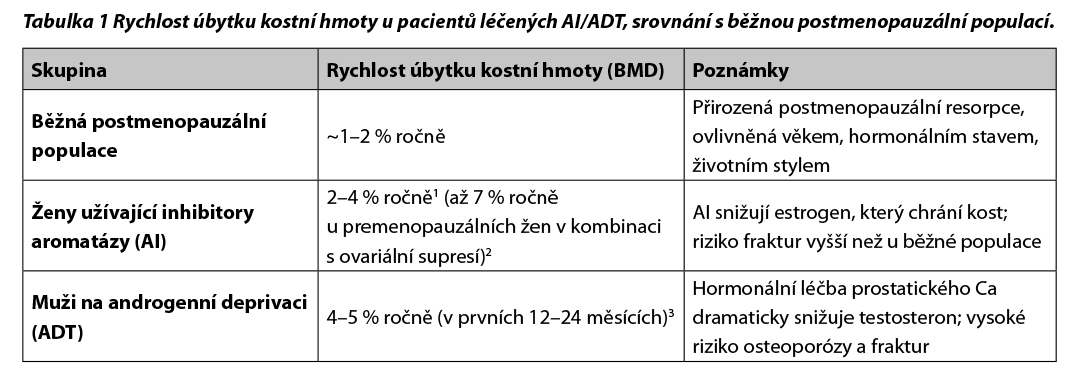
Osteoporóza je chronické metabolické onemocnění skeletu charakterizované úbytkem minerálové kostní hustoty a zhoršenou mikroarchitektonikou kostní tkáně. Klinickou manifestací jsou nízkoenergetické fraktury a/nebo kompresivní vertebrální zlomeniny, typicky bez známek traumatu. Klinickými projevy vertebrálních zlomenin jsou bolesti zad, snížení tělesné výšky, vznik kyfoskoliózy a omezení hybnosti. Celkovým dopadem osteoporózy je chronický algický syndrom, snížená mobilita a soběstačnost, zhoršená kvalita života a ve svém důsledku má osteoporóza značný socio-ekonomický dopad. Osteoporóza je typickým onemocněním vyššího věku, častější u štíhlých žen, ale existuje celá řada onemocnění, které zvyšují riziko vzniku osteoporózy, urychlují progresi kostní resorpce a posouvají klinickou manifestaci osteoporózy do mladšího věku. Onkologická onemocnění a některá léčiva používaná v onkologii patří mezi ně. Zvýšenou bdělost pro rozvoj osteoporózy je třeba mít u všech onkologicky nemocných, ale rutinní management rizika osteoporózy se týká zejména 2 klinických situací: 1/ ženy (příp. muži) s karcinomem prsu užívající inhibitory aromatázy (IA); 2/ muži s androgen deprivační léčbou (ADT). Rychlost úbytku kostní minerální hustoty (BMD) je shrnuta v Tab. 1.
Diagnostika
Zlatý standard pro diagnostiku osteoporózy je vyšetření DXA (Dual-energy X-ray Absorptiometry), které měří minerální kostní hustotu (BMD). Obvykle jsou měřena 3 referenční místa - bederní páteř a oba proximální femury nebo bederní páteř, proximální femur a distální předloktní nedominantní končetiny. BMD proximálního femuru nelze stanovat po TEP kyčle. Výsledkem DXA je T-skóre, které porovnává měřené BMD s BMD referenční mladé zdravé populace stejného pohlaví. Hodnocení výsledku je uvedeno v Tab. 2.

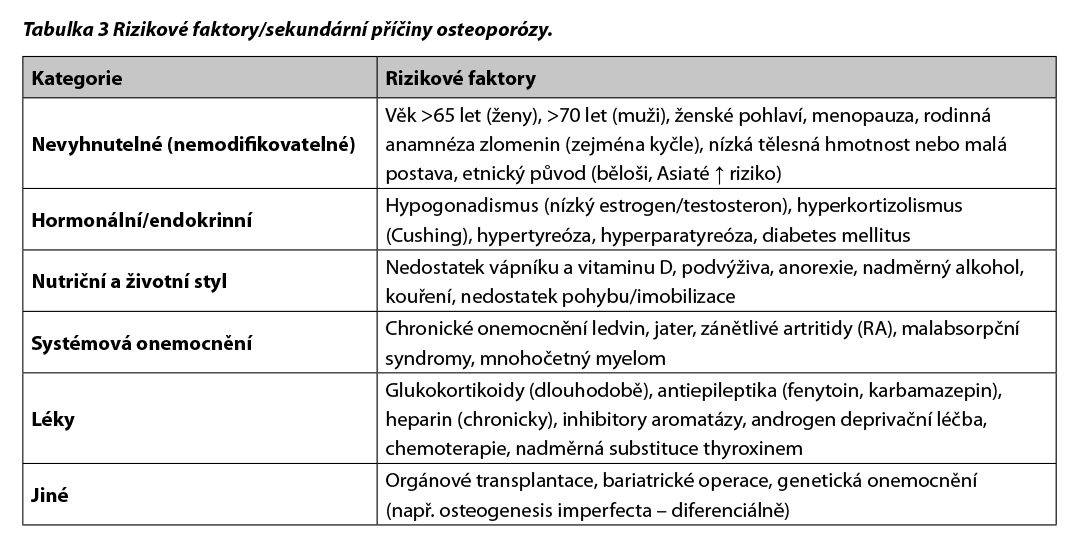
Samotná diagnóza se často stanoví podle T-skóre ≤ −2,5. Druhou možnou diagnostickou cestou je prodělání osteoporotické zlomeniny a to bez ohledu na T-skóre. V případě zlomeniny musí být pro diagnostiku osteoporózy vyloučena jiná (traumatická, onkologická) příčina(Melton et al.). V diferenciální diagnostice kostní nádorové nemoci vs. osteoporózy je nutné v některých případech přistoupit k biopsii. Není-li zjištěna příčina sekundární osteoporózy, jedná se o osteoporózu primární. Přehled nejčastějších příčin sekundární osteoporózy je uveden v Tab. 3.
Stratifikace rizika zlomenin u onkologicky nemocných
U všech pacientů, před zahájením léčby AI/ADT, má být dle doporučení ESMO4 proveden management kostního rizika, zahrnující:
- anamnézu fragilitní zlomeniny,
- věk, BMI,
- kouření, alkohol,
- oučasná kortikoterapie,
- rodinnou anamnézu zlomenin.
Vyšetření:
- DXA (bederní páteř+oba prox. femury, bederní páteř+prox. femur+dist. radius)
- laboratorně:
- Minimum: Ca, P, 25-OH vitamin D, PTH, TSH, albumin, urea, kreatinin, ALT, AST, ALP, GGT, glukóza, CRP, bílkovina v moči.
- Kostní markery: CTX-I (CrossLaps) a PINP jsou indikovány u pacientů před začátkem farmakoterapie a dále k monitoraci
léčby a přehodnocení terapie v pravidelných intervalech.
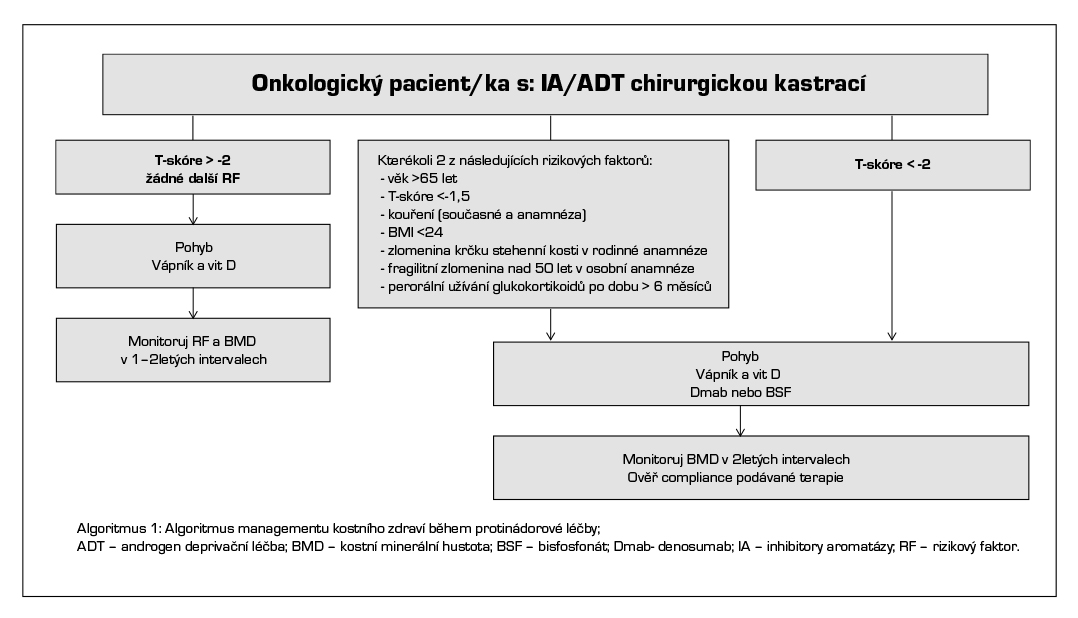
Terapii IA/ADT je třeba brát jako sekundární osteoporózu a je zde nižší práh pro léčbu oproti běžné populaci. Algoritmus sledování a zahájení léčby je uveden v Algoritmu 1 (přeloženo z 4).
Léčba
Léčba snížené kostní hustoty (osteoporózy i osteopenie) má 3 základní pilíře, z nichž první 2 lze bezpečně aplikovat u všech onkologických pacientů, a jsou součástí komplexního onkologického přístupu:
1. Pohyb – trénink s váhovým zatížením, odporový a balanční trénink, prevence pádů.
2. Nutrice a suplementace
a. vápník 1000–1200 mg/den, vitamin D 800–2000 IU (20–50 μg)/den, cílová hladina 25-OH vitD: min > 50 nmol/l
a optimum >75 nmol/l
b. vitamin K2 120–300 ug/den
c. proteiny 0,8 g/kg váhy/den
3. Specifická antiresorpční léčba.
Vápník by měl být preferenčně zajištěn stravou (přirozený zdroj, lepší biologická dostupnost, lepší snášenlivost), což však mnohdy není dostatečné a je nutné přistoupit k farmakologické substituci. Zde je potřeba upozornit, že mnoho preparátů nebývá pacienty dobře snášeno a není užíváno pravidelně. Dokud není vyřešen dostatečný přísun vápníku, není bezpečné zahájení specifické antiresorpční léčby vzhledem k riziku hypokalcémie.
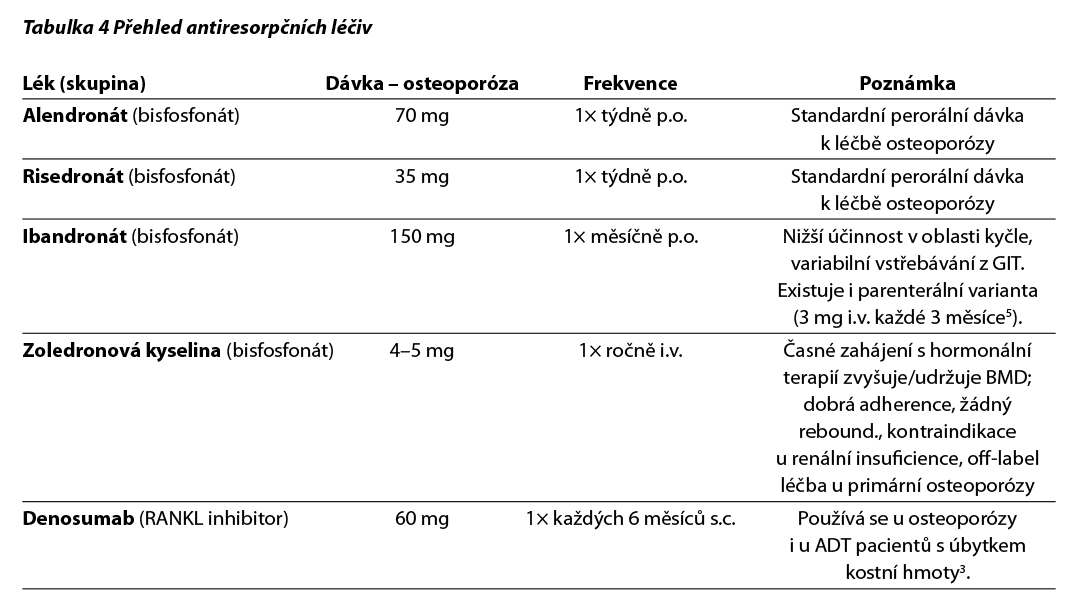
Pro iniciaci zahájení antiresorpční léčby je klíčová správná stratifikace rizika zlomeniny a zhodnocení prognózy pacienta s ohledem na základní onemocnění. Osteoporóza je podobně jako např. hypertenze celoživotní onemocnění vyžadující trvalé sledování a mohou se střídat období aktivní léčba a přerušení. Přehled léčiv je uveden v Tab. 4.
Perorálně užívané bisfosfonáty mají variabilní GI resorpci a riziko nežádoucích GI účinků. Z obou těchto důvodů je nutné dodržovat následující postup užívání:
- užívat nalačno, nejméně 30 minut před prvním ranním jídlem nebo jinými léky, zapít pouze čistou vodou v dostatečném množství
- po užití minimálně 60 minut nelehat z důvodu možné iritace sliznic, tabletu necumlat, nepřevalovat v ústech, nedrtit
Specifickou situací je adjuvantní podávání bisfosfonátů u pacientek s časným, rizikovým karcinomem prsu, kde antiresorpční léčba zoledronátem má protinádorový a zároveň antiosteoporotický přínos (viz kapitoly Farmakoterapie kostní nádorové nemoci a Zhoubný novotvar prsu).
Komplikace antiresorpční léčby
Mezi závažné komplikace dlouhodobé antiresorpční léčby patří osteonekróza čelisti (ONJ, viz kapitola Farmakoterapie kostní nádorové nemoci), atypická zlomenina femuru (AFF) a re-bound fenomén při vysazení denosumabu. AFF je vzácnou avšak závažnou komplikací antiresorpční léčby, projevuje se bolestí ve stehně nebo třísle bez předchozího traumatu, má nezvyklou lokalizaci (subtrochanterická, diafyzární) je charakterizována obvykle příčnou lomnou linií s ostrým odlomením. Riziková léčba pro AFF je léčba BSF či Dmab nad 3 roky (7–10 a více). Při přerušení léčby se riziko AFF do 2 let minimalizuje (lékové prázdniny).
Rebound fenomén se týká pouze denosumabu a projevuje se jako akcelerace kostního obratu, opětovnou a rychlou ztrátou BMD s mnohočetnými vertebrálními zlomeninami. Z tohoto důvodu je vždy nutné při vysazení Dmab pokračovat terapií BSF, ideálně Zoledronát 4–5 mg i.v. 6 měsíců po poslední dávce Dmab.
Literatura:
- PEREZ EA, M. S, Durling FC, WEILBAECHER K. Aromatase Inhibitors and Bone Loss. Oncology (Williston Park). srpen 2006;20(9):1029–48.
- Rada R. Osteologický bulletin. Dostupné na https://smos.cz/wp-content/uploads/2019/11/osteologicky_bulletin_2017_04.pdf
- Lee CE, Leslie WD, Czaykowski P, Gingerich J, Geirnaert M, Lau YKJ. A comprehensive bone-health management approach for men with prostate cancer
receiving androgen deprivation therapy. Curr Oncol. srpen 2011;18(4):e163–72. - Coleman R, Hadji P, Body JJ, Santini D, Chow E, Terpos E, et al. Bone health in cancer: ESMO Clinical Practice Guidelines†. Annals of Oncology. 1. prosinec
2020;31(12):1650–63. - Compston J, Cooper A, Cooper C, Gittoes N, Gregson C, Harvey N, et al. UK clinical guideline for the prevention and treatment of osteoporosis. Arch Osteoporos.
2017;12(1):43.
