Léčba primárních kostních nádorů je vedena vždy na základě rozhodnutí multioborového týmu (MDT, ortoped, hrudní chirurg, příp. cévní, plastický chirurg, radiodiagnostik, intervenční radiolog, klinický/dětský onkolog, radiační onkolog, patolog, psycholog) s dostatečnými zkušenostmi s léčbou těchto nádorů. Vhodné je zařazení těchto pacientů k léčbě v rámci probíhajících mezinárodních klinických studií. Protokoly pro léčbu konvenčního osteosarkomu a Ewingova sarkomu nelze na tomto místě zjednodušit, nutno vycházet z originálních textů protokolů klinických studií (zmíněny pouze základní režimy). Léčba chordomu, obrovskobuněčného kostního nádoru či adamantinomu je nad rámec kapitoly.
Volba léčebné strategie závisí na lokalizaci a rozsahu primárního nádoru, operabilitě, histologickém subtypu, přítomnosti vzdálených metastáz, celkovém stavu pacienta, přítomnosti komorbidit, věku a preferencích pacienta. Základní modalitou je léčba chirurgická, doplněná léčbou systémovou dle histologie. Radioterapie má postavení metody doplňkové.
V případě relapsu je prioritou dosažení chirurgické remise.
10.1 Konvenční osteosarkom
- neoadjuvantní chemoterapie – HD methotrexát, cisplatina, doxorubicin (MAP,„EURAMOS1“), při riziku podání MTX (věk, interkurence) pouze kombinace AP, AP-I, restaging, chirurgický výkon a
- adjuvantní chemoterapie – MAP ± mifamurtid*,
- pacienti vyššího věku mohou profitovat z primárně chirurgického výkonu s následnou adjuvantní chemoterapií.
2. linie – není jasně definována, individuální přístup dle předléčení, EFS, PS, lokalizace a počtu metastáz (ifosfamid/etoposid, cyklofosfamid/etoposid, cyklofosfamid/topotekan, gemcitabin, gemcitabin/docetaxel, sorafenib, regorafenib, cabozantinib, HD ifosfamid, ifosfamid/karboplatina/± etoposid, bisfosfonáty, samarium).

10.2 High grade vřetenobuněčné/nediferencované pleiomorfní kostní sarkomy)
- neoadjuvantní chemoterapie – dle MDT – doxorubicin/cisplatina,
- adjuvantní chemoterapie možná – doxorubicin/cisplatina,
- paliativní chemoterapie – obecně režimy pro osteogenní sarkom.
10.3 Chondrosarkom
- adjuvantní chemoterapii kombinovanou na bázi antracyklinu lze zvážit (není standard) u dediferencovaného typu chondrosarkomu, neoadjuvantní/adjuvantní u mesenchymálního typu chondrosarkomu, v ostatních případech není indikována,
- paliativní chemoterapie při klinickém stadiu IV je možná (doxorubicin, cisplatina, ifosfamid, gemcitabin/docetaxel, pazopanib, inhibitor IDH1 dle NGS).
10.4 Nádory skupiny Ewingova sarkomu (i mimokostní)
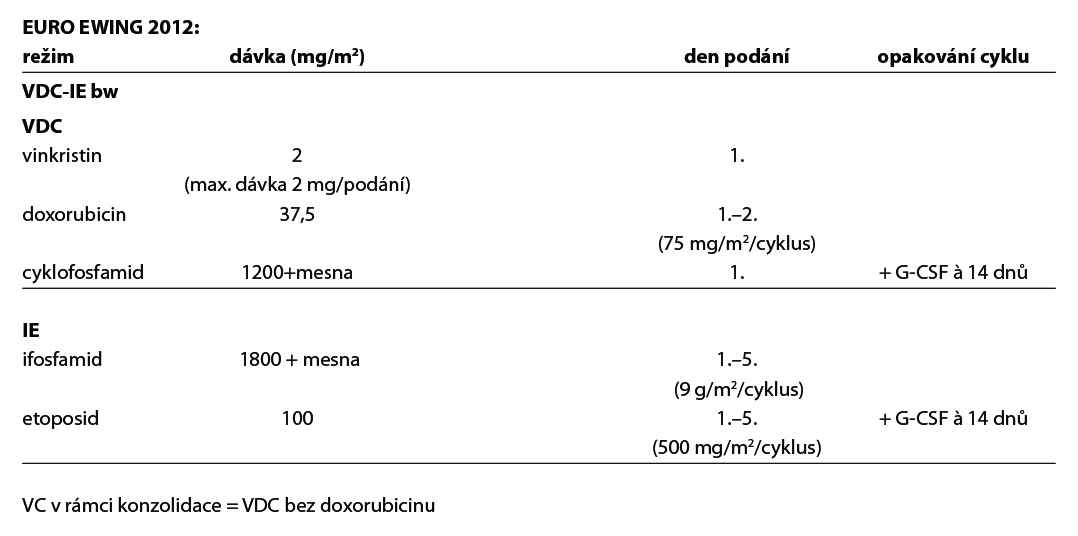
- indukční chemoterapie – režim VDC-IE a 2 týdny (protokol Euro Ewing 2012), restaging, lokální léčba a
- konzolidační chemoterapie – režim IE/VC a 2 týdny, RT pouze v indikovaných případech, HD chemoterapie busulfan/ melfalan nebo treosulfan/melfalan s auto PBSC pouze v indikovaných případech a to jako konzolidace CR u high risk, M0, poor responderů.
2. linie – individuální přístup: topotekan/cyklofosfamid, HD ifosfamid, karboplatina/etoposid (případně: docetaxel/gemcitabin, irinotekan/temozolomid, cabozantinib), bisfosfonáty.
10.4.1 Kulatobuněčné (Ewing like) sarkomy
U raritní podskupiny kulatobuněčných sarkomů (s EWSR1-non ETS fuzí, CIC-DUX, BCOR rearanž…) v současné době neexistuje jednoznačné doporučení, zda tyto nádory léčit jako Ewingův sarkom či jako HG sarkomy měkkých tkání jako takové.
10.5 Vybrané informace k preparátu mifamurtide* (liposomální muramyl tripeptid):
Tomuto přípravku byl přiznán statut „orphan drug“. MEPACT je indikován dle SPC u pacientů ve věku od 2 do 30 let pro léčbu resekovatelného osteosarkomu vysokého stupně bez metastáz po makroskopicky kompletní chirurgické resekci v kombinaci s pooperační chemoterapií.
Doporučená dávka mifamurtidu pro všechny pacienty je 2 mg/m2 tělesného povrchu. Tato dávka by měla být podávána jako adjuvantní léčba následující po resekci: dvakrát týdně s pauzou nejméně 3 dny po dobu 12 týdnů a dále jedenkrát týdně po dalších 24 týdnů, takže celkové podané množství je 48 infuzí za 36 týdnů.
Červeně jsou označeny léky, které nemají k 1. 3. 2024 stanovenu úhradu ze zdravotního pojištění pro léčbu kostních
sarkomů. (vyjma úhrady některých z nich na základě Dohody mezi ČOS a pouze ZP 111). Indikace ostatních moderních
preparátů je podmíněna splněním pravidel úhrady dle SÚKL (www.sukl.cz).
Sledování po léčbě: je doporučeno individualizovat v závislosti na míře rizika relapsu v korelaci s histologickým subtypem, charakterem a efektem proběhlé léčby (klinické vyšetření, zobrazovací metoda primárního tumoru a plic u LG sarkomů a 4–6 měsíců do 5 let, u HG sarkomů a 3–4 měsíce do 3 let, poté 2× ročně, po 6 letech ročně, další vyšetření při klinické indikaci).
Literatura:
- NCCN Clinical Practise Guidlines in Oncology, Bone Cancer, V 1/2024, www.nccn.org.
- Strauss S J, Frezza A M, Abecassis N et al.: Bone sarcomas: ESMO-EURACAN-GENTURIS-ERNPaedCan Clinical Practice Guideline for diagnosis, treatment and
follow-up. Ann Oncol. 2021 Sep 1;S0923-7534(21)04280-0. doi: 10.1016/j.annonc.2021.08.1995. - Ferrari S, Bielack SS, Smeland S et al. EURO-B.O.S.S.: a European study on chemotherapy in bone-sarcoma patients aged over 40: outcome in primary highgrade
osteosarcoma. Tumori 2018; 104: 30–36. - Piperno-Neumann S, Ray-Coquard I, Occean BV et al. Results of API-AI based regimen in osteosarcoma adult patients included in the French OS2006/Sarcome-
09 study. Int J Cancer. 2020; 146 (2): 413-423. - Longhi A, Bielack SS, Grimer R et al. Extraskeletal osteosarcoma: A European Musculoskeletal Oncology Society study on 266 patients. Eur J Cancer. 2017;
74: 9-16. - Chow W, Frankel P, Ruel C, et al. Results of a prospective phase 2 study of pazopanib in patients with surgically unresectable or metastatic chondrosarcoma.
Cancer. 2020 Jan 1;126(1):105-111 - Tap WD, Villalobos VM, Cote GM, et al. Phase I study of the mutant IDH1 inhibitor ivosidenib: safety and clinical activity in patients with advanced chondrosarcoma.
J Clin Oncol 2020;38:1693-1701. - Brennan B, Kirton L, Marec-Bérard P et al.: Comparison of two chemotherapy regimens in patients with newly diagnosed Ewing sarcoma (EE2012): an
open-label, randomised, phase 3 trial. Lancet. 2022 Oct 29;400(10362):1513-1521. - McCabe MG, Kirton L, Khan M, et al. Results of the second interim assessment of rEECur, an international randomized controlled trial of chemotherapy for
the treatment of recurrent and primary refractory Ewing sarcoma (RR-ES). J Clin Oncol. 2020, 38, 15_suppl, 11502-11502. - Italiano A, Mir O, Mathoulin-Pelissier S, et al. Cabozantinib in patients with advanced Ewing sarcoma or osteosarcoma (CABONE): a multicentre, single-
arm, phase 2 trial. Lancet Oncol. 2020 Mar;21(3):446-455. - Marabelle A, Fakih M, Lopez J, et al. Association of tumour mutational burden with outcomes in patients with advanced solid tumours treated with pembrolizumab:
prospective biomarker analysis of the multicohort, open-label, phase 2 KEYNOTE-158 study. Lancet Oncol 2020;21:1353-1365 - Atta S, Bolejack V, Ganjoo K et al. A Phase II trial of regorafenib in patients with advanced Ewing sarcoma and related tumors of soft tissue and bone:
SARC024 trial results. Cancer Med 2023, 12, 1532-1539. - Locquet, MA., Brahmi, M., Blay, JY. et al. Radiotherapy in bone sarcoma: the quest for better treatment option. BMC Cancer 23, 742 (2023). https://doi.
org/10.1186/s12885-023-11232-3.





