30.1 Kostní nádorová nemoc
Skelet je jedním z nejčastějších míst nádorové diseminace. Kostní metastázy jsou zdrojem závažné morbidity: způsobují bolest, omezují hybnost a snižují celkovou kvalitu života. Mohou vést k patologickým frakturám, syndromu míšní komprese a hyperkalcémii. Kromě modalit protinádorové léčby využíváme v léčbě kostních metastáz také léky ovlivňující metabolismus kostí (bone modifying agents – BMA), které jsou součástí komplexní paliativní léčby kostní nádorové choroby. Vedou k redukci komplikací nádorového postižení skeletu (tzv. skeletal related events – SRE), mezi které řadíme vznik patologické fraktury, míšní kompresi, nutnost paliativní radioterapie, nutnost operačního řešení kostí metastázy; někdy je sem řazena i nádorová hyperkalcémie. Pro hodnocení účinnosti BMA je tedy určující prevence nebo oddálení vzniku SRE. Vliv užívání BMA na celkovou délku přežití je předmětem intenzivního výzkumu.
30.2 Léčba kostní nádorové choroby
K léčbě kostní nádorové choroby jsou v ČR dostupné tyto BMA (bone modifying agents – léky ovlivňující metabolismus kosti):
• bisfosfonáty (BF): ibandronát (IBA), klodronát (KLO), pamidronát (PÁM) a zoledronát (ZOL)
• monoklonální protilátka: denosumab (DMAB)
Efektivita BMA u jednotlivých typů nádorů
30.2.1 Karcinom prsu
Na základě metaanalýzy Cochrane Review3 BF obecně snižují u pacientek s metastatickým postižením skeletu riziko vzniku SRE o 17 %, pokud vyloučíme z posuzovaných parametrů hyperkalcémii, dochází ke snížení ostatních SRE o 15 %. Perorální BF snižují riziko SRE o 16 %, parenterální BF o 17 %. Snížení relativního rizika vzniku SRE ve srovnání s placebem
pro jednotlivé BF je následující: ZOL: 41 %, PAM 23 %, IBA i.v.: 20 %, IBA p.o.: 14 %; KLO p.o.: 15 %, u všech statisticky významně kromě IBA p.o. Statisticky a klinicky významný efekt na bolest skeletu byl prokázán u všech BF. Srovnání ZOL a PAM ukazuje 20 % redukci relativního rizika SRE ve prospěch ZOL.
Monoklonální protilátka DMAB snižuje riziko SRE ve srovnání se ZOL o dalších 18 %–26 % (v závislosti na typu SRE), snižuje průměrnou kostní morbiditu o 22 % (p = 0,0041), vyžaduje přechod na silné opiáty u nižšího procenta pacientek ve srovnání se ZOL a vede ke zlepšení kvality života u vyššího procenta pacientek ve srovnání se ZOL.
Na základě publikovaných dat mají z léčby BMA prospěch všechny pacientky s metastatickým postižením skeletu prokázaným na RTG bez ohledu na přítomnost symptomů. Pozitivní nález na scintigrafii skeletu bez odpovídajícího korelátu na RTG, resp. CT vyšetření není indikací k zahájení léčby BMA.
30.2.2 Karcinom prostaty
BMA obecně snižují riziko SRE a vedou ke zmírnění kostní bolesti. Ve studii srovnávající ZOL s placebem bylo prokázáno snížení rizika SRE z 49 % na 38 % (redukce o 11 %) a objevení prvního SRE se oddálilo o více než 5 měsíců. Na základě publikovaných dat se jako nejúčinnější bisfosfonát v redukci rizika SRE u nádoru prostaty jeví ZOL. V menší randomizované studii u pacientů s metastatickým karcinomem prostaty léčených hormonální terapií bylo přidání klodronátu v dávce 2080 mg p.o. spojeno s významným prodloužením 5 letého přežití (30 % vs. 21 %), nicméně další studie s jinými BF tyto výsledky nepotvrdili.
DMAB v přímém srovnání se ZOL ve studii fáze III snížil riziko první SRE o 18 %, p = 0,008 a prodloužil čas do vzniku SRE o 3,6 měsíce.
30.2.3 Bronchogenní karcinom
V jediné publikované studii fáze III, která zahrnovala více diagnóz se solidními nádory, bylo v podskupině pacientů s plicním karcinomem a metastatickým postižením skeletu aplikací ZOL sníženo relativní riziko SRE o 27 % (při zahrnutí i hyperkalcémie o 29 %). Účinnost ostatních BF nebyla v rozsáhlejších studiích u pacientů s bronchogenním karcinomem testována.
DMAB ve srovnání se ZOL ve studiích s různými solidními tumory nebo mnohočetným myelomem, v podskupině pacientů s plicním karcinomem snížil riziko SRE o 16 %, ale ne signifikantně. V této studii bylo u denosumabu ve srovnání se ZOL v podskupině pacientů s plicním karcinomem prokázáno prodloužení celkového přežití o 1,2 měsíce (8,9, vs. 7,7 měsíce, p = 0,01) a ve skupině pacientů s NSCLC o 1,4 měsíce (9,5 vs. 8,1 měsíce, p = 0,0104)
30.2.4 Ostatní solidní tumory
Jsou dostupná data ze studií se solidními nádory, kde byly zahrnuty diagnózy karcinom ledviny, karcinom hlavy a krku, plicní karcinom, karcinom štítné žlázy a jiné) a ZOL oproti placebu redukovala riziko vzniku SRE o 31 % a prodloužila čas do vzniku prvé SRE.
Efektivita DMAB byla srovnávána se ZOL ve studii fáze III12 zahrnující pacienty s jinými solidními nádory než karcinom prsu nebo prostaty. Monoklonální protilátka DMAB ve srovnání se ZOL oddálila vznik první SRE o 6 měsíců (21,4 vs. 15,4 měsíce) a o 19 % snížila riziko první SRE (p = 0,034). Riziko první a další SRE snížil DMAB ve srovnání se ZOL o 15 %, p = 0,048.
30.3 Aplikační forma
BMA jsou k dispozici ve formě tablet k perorálnímu užití (KLO, IBA), intravenóznímu užití (KLO, PAM, IBA, ZOL) nebo k subkutánnímu (DMAB). Při dlouhodobé léčbě nádorové kostní nemoci je klíčově důležitá kompliance pacientů k léčbě. Při léčbě BMA se jedná o cílovou skupinu pokročile onkologicky nemocných, kteří často trpí zažívacími potížemi různého druhu. Praktické aspekty perorální léčby (velikost tablet, užívání nalačno a povinný interval do nejbližšího jídla, stejně tak GIT nežádoucí účinky – dyspepsie a průjmy) mohou pro některé pacienty představovat závažný problém. V mezinárodních doporučených postupech je u BF upřednostňováno podání parenterální před perorálním. Při léčbě hyperkalcémie je jednoznačně indikované intravenózní nebo subkutánní podání. Perorální formy by měly být voleny u pacientů, kteří jim sami dávají předost a pro které je zatěžující pravidelné docházení do nemocnice. Dobrá informovanost, postoj lékaře
a jeho schopnost vyjít vstříc požadavkům pacienta a zapojit jej do rozhodování o léčebném postupu jsou hlavními body, které přispívají k dobré spolupráci. Doporučené dávkování BMA v léčbě kostní nádorové choroby uvádí tab. č. 1.

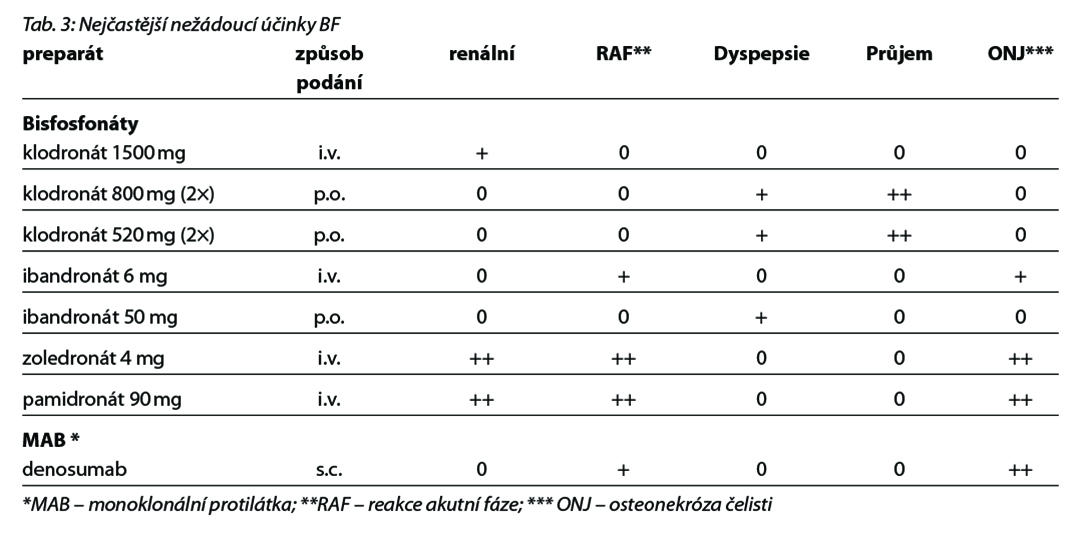
30.4 Nežádoucí účinky
BMA jsou obecně poměrně dobře snášeny. Přesto se při jejich užívání mohou vyskytnout některé klinicky významné nežádoucí účinky. Patří mezi ně renální toxicita, symptomy reakce akutní fáze, gastrointestinální symptomy, hypokalcémie a osteonekróza čelisti.
30.4.1 Renální toxicita
30.4.1.1 Bisfosfonáty
U perorálních BF klinicky významná renální toxicita nebyla popsána. Toxicita intravenózních BF závisí na druhu, dávce, rychlosti a frekvenci podání. Snížení dávky a zpomalení rychlosti aplikace snižuje akutní toxicitu, prodloužení intervalu mezi jednotlivými aplikacemi snižuje chronickou toxicitu. U pacientek léčených IBA se významná renální toxicita nevyskytla. Tabulka č. 2 uvádí doporučenou redukci dávek nebo úpravu rychlosti aplikace BMA při zhoršení renálních parametrů.
U zoledronátu a pamidronátu se doporučuje kontrola renálních funkcí před zahájením léčby a před každou aplikací. U ibandronátu je vhodná kontrola renálních funkcí na začátku léčby; průběžné kontroly před jednotlivými aplikacemi nejsou nutné.
30.4.1.2 Denosumab
Denosumab není vylučován ledvinami, proto při jeho podávání není nutné monitorovat renální funkce ani upravovat dávku v závislosti na clearance kreatininu.

30.4.2 Reakce akutní fáze
Souhrnné označení „reakce akutní fáze“ zahrnuje celou řadu symptomů podobných chřipce: subfebrilie až febrilie, leukocytóza, svalová a kostní bolest, pocit únavy a vyčerpání.
Tato reakce se vyskytuje pouze po parenterálně podaných dusíkatých BF (PAM, ZOL, IBA), nejčastěji po aplikaci první dávky.
Při opakovaném podání se vyskytuje výjimečně. Symptomy většinou odeznívají do 48 hod. a obvykle dobře reagují na nesteroidní antiflogistika. Frekvence tohoto syndromu je u BF v rozmezí 20–30 %, u denosumabu se vyskytla u 8,7 %.
30.4.3 Nežádoucí účinky na GIT
Při perorálním podání BF se mohou vyskytnout pocity břišního diskomfortu, flatulence a průjmy, vzácněji ulcerace jícnu, žaludku a tlustého střeva. Absorpce BF je výrazně snížena při současnému příjmu tekutin a potravy. Proto je nutné BF užívat nalačno (nebo minimálně 2 hodiny po jídle), zapíjet dostatečným množstvím vody (150–250 ml) a stravu přijímat nejdřív za 30–60 minut (v závislosti na volbě preparátu). Z publikovaných studií vyplývá, že klinicky významné GIT nežádoucí účinky (především průjem) se vyskytují v 3–10 % při léčbě klodronátem a v < 7 % při léčbě ibandronátem.
30.4.4 Osteonekróza čelisti (ONJ)
Incidence kolísá v závislosti na léčené populaci v rozmezí 1–10 % (častější u mnohočetného myelomu než u ostatních solidních nádorů), na použitém BMA (častější u DMAB a ZOL než u PAM) a na délce užívání BMA. Uvedená čísla je třeba interpretovat uvážlivě vzhledem k velmi rozdílnému počtu pacientů léčených jednotlivými preparáty. Osteonekrózu čelisti je třeba považovat za nežádoucí účinek celé skupiny BMA (BF s obsahem dusíku – PAM, ZOL, IBA i monoklonální protilátky DMAB) a u všech léčených pacientů je třeba dodržovat doporučená profylaktická opatření. Před zahájením léčby BMA by mělo předcházet stomatologické vyšetření a je vhodné provádět pravidelné kontroly.
30.4.5 Hypokalcémie
Všechny BMA mohou vést k vzniku hypokalcémie. Před zahájením léčby je třeba upravit preexistující hypokalcémii a hladinu kalcia je třeba v průběhu léčby kontrolovat. Při léčbě DMAB je riziko hypokalcémie vyšší než při léčbě ZOL, rizikový jsou zejména pacienti s renální insuficienci. Současně s podáváním BMA je doporučováno podávat kalcium (500 mg–1 g/d) a vitamin D3 (400–800 IU/ den).
30.5 Zahájení a trvání léčby
Podání BMA by mělo být u výše uvedených typů nádorů zahájeno bezprostředně po zjištění metastatického postižení skeletu na RTG nebo CT. Riziko nových SRE je prakticky trvalé, proto se doporučuje v léčbě pokračovat i při výskytu SRE. U pacientů s pokročilým onemocněním s limitovanou prognózou přežití je třeba zvažovat, zda je redukce SRE relevantním cílem s ohledem na celkové cíle léčby a péče. Aplikace BMA v této indikaci neprodlužuje přežití pacientů. Optimální délka léčby není stanovena. Ve většině klinických studií s BP byla léčba zkoumána po dobu 2 let. V individuálních případech je možné v léčbě pokračovat delší dobu. Několik studií potvrdilo srovnatelnou účinnost zoledronátu při 12týdenním a 4týdenním intervalu podávání. Lze konstatovat, že režim s 12týdenní aplikací ZOL je stejně účinný a o něco méně toxický než 4týdenní režim a vzhledem k výhodnějšímu režimu aplikace z hlediska pacienta i poskytovatele péče, ho lze doporučit. 4týdenní režim je vhodné použít u pacientů s velkým rozsahem kostního postižení, hrozící skeletální příhodou nebo v případě hyperkalcémie hyperkalcémie, alespoň na začátku léčby. Objevují se iniciálně data, že 12týdenní interval i v případě denosumabu prokazuje srovnatelné výsledky, nicméně na definitivní zhodnocení je potřeba vyčkat na výsledky
studií s adekvátním počtem pacientů. Rutinní vyšetřování markerů kostního metabolismu se pro hodnocení léčebné odpovědi nedoporučuje. Ukončit léčbu je třeba v případě zhoršení celkového stavu pacienta.
30.6 Zásady terapie kostní nádorové nemoci
• Optimální řešení kostních metastáz vyžaduje multidisciplinární tým
• Terapie BMA by měla být zahájena u všech pacientů s kostními metastázemi
• BMA oddalují vznik skeletálních příhod, snižují bolest a zlepšují kvalitu života
• Zoledronová kyselina je nejúčinnějším bisfosfonátem, je doporučován režim aplikace každých 12 týdnů
• Denosumab je účinnější než zoledronová kyselina v prevenci SRE
• Před zahájením terapie BMA je vhodná stomatologická kontrola
• Současně s podáváním BMA se doporučuje podávat kalcium a vitamin D3
• Terapie BMA se ukončuje při výrazném zhoršení stavu pacienta nebo při významné toxicitě
Literatura:
- Rosen, L.S., Gordon, D., Kaminski, M. et al.: Long term effi cacy and safety of zoledronic acid compared with pamidronate disodium in the treatment of skeletal
complicationsin patients with advanced multiple myeloma or breast carcinoma: a randomised, double blind, multicenter, comparative trial. Cancer
2003; 98: 1735-1744. - Stopeck, A.T., Lipton, A., Body, J.J., Steger, G.G., Tonkin, K., De Boer, R.H. et al. (2010a) Denosumab compared with zoledronic acid for the treatment of bone
metastases in patients with advanced breast cancer: A randomized, double-blind study. J ClinOncol 28: 5132-5139. - Saad, F., Gleason, D.M., Murray, R. et al. Long term effi cacy of zoledronic acid for the prevention of skeletal complications in patients with metastatic hormone
refractory prostate cancer. J Natl Cancer Inst 2004; 96: 879-882. - Yuen, K.K., Shelley, M., Sze, W.M. et al. Bisphosphonates for advanced prostate cancer. Cochrane Database Syst Rev 2006; Oct 18; (4), 4-19.
- Fizazi, K., Carducci, M., Smith, M., Damiao, R.,Brown, J., Karsh, L. et al. (2011) Denosumab versus zoledronic acid for treatment of bone metastases in men
with castration-resistant prostate cancer: A randomised, double-blind study. Lancet 377: 813-822. - Rosen, L.S., Gordon, D., Tchekmedyian, S. et al. Long term efficacy and safety of zoledronic acid in the treatment of skeletal metastases in patients with
NSCLC and other solid tumors: a randomised, phase III, double blind, placebo controlled trial. Cancer 2004; 100: 2613-2621. - Durie, B.M.G., Katz, M., Crowley, J. Osteonecrosis of the jaw and bisphosphonates. N Eng J Med 2005; 23: 8580-8587.
- Clemons MJ, Ong M, Stober C, et al. A randomized trial comparing four-weekly versus 12-weekly administration of bone-targeted agents (denosumab,
zoledronate, or pamidronate) in patients with bone metastases from either breast or castration-resistant prostate cancer. Journal of Clinical Oncology 37,
no. 15_suppl (May 20, 2019) 11501-11501.





