31.1 Úvod
Indikace k nutriční podpoře onkologických pacientů vycházejí z platných standardů Evropské společnosti pro parenterální a enterální výživu (ESPEN), publikovaných v roce 2021 pod titulem „ESPEN practical guideline: Clinical Nutrition in Cancer“.
• Nutriční podpora je integrální součástí komplexní onkologické léčby.
• V zájmu včasného rozpoznání rizika podvýživy je doporučeno u většiny onkologických pacientů provádět nutriční rizikový screening, a to již v době stanovení diagnózy nádorového onemocnění, optimálně pomocí zavedeného standardního hodnocení.
• Nutriční podpora je pak poskytována nemocným s významným rizikem vzniku malnutrice nebo s rizikem prohloubení již přítomné podvýživy, a to systematicky, v mnoha případech po většinu doby protinádorové léčby.
31.2 Diagnostika nutričního rizika (nutriční screening)
Pro zjištění nutričního rizika je možno využít některé z publikovaných nástrojů (testů) pro nutriční screening. Podle jejich složitosti a personálních možností pracoviště lze využít buď jednodušší nástroje (1.stupeň screeningu), nebo složitější (2.stupeň), optimálně však obojí (Tab. 31.1).
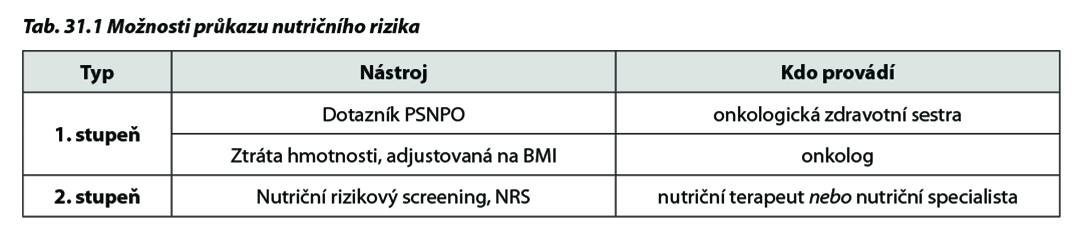
Cílem nutričního screeningu je zjistit u jednotlivých pacientů zvýšené riziko podvýživy, ale také dokumentovat základní vstupní nutriční parametry (za účelem pozdější kontroly). Systematické provádění nutričního screeningu by mělo být spojeno se spolehlivým zvážením pacienta a v mnoha případech také se změřením tělesné výšky, spolu se stanovením aktuálního indexu tělesné hmotnosti, BMI. Dokumentována by měla být i původní tělesná hmotnost, před začátkem hubnutí, jakož i doba hubnutí.
Spolehlivé zjištění aktuální tělesné hmotnosti a výšky je potřebné i pro stanovení dávky léků při protinádorové terapii.
31.2.1 Dotazník PSNPO, pro primární orientační screening
Dle PSNPO při ČOS je v 1. stupni doporučeno rutinní používání Dotazníku PSNPO (Tab. 31.2), který může provádět onkologická zdravotní sestra.

Za nutričně rizikové diagnózy jsou považovány nádory postihující přímo nebo nepřímo zažívací systém, zejména nádory hlavy a krku, nádory v oblasti horního GIT, nádory utlačující zažívací systém (včetně maligního lymfomu), lokálně pokročilý nádor tlustého střeva, nádory s celkovými příznaky (horečky, pocení, úbytek váhy) a většina pokročilých a relabujících nádorů vůbec.
Za nutričně rizikovou léčbu se považuje chemoterapie nebo radioterapie, která může vyvolat závažnou mukozitidu zažívacího traktu, multimodální protinádorová léčba, velká bezprostředně plánovaná operace nádoru, transplantace krvetvorných buněk i jiné typy protinádorové léčby, které mají vysoké riziko omezení příjmu stravy. Dotazník PSNPO, dostupný na stránkách PSNPO, je dokumentem, doporučeným ze strany ČOS a požadovaným zdravotními pojišťovnami jako doklad, opravňující lékaře-onkologa k předpisu přípravků pro sipping s úhradou zdravotní pojišťovnou (za stanovených podmínek).
31.2.2 Ztráta tělesné hmotnosti, adjustovaná na BMI
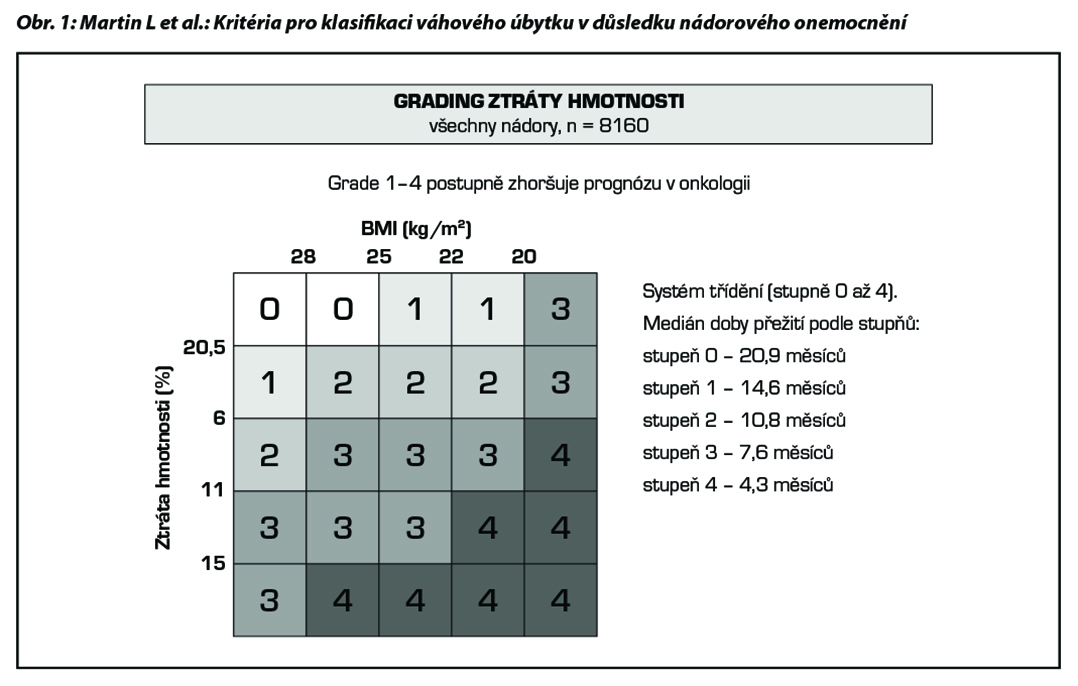
Lze použít také parametr Ztráty tělesné hmotnosti, adjustované na aktuální hodnotu BMI podle Obr. 1. Jedná se o ztrátu hmotnosti za posledních 6–12 měsíců. Výhodou je prognostická informace, nezávislá na typu nádorového onemocnění. Adjustovaná ztráta hmotnosti je zvláště významná, pokud jde o aktuálně pokračující ztrátu, která je provázena sníženým příjmem stravy a snížením fyzické výkonnosti pacienta (slabost, únavnost, zhoršení PS), přičemž nemusí být přítomny všechny tři tyto atributy.
31.2.3 Nutriční rizikový screening kompletní
Optimálním postupem je provedení kompletního NRS (2. stupeň) u nemocných, u nichž bylo v 1. stupni orientačním testem zjištěno zvýšené riziko. Výhodou NRS je odstupňování nutričního rizika ve škále 0–7 bodů. Tato hodnota je zřetelně uvedena v dokumentaci pacienta a onkolog k ní může přihlížet při plánování protinádorové léčby (Tab. 31.3).
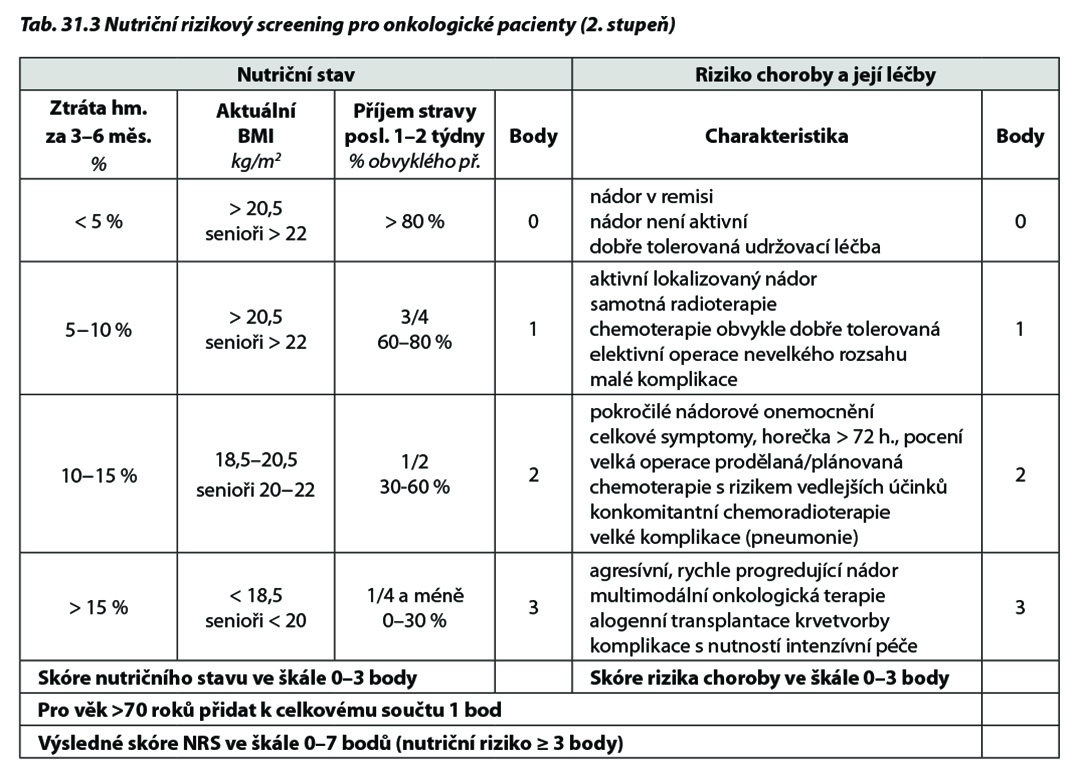
Bodové skóre za obě domény se následně sčítá a u nemocných nad 70 roků se automaticky přičítá 1 bod, který zohledňuje menší nutriční rezervy a významně vyšší riziko podvýživy u seniorů. Výsledkem je celkové skóre NRS ve škále 0–7 bodů, přičemž 3 body a více znamenají přítomnost významného nutričního rizika.
Doména na levé straně tabulky hodnotí nutriční stav pacienta, doména na pravé straně pak riziko vyplývající z typu nádoru, jeho léčby a přítomných komplikací.
Doména nutričního stavu zahrnuje tři základní pilíře hodnocení stavu výživy, jednak již vzniklou ztrátu hmotnosti, dále aktuální BMI a konečně odhad poklesu příjmu stravy, proti obvyklému plnému příjmu pacienta z doby před onemocněním. Skóre této domény (0-3 body) není dáno součtem, ale je určeno podle nejvíce narušeného parametru, přičemž hodnocení je možno posunout o jednu kategorii výše nebo níže podle toho, o jaké hodnoty a jejich kombinaci se jedná (s využitím zkušenosti vyšetřující osoby). Tímto způsobem je v uvedené doméně obsaženo jednoduché hodnocení stupně malnutrice (lehká =1 b., střední = 2 b., těžká = 3 body).
Výsledek kompletního testu NRS, založený v dokumentaci pacienta, poskytuje doklad o vstupních nutričních údajích, umožňuje jejich pozdější kontrolu a současně je vodítkem pro rozhodování o nutričním plánu.

31.3 Diagnóza nádorové kachexie
Nádorová kachexie je charakterizována progresívní pokračující ztrátou hmotnosti a svalové hmoty při aktivním nádorovém onemocnění, která je provázena poruchou metabolismu. Při této poruše mohou, ale nemusí vždy být přítomny známky aberantního systémového zánětu s nádorovou elevací CRP, případně i s poklesem hladiny albuminu v séru. Aberantní zánět je způsobený zvýšenou tvorbou prozánětlivých cytokinů, která současně vede k nechutenství, které je v plně vyjádřené formě označováno jako nádorová anorexie. Porucha metabolismu zahrnuje často také insulinovou rezistenci a způsobuje nedostatečné využití přijímaných živin, takže pacient může ztrácet na hmotnosti i při zachovaném příjmu stravy.
Nádorová kachexie může být diagnostikována už v časné fázi, kdy ztráta činí pouze kolem 5 % původní hmotnosti (diagnóza tedy není založena na přítomnosti extrémní hubenosti).
Z terapeutického hlediska nedostačuje samotné podávání živin v běžném složení k úpravě tohoto stavu, pokud se nepodaří zmírnit poruchu metabolismu. Nejlepším způsobem úpravy metabolismu je účinná protinádorová léčba s potlačením růstu nádoru. K tomu může významně přispívat i nutriční a metabolická intervence, zahrnující omega-3 polynenasycené mastné kyseliny z rybího oleje (n-3 PUFA).
31.3.1 Glasgowské Prognostické Skóre (GPS, Glasgow Prognostic Score)
Je založeno na dvou běžných laboratorních hodnotách, hladinách albuminu a CRP v séru.
Výsledek nabývá hodnot ve škále 0–2 body (CRP > 10 mg/l, albumin < 35 g/l).
Modifikované skóre mGPS je pozitivní pouze při zřetelné nádorové elevaci CRP, při nepřítomnosti infekce (bod za albumin < 35 g/l je přidělen jen při současném CRP > 10 mg/l).
Hodnota mGPS ukazuje na systémový zánět, odráží přítomnost poruchy metabolismu a tím také přítomnost nádorové kachexie (není však podmínkou této diagnózy).
Pozitivní GPS (1–2 body) je nezávislým prognostickým faktorem nádorového onemocnění.
31.4 Cíl nutriční podpory onkologických pacientů
Nutriční podpora by měla být poskytována po delší dobu systematicky a měla by mít stanovené cíle, kterých může být a také je třeba dosáhnout.
31.4.1 Reálné cíle včasné a systematicky prováděné nutriční podpory
• Udržení nebo zlepšení nutričního stavu, zabránit dalšímu hubnutí pacienta
• Podpora svalové hmoty a její funkce (udržení výkonnostního stavu PS)
• Zvýšení protinádorového efektu onkologické léčby – především nepřímo, dodržením celé dávky protinádorové léčby bez odkladů
• Snížení nežádoucích účinků onkologické léčby
• Zlepšení kvality života nemocných.
31.5 Způsoby nutriční podpory onkologického pacienta
Nutriční podpora onkologických pacientů využívá stejných postupů, jako v jiných oborech medicíny, tedy úpravy diety, sippingu, enterální a parenterální výživy (Tab. 31.5).
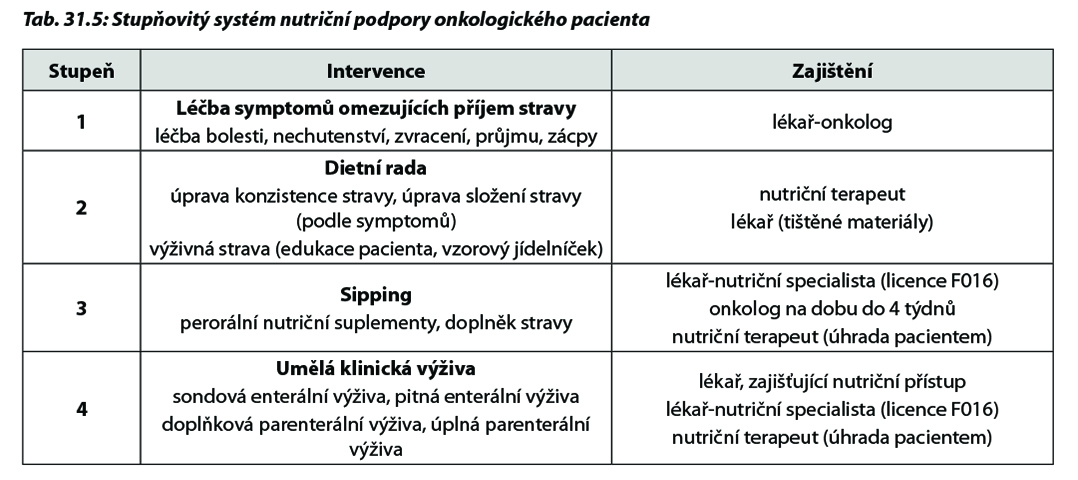
31.5.1 Léčba symptomů, omezujících příjem stravy
Příjem stravy je v mnoha případech omezený různými symptomy nádorového onemocnění a jeho léčby (nutrition impact symptoms). Mezi prvními opatřeními je léčba těchto symptomů, farmakologická i nefarmakologická.
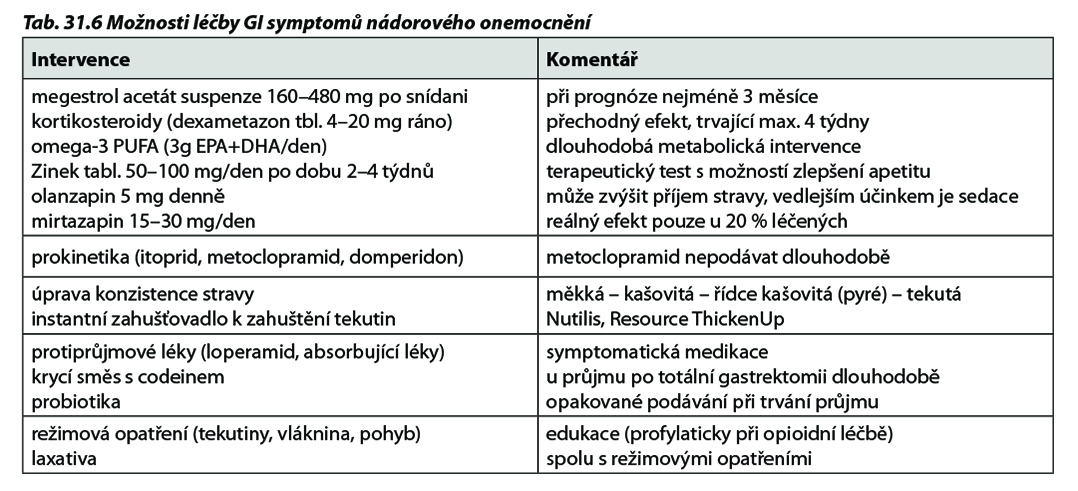
Tab. 31.6 ukazuje některé možnosti zmírnění gastrointestinálních symptomů (GI symptomy).
31.5.2 Sipping
Perorální nutriční suplementy (ONS), užívané formou popíjení (sipping), jsou nejjednodušší formou nutriční podpory. Obvykle jsou indikovány jako doplněk stravy, ke zvýšení příjmu energie, bílkovin a dalších živin, mohou však být indikovány i při plném příjmu stravy, pokud nedostačuje k udržení tělesné hmotnosti. Přednost mají ONS ze skupiny vysokoproteinových,
imunomodulačních s obsahem n-3 PUFA, případně diabetických přípravků s obsahem vlákniny.
Výhodou ONS je vysoký obsah všech mikronutrientů v poměru k obsahu energie.
Užívání ONS by se mělo řídit zásadami efektivního sippingu. Často je vhodnější rychlejší popíjení tak, aby byla snáze dodržena stanovená léčebná dávka.
V jednotlivých případech může popíjení většího množství (> 50 % celkové potřeby energie, je-li tolerováno) ve formě pitné enterální výživy nahradit výživu sondovou.
31.5.3 Nazogastrická sondová výživa
Tekutá enterální výživa (EV), podávaná tenkou sondou (zevní průměr 3 mm), je jednoduchým a efektivním způsobem nutriční podpory, kterým lze krátkodobě (2–4 týdny) překlenout nedostatečný příjem stravy při komplikacích léčby nádorového onemocnění (po selhání perorální nutriční intervence). Může být intervencí, která nastartuje zvýšení příjmu stravy při atrofii střevní sliznice u těžké malnutrice (podporou trávení a vstřebávání živin ve střevě).
31.5.4 Perkutánní endoskopická gastrostomie (PEG)
Profylaktické zavedení PEG před radioterapií (RT) nádoru hlavy a krku by nemělo být indikováno paušálně před každou RT, ale pouze při vysokém riziku těžké dysfágie (plánovaná plná dávka RT na obě strany krku, předcházející dysfágie a malnutrice).
Nevýhodou PEG je delší přetrvávání dysfagických potíží a pozdější obnovení přirozeného příjmu stravy. Kdykoliv je to možné, měl by být pacient s PEG podporován k udržení schopnosti polykat alespoň malé množství stravy, optimálně s péčí logopeda.
Vedle samotného zavedení PEG je nutný předpis adekvátního množství enterální výživy, spolu s řádným poučením pacienta.
Cílem je udržet tělesnou hmotnost po celou dobu léčby. Praxe však ukazuje, že se tento cíl u mnoha léčených nenaplní, z čehož vyplývá potřeba kvalitní edukace a spolupráce pacienta.
31.5.5 Doplňková parenterální výživa (PV)
Doplňková PV může být účinným způsobem nutriční podpory u pacienta s přetrvávajícím nedostatečným příjmem stravy a hubnutím, u něhož je přítomna malabsorpce živin (chronický průjem). Indikována může být tam, kde není proveditelná sondová EV s oligomerním přípravkem, nebo po jejím selhání.
Doplňkovou PV je možno podávat snadno a bezpečně cestou žilního katetru typu PICC, a to i v domácím prostředí. Vzhledem k celkově nižšímu obsahu energie má nižší výskyt komplikací. Déletrvající podávání doplňkové PV může být flexibilní s cílem udržet tělesnou hmotnost, není nutné, aby byla podávána každý den, pokud je hmotnost stabilizovaná.
31.5.6 Úplná parenterální výživa
Při komplikacích, které znemožňují enterální nutriční podporu, je většinou podávána za hospitalizace. U pacientů s pokročilým nádorovým onemocněním může být indikována spíše výjimečně jako domácí ÚPV (DPV) při současném splnění většiny definovaných podmínek:
• afagický pacient s kontraindikací EV (nulový příjem stravy),
• doba očekávaného přežívání alespoň 3 měsíce,
• nádor není rychle progredující (smrt by nastala dříve na podvýživu než na progresi nádoru),
• výkonnostní stav podle Karnofsky indexu je lepší, než 50 (vyjde alespoň jedno poschodí),
• hodnota GPS ≥ 1 signalizuje horší prognózu (svědčí spíše proti DPV).
Příznivý efekt DPV se projeví, pokud je PV podávána nejméně 2 měsíce. V takovém případě může být spojena i s prodloužením přežívání (což však není primárním cílem).
31.6 Zásady pro poskytování nutriční podpory onkologických pacientů
• Podávání většinou paralelně s protinádorovou léčbou.
• Včasné zahájení, dříve, než dojde k nenávratné ztrátě svalové hmoty a tělesných bílkovin.
• Systematické podávání po delší dobu, podle tolerance nutriční podpory.
• Kontrola tolerance a efektu nutriční podpory v pravidelných intervalech.
• Mezi prvními opatřeními je zmírnění symptomů, omezujících příjem stravy (Tab. 31.6)
– zahrnuje i řešení deficitu chrupu nebo podporu polykání při dysfágii (logopedická péče).
• Celková potřeba energie 25–30 kcal/kg/den není vyšší než u neonkologických pacientů.
• Potřeba bílkovin nejméně 1–1,5 g/kg/den.
• Vitamíny a minerální látky by měly být podávány v dávkách přibližně odpovídajících denním doporučeným dávkám pro neonkologické pacienty, pokud není přítomný deficit.
• Alternativní diety bez prokázaného účinku při nádorovém onemocnění nejsou doporučeny
– zatím neexistuje žádná dieta, která by konzistentně vedla k léčbě nádorového onemocnění.
– naopak, alternativní diety zvyšují riziko hubnutí a rozvoje malnutrice.
31.7 Možnosti nutriční a metabolické intervence při nádorovém onemocnění
Nutriční podpora speciálního složení se může stát metabolickou intervencí, jejímž cílem je zmírnit poruchu metabolismu (protizánětlivý efekt, anabolický efekt). Taková podpora začíná již speciálním složením stravy (cancer specific diet) a zahrnuje doplňky stravy a případně i speciální složení EV a PV.
31.7.1 Zvýšený příjem tuků na úkor sacharidů
Porucha metabolismu při nádorové kachexii většinou zahrnuje také insulinovou rezistenci, při níž je doporučeno zvýšit příjem energie ve formě tuku a snížit příjem sacharidů. Tuk jako koncentrovaný zdroj energie tak přispívá k celkovému zvýšení energetického příjmu. Optimální je přitom proporcionální zastoupení tuku živočišného a rostlinného.
Vzhledem ke zvýšené potřebě bílkovin může být pro energetické zastoupení tří hlavních živin vhodný poměr bílkoviny/ sacharidy/tuky 20:40:40.
Ketogenní dieta s minimálním množstvím sacharidů ve stravě není v současné době doporučena, hlavně kvůli špatným chuťovým vlastnostem a riziku poklesu příjmu živin.
31.7.2 Omega-3 polynenasycené mastné kyseliny (n-3 PUFA)
Při přetrvávání aberantního systémového zánětu (CRP>10 mg/l při nepřítomnosti infekce), často spolu s nechutenstvím nebo časnou sytostí, je pro metabolickou intervenci doporučeno podávat zvýšenou dávku n-3 PUFA, především dlouhořetězcových z rybího oleje.
• Metabolicky účinná dávka, vyjádřená součtem obsahu EPA a DHA, je 3 g/den (EPA 2 g/d).
• Lze očekávat mírný protizánětlivý účinek a zlepšení apetitu u nemocných s nechutenstvím.
• Déletrvajícím cílem je stabilizace tělesné hmotnosti a podpora svalové hmoty.
• Optimální je kombinace s protinádorovou terapií.
• Potřebná je delší doba podávání (týdny až měsíce).
• Dodržení denní dávky (vzhledem k omezené toleranci sippingu) vyžaduje přijímat n-3 PUFA nejméně ze dvou zdrojů současně nebo střídavě (ONS s n-3 PUFA klasický typ, džusový typ s n-3 PUFA, kapsle s rybím olejem, tekutý rybí olej, nebo i EV či PV s n-3 PUFA).
Podle ESPEN guideline jde vzhledem k omezeným vědeckým dokladům o slabé doporučení. Efekt může být větší při včasném a déletrvajícím podávání, při kombinaci s chemoterapií a při současném zvýšení příjmu bílkovin a cvičení k podoře svalové hmoty ve formě multimodální intervence.
Nutriční příprava s n-3 PUFA před velkou operací k resekci nádoru horní části GIT však má podle ESPEN silné doporučení, což se týká i pacientů v dobrém nutričním stavu a také nutriční podpory po operaci.
31.7.3 Zajištění příjmu mikronutrientů
Nutriční podpora při nádorovém onemocnění by měla od počátku obsahovat běžné denní doporučené dávky vitamínů a stopových prvků. Pokud nejde o léčbu prokázaného deficitu mikronutrientů, nejsou dnes indikovány zvýšené dávky mikronutrientů.
Výjimkou je těžká malnutrice s předcházejícím déletrvajícím nedostatečným příjmem stravy, kdy lze předpokládat také nedostatečný příjem mikronutrientů. V takovém případě je vhodné krátkodobě podávat multivitamínové přípravky s obsahem běžné nebo i dvojnásobné denní dávky vitamínů, a to i vedle zavedené nutriční podpory.
31.7.4 Úprava prokázaného deficitu jednotlivých mikronutrientů
Suplementace vyšší dávky může být indikována při laboratorním průkazu deficitu jednotlivých vitamínů (zejména vitamínu D) nebo stopových prvků (zinek, selén). Nebylo však prokázáno, že taková léčba ovlivní průběh nádorového onemocnění.
31.7.5 Kombinace nutriční podpory s fyzickou aktivitou
Fyzická aktivita střední intenzity je podle ESPEN při léčbě nádorového onemocnění silně doporučena. Cílem je podpora svalové hmoty, fyzické výkonnosti a příznivé ovlivnění poruchy metabolismu. Střední intenzita odpovídá úrovni 50–75 % maximální srdeční frekvence nebo aerobní kapacity. Doporučena je kombinace aerobního a rezistenčního cvičení po dobu alespoň 10–60 minut 3krát týdně.
Je prokázáno, že fyzická aktivita je proveditelná i při pokročilém nádorovém onemocnění, je přitom dobře tolerována a bezpečná. Pravidelná fyzická aktivita může vést k signifikantnímu zlepšení aerobní kapacity, svalové síly, kvality života, k redukci únavy a úzkosti.
31.8 Nutriční podpora v paliativně symptomatické a terminální fázi
Ukončení protinádorové léčby není důvodem k ukončení nutriční podpory. Pokračování nutriční péče je založeno na individuálním přístupu, zohledňujícím postoj pacienta.
31.8.1 Nutriční péče v paliativně symptomatické fázi
Hlavním cílem se stává udržení nebo i zlepšení kvality života, a to i za cenu, že pacient svým příjmem nenaplní celou potřebu živin. Při nutriční podpoře je třeba vždy posuzovat také zátěž z této samotné intervence. Na druhé straně však deplece bílkovin a svalové hmoty přispívá ke zhoršení kvality života. Přístup je proto individuální, se zohledněním přání pacienta.
31.8.2 Nutriční péče v terminální fázi nádorového onemocnění
V terminální fázi onemocnění (stav pacienta se obvykle zhoršuje z týdne na týden) se nutriční péče řídí komfortem pacienta. Potřeba energie a živin se výrazně snižuje, ve většině případů pacient nepociťuje hlad či žízeň, a to ani při minimálním příjmu stravy a tekutin. Plnou dávku živin již pacient není schopen využít, naopak, nucený příjem stravy může být zatěžující. Někteří nemocní pak preferují velmi malé množství sippingu (1–2 lahvičky denně) před příjmem přirozené stravy. Mírná dehydratace může být výhodou, s výjimkou náhlého stavu zmatenosti, který může být způsobený dehydratací a může pak příznivě odpovědět na šetrné zvýšení příjmu tekutin.
31.9 Komplikace nutriční podpory
Podávání nutriční podpory může vést samo o sobě ke vzniku komplikací. Může jít o mechanické komplikace při zavádění nutričního přístupu (PV i EV), infekční komplikace, gastrointestinální intoleranci EV a také o metabolické komplikace (PV i EV).
Mezi nejčastější metabolické komplikace patří:
• hyperglykémie, která je často spojena se zvýšeným výskytem infekční komplikací,
• iontové dysbalance, spojené s nedostatečným nebo nadměrným přívodem minerálních látek,
• refeeding syndrom, RFS (náhlé obnovení výživy po předchozím hladovění),
• overfeeding syndrom (relativní nadbytek živin při stresovém metabolismu v intenzívní péči)
– může vzniknout i při správném výpočtu celkové potřeby energie, pokud není zohledněna mobilizace vlastních živin (ze zásob a metabolické tvorby).
31.9.1 Prevence refeeding syndromu
Riziko vzniku RFS je vysoké u nemocných s předcházejícím nedostatečným příjmem stravy (nejméně 5-10 dnů předem), zejména při zvracení nebo dysfgágii a při současné malnutrici s nízkou hodnotou BMI, pokud je náhle obnovena výživa formou nutriční podpory (typickou situací je zavedení PEG).
V diagnostice se uplatňují především laboratorní hodnoty (hypofosfatémie, hypokalémie, hypomagnezémie). Předpokládat je třeba také nedostatek vitamínů skupiny B.
Prevence zahrnuje zahájení výživy nízkou dávkou energie s postupným zvyšováním dávky.
Je třeba monitorovat hladiny elektrolytů, zejména fosforu, spolu s jeho včasnou suplementací. Indikováno je podání vysoké dávky thiaminu kolem 200 mg i.v. denně a zvýšené dávky komplexu vitamínu B (B-komplex forte 2-2-2) v prvních dnech nutriční podpory.
31.10 Organizační zajištění nutriční péče v nemocnici a na ambulanci
Aktivně prováděná a dobře zajištěná rutinní nutriční péče se promítá do viditelných výstupů:
• Je zavedený nutriční screening (i když nemusí být prováděn u všech nemocných).
• Všichni pacienti jsou spolehlivě váženi (nestačí anamnestické zjištění hmotnosti).
• Většina pacientů má vstupně změřenou tělesnou výšku a stanovenu hodnotu BMI.
• Laboratorní monitorování (albumin, prealbumin, CRP, ionty včetně P, Zn, vitamín D).
• U nemocných s nutričním rizikem je orientačně sledován příjem stravy (čtvrtiny, %).
• Edukace nemocných o výživné stravě, tištěné materiály.
• Systematická nutriční podpora formou sippingu pacientů s neúplným příjmem stravy
– rozlišování a volba přípravků podle jejich složení; dávkování sippingu,
– hodnocení efektu sippingu.
• Dostupnost enterální a parenterální výživy, včetně domácí.
• Spolupráce s nutričním terapeutem.
• Spolupráce s nutriční ambulancí.
31.10.1 Nutriční ambulance
Pro pacienty s vysokým nutričním rizikem (NRS ≥ 4 body) by měla být dostupná nutriční ambulance, přinejmenším ve všech velkých centrech a téměř ve všech nemocnicích, pokud léčí pacienty s nutričním rizikem. Nutriční ambulance má v mnoha ohledech nezastupitelný způsob specializované péče (Tab. 31.7).
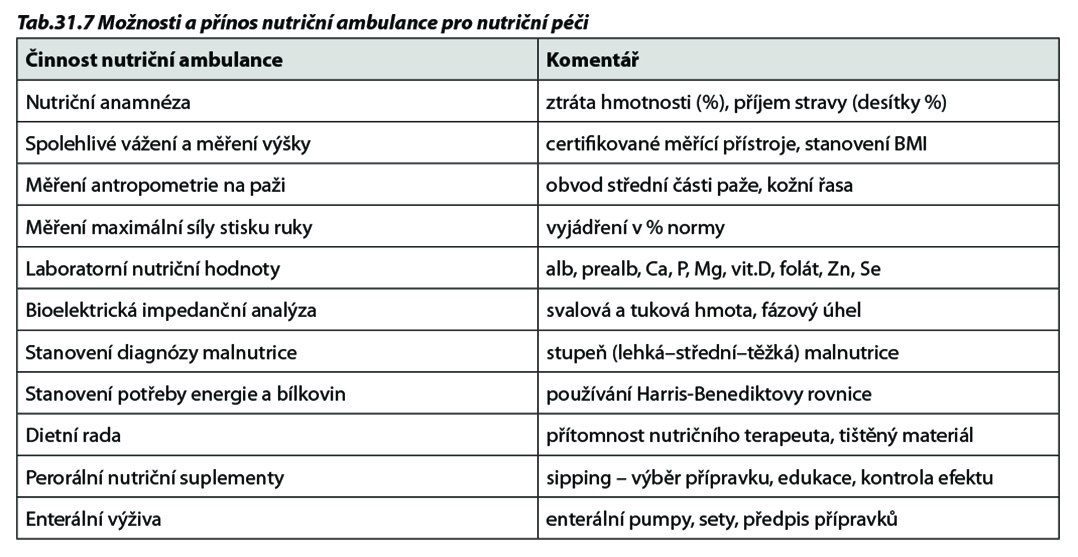
V nemocnici zajišťuje nutriční ambulance pokračování nutriční podpory po propuštění pacienta do ambulantní péče a současně je místem pro specializovanou léčbu malnutrice s oprávněním k předpisu přípravků umělé klinické výživy.
31.10.2 Dokumentace nutriční péče
Údaje o provedení nutričního screeningu, o nutričním stavu a nutriční podpoře by měly být viditelnou součástí onkologické dokumentace. V optimálním případě tak onkolog přistupuje k léčbě svého pacienta se znalostí jeho nutričního rizika (NRS 0–7 bodů).
Ve vybraných případech může být přínosem vedení samostatného nutričního dekurzu, což nejlépe zajistí spolupracující nutriční terapeut nebo lékař nutriční ambulance.
31.10.3 Podmínky pro předpis ONS lékařem s úhradou ZP
Oprávnění k předpisu přípravků tekuté enterální výživy k popíjení (ONS) na recept s úhradou zdravotní pojišťovny (ZP) mají pouze lékaři
• s funkční licencí F016, bez omezení,
• s odborností onkologickou (klinický, radiační či dětský onkolog), s omezením,
• s odborností chirurgickou, s omezením.
Omezení zahrnuje předpis na maximální dobu 4 týdnů, v množství odpovídajícím 600 kcal na den. Podmínkou je časová nebo místní nedostupnost nutriční ambulance a dokumentace nutričního rizika, založená v dokumentaci pacienta (Dotazník hodnocení nutričního rizika dle PSNPO, hodnota 2–4 body). Podmínky úhrady jsou uvedeny na stránkách www.sukl.cz.
Pacientovi je vhodné předat současně s receptem i edukační materiály (Výživná strava, Předpis sippingu), dostupné na webu ČOS v sekci PSNPO.
Literatura:
- The International Declaration on the Human Right to Nutritional Care, Vienna 5.9.2022, dostupné na www.espen.org/files/Vienna-Declaratio-2022.pdf
- Muscaritoli M., Arends J, Bachmann P et al. ESPEN practical guideline: Clinical Nutrition in Cancer. Clin Nutr. 2021, Volume 40, Issue 5, May 2021, Pages
2898-2913 . - Deutz NEP, Safar A, Schutzler S et al.: Muscle protein synthesis in cancer patiens can be stimulated with a speciály formulated medici food. Clinical Nutrition
(2011) 30: 759-768. - Mariani L, Lo Vullo S, Bozzetti F: on behalf of the SCRINIO Working Group: Weight loss in cancer patients: a plea for a better awareness of the isme, Support
Care Cancer (2012) 20:301–309. - Martin L, Senesse P et al. Diagnostic criteria for the classification of cancer-associated weight loss. J Clin Oncol. 2015 Jan 1;33(1):90-9. doi: 10.1200/
JCO.2014.56.1894. Epub 2014 Nov 24. - Bozzetti F, Cotogni P, Lo Vullo S, et al. Development and validation of a nomogram to predict survival in incurable cachectic cancer patients on home parenteral
nutrition. Ann Oncol. 2015 Nov;26(11):2335-40. doi: 10.1093/annonc/mdv365. Epub 2015 Sep 7. PMID: 26347103. - Faber J, Berkhout M, Fiedler U, Avlar M, Witteman BJ, Vos AP, Henke M, Garssen J, van Helvoort A, Otten MH, Arends: Rapid EPA and DHA incorporation
and reduced PGE2 levels after one week intervention with a medical food in cancer patients receiving radiotherapy, a randomized trial. Clin Nutr. 2012,
Jun;32(3):338-45. doi: 10.1016/j.clnu.2012.09.009. Epub 2012 Sep 28. - Vaughan VC, Martin P, Lewandowski PA. Cancer cachexia: impact, mechanism and emerging treatments, J Cachexia Sarcopenia Muscle. 2013 June;4(2):
95-109. - Bozzetti F. Nutritional support of the oncology patient. Oncology/hematology 2013;87: 172-200.
- Dotazník nutričního rizika PSNPO. Dostupný z /files/Dotaznik_nutricniho_rizika.pdf.
- FORD, K L., ARENDS J, ATHERTON P.J., et al. The importance of protein sources to support muscle anabolism in cancer: An expert group opinion. Clinical
Nutrition [online]. 2022, 41(1), 192-201 [cit. 2022-12-09]. ISSN 02615614. Dostupné z: doi:10.1016/j.clnu.2021.11.032





