Konference: 2011 2. pražské mezioborové onkologické kolokvium
Kategorie: Gastrointestinální nádory
Téma: Prezentace
Číslo abstraktu: 005
Autoři: MUDr. Pavel Vítek, PhD.; Mgr. et MUDr. Petra Holečková, Ph.D., MBA; MUDr. Miloslav Pála, Ph.D. MBA,; Doc. MUDr. Josef Dvořák, Ph.D.
Úvod
Epiteliální nádory žaludku a břišní části jícnu tvoří skupinu
častých nádorů. Histologická typizace nejčastěji odpovídá různým
druhům adenokarcinomu. Biologické vlastnosti nádorů žaludku a
distálního jícnu jsou podobné a nádory distálního jícnu často
přerůstají na žaludek. V klinickém výzkumu jsou často obě
onemocnění zařazována do jedné skupiny ´gastroezofageálních´ nádorů
a tento souhrnný termín užíváme v dalším textu. Zhruba polovina z
nich je diagnostikována v pokročilém stadiu. Proto vedle léčby
chirurgické mají významné postavení chemoterapie, biologická léčba
a ozařování. Chemoterapie prošla od 70. let předchozího století
vývojem, během něhož byly vyvinuty různé režimy s postupně se
zvyšující účinností a variabilní toxicitou (FAM,FAMTX, EAP, ELF,
CF). Nejvíce zastoupenými účinnými látkami jsou platinové deriváty
a fluorované pyrimidiny. V posledním desetiletí byl standardním
režimem první řady režim ECF epirubicin, cisplatina, 5-fluorouracil
(5-FU). V tom je 5-FU aplikován formou kontinuální infuze po celou
dobu trvání cyklu. Kontinuální infuze je tudíž ´nekonečná´ a při
ideálním průběhu se protrahuje po dobu podávání režimu ECF. To
přirozeně přináší všechny atributy dlouhodobé kontinuální infuze,
jakými jsou nutnost centrálního žilního přístupu, užívání
přenosného infuzoru, rizika infekčních komplikací souvisejících s
infuzním portem nebo centrálním žilním katetrem, případně i rizika
katetrové sepse nebo tromboembolizmu. Samostatná chemoterapie s
režimem ECF v první volbě je indikována jako paliativní léčba první
řady u pokročilých nádorů a v omezené míře jako léčba neoadjuvantní
u lokálně pokročilých nádorů s výhledem dosažení operability.
V posledním desetiletí je v rozvinutých zemích mimo Asie považována
za standard léčby pooperační (poresekční) adjuvantní
chemoradioterapie s ozářením lůžka žaludku a rizikových spádových
lymfatik podle lokalizace primárního nádoru. Je to léčba provázená
mnohými kontroverzemi, které počínají již u použitého
chemoterapeutického režimu. V unikátní studii,(1) na
jejímž základě se chemoradiace stala standardem, byl použit režim,
který ani za jednoznačnou chemoradiaci považovat nelze, časový
souběh chemoterapie a ozařování je pouze několikadenní. Variantou
ale je kontinuální podání 5-FU po celou dobu ozařování. Rizika a
komplikace kontinuální infuze po celou dobu minimálně pětitýdenního
ozařování jsou podobná jako u režimu ECF.
Orální podání fluorovaných pyrimidinů
Orální formy fluoropyrimidinů byly vyvíjeny již záhy po zavedení
výchozí látky, 5-FU, před půl stoletím. První z nich, tegafur, byl
dokonce široce užíván v bývalém Československu. Další orální formy
S1 a UFT byly vyvíjeny a jsou užívány především ve východní Asii,
zejm. v Japonsku a Korei. U nás byl registrován a od počátku právě
uplynulého desetiletí je stále šířeji užíván preparát capecitabin
(Xeloda®), prekurzor 5-FU. V současné době jsou režimy s
capecitabinem zavedené do standardní terapie nádorů kolorekta,
mammy a do určité míry i u nádorů gastroezofageálních.
Capecitabin je zvláště u nádorů GITu (na rozdíl od nádorů mammy)
považován za náhradu 5-FU. K tomu přispěla i představa,že prekurzor
capecitabin metabolizující se na účinnou látku - 5-FU, svou
kinetikou simuluje kontinuální podání 5-FU, hojně využívané právě u
nádorů GITu. Navíc kontinuální podání 5-FU bylo srovnávacími
studiemi u nádorů kolon ověřeno jako nejúčinnější.(2) V
tomto kontextu vzniká několik základních otázek:
- Lze skutečně považovat orální podání capecitabinu z hlediska farmakokinetiky pouze za náhradu kontinuální infuze 5-FU?
- Jsou režimy s capecitabinem u nádorů gastroezofageálních stejně účinné jako režimy s kontinuálním 5-FU? (Potvrdila se analogie s nádory kolorekta?)
- Bude capecitabin vhodný pro kombinaci s biologickou léčbou (jako u nádorů kolorekta)?
- Lze capecitabin využít i pro chemoradiaci gastroezofageálních nádorů, podobně jako u nádorů rekta?
Farmakologická data
Farmakokinetické parametry capecitabinu jsou dobře popsány.
Capecitabin je bioaktivován v játrech na 5 deoxyfluorocytidin
(5-DFCR) a 5 deoxyfluorouridin (5-DFUR), dále ve tkáních včetně
nádorové na 5-FU. (Obrázek č. 1)
Obrázek 1: Metabolismus capecitabinu
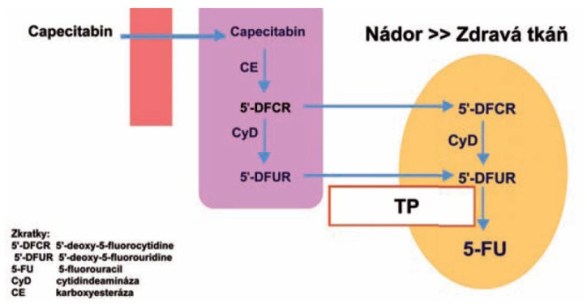
Další přeměna spočívá v katabolismu nebo anabolismu 5-fluorouracilu
do aktivní formy FdUMP nebo katabolismu do neúčinných forem
fluoro-beta-alanin (F-BAL). (Obrázek č. 2)
Obrázek 2: Metabolismus 5-FU
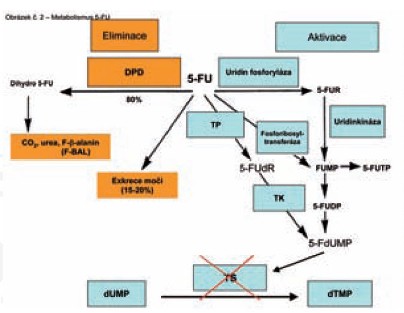
Zkratky
DPD dihydropyrimidindehydrogenáza
5-FU 5-fluorouracil
TP thymidifosforyláza
5-FUR 5-fluorouridin
5-FUdR 5-fluorodeoxyuridin
FUMP fluorouridimonofosfát
S-FUTP 5-fluorodeoxyuridimonofosfát
TK thymidinkináza
5-FUDP 5-fluorouridindifosfát
5-FdUMP 5-fluorodeoxyuridinmonosfát
dUMP deoxyuridinmonofosfát
TS thymidylsyntetáza
dTMP deoxythymidinmonofosfát
Bioaktivace je rychlá, plazmatické hladiny 5-DFCR a 5-DFUR
dosahují maxima cca za 2 hod. po orální aplikaci capecitabinu.
Hladina 5-FU v cirkulaci dosahuje maxima cca za 2 hod. 30 min. a
vrací se k neměřitelným hodnotám do 6 hod. Při podávání po dobu 14
dní nebyly pozorovány významné rozdíly v kinetice a není patrná
tendence k akumulaci. F-BAL dosahuje maxima po 3,3-3,8 hod. a klesá
s poločasem 2,5-2,7 hod. Lze srovnat plochu pod křivkou (AUC)pro
5-FU při 2 možnostech: buď po podání samotného 5-FU formou
kontinuální infuze (300 mg/m2/den) nebo po orálním
podání capecitabinu (1 250 mg/m2, 2x denně, interval 12
hod.). AUC je 1,6x větší po kontinuální infuzi. Mj. při podání 5-FU
formou bolu je AUC 6-2 2x vyšší než po
capecitabinu.(3)
Z farmakokinetických dat je patrné, že aplikace capecitabinu
simuluje kontinuální infuzi 5-FU velmi omezeně,podobná je AUC, ale
o kontinuální expozici 5-FU nejde. Přitom je z
klinických studií patrné, že protinádorová účinnost kontinuální
infuze 5-FU a capecitabinu aplikovaného v intervalu 12 hod. je
obdobná. Capecitabin svým efektem nahrazuje kontinuální
infuzi 5-FU, ale nesimuluje ji.
Plazmatické hladiny 5-FU jsou pro účinnost capecitabinu méně
významným faktorem. Finální konverze 5-DFUR na 5-FU probíhá ve
tkáních a je závislá na koncentraci konvertujícího enzymu
thymidinfosforylázy (TP). Po aplikaci capecitabinu proto převyšuje
tkáňová hladina 5-FU hladinu plazmatickou, a to v poměru 8-10:1.
Navíc řada prací prokazuje, že aktivita TP je vyšší v nádorových
tkáních než v okolní tkáni zdravé, a to v průměrně 3,2x. To
zajišťuje určitou selektivitu efektu a navýšení koncentrace 5-FU v
nádoru proti koncentraci plazmatické v poměru až
20:1.(4) Aktivita TP je pak mnohem významnějším faktorem
pro účinnost capecitabinu než plazmatická koncentrace. Neméně
významným faktorem je aktivita katabolického enzymu
dihydropyrimdindehydrogenázy (DPD).
Tkáňová (nádorová) koncentrace 5-FU je za současného působení
konvertujícího a katabolického enzymu dána určitou dynamickou
rovnováhou, resp. poměrem jejich aktivit. To potvrzují originální
práce Ischikawy a spol. u experimentálních nádorů.(5)
Poměr aktivit TP vs. DPD koreluje s účinností 5-dFURd, UFT a zejm.
capecitabinu.(6,7) Poměr koncentrace DPD v nádorové vs.
zdravé tkáni nebyl určen tak jednoznačně jako u TP, evidentní je
velká variabilita v různých tkáních včetně nádorových.
Z hlediska tkáňové, selektivní, konverze 5-DFUR na 5-FU je význam
plazmatické kinetiky 5-FU pro protinádorovou účinnost malý.
Capecitabin je sice prekurzorem 5-FU, ale pro jeho efekt je
určující,s jakou kinetikou se konvertuje z 5-DFUR na 5-FU,a to
intracelulárně.
TP je masivně exprimována u cca poloviny adenokarcinomů žaludku. TP
je identická s angiogenním faktorem PD-ECGF ´Platelet Derived
Endothelial Cell Growth Factor´.(8)
Proto lze zvýšené expresi TP přisuzovat pozitivní prediktivní
hodnotu pro terapii fluorovanými pyrimidiny včetně capecitabinu.
Zároveň ale má negativní prognostickou hodnotu pro
gastroezofageální adenokarcinom obecně.(9) I přes
dostatečnou evidenci se TP jako prediktor běžně nestanovuje.
Capecitabin u gastroezofageálních nádorů – paliativní a
neoadjuvantní indikace
Porovnání účinnosti capecitabinu a 5-fluorouracilu bylo u
gastroezofageálních nádorů předmětem studií fáze III – ´REAL-2´ a
´ML17032´.(10,11) Obě studie zařazovaly nemocné s pokročilými
gastroezofageálními nádory.
Studie REAL-2 byla navržena s cílem prokázat ekvipotenci
(´noninferiority´) capecitabinu a 5-FU v tripletu (trojkombinaci) a
současně prokázat ekvipotenci oxaliplatiny a cisplatiny. Vznikla
tak čtyřramenná studie srovnávající režimy ECX, ECF, EOX, EOF
(zkratky a režimy jsou uvedené v Tabulce č. 1) u celkového počtu 1
002 probandů. V parametrech přežívání, včetně rizika úmrtí (´hazard
ratio´ HR), a parametrech doby do relapsu byla ekvipotence
prokázána, a to pro capecitabin a 5-FU i pro platinové
deriváty.
Studie ML 17032 byla navržena také s cílem prokázat ekvipotenci
5-fluorouracilu a capecitabinu v dubletovém režimu s cisplatinou,
tzn. CF vs. CX. V parametrech přežívání bez progrese a celkového
přežívání byla ekvipontence prokázána. Navíc v parametru počtu
odpovědí na léčbu (´response rate´ – RR) je signifikantní výhoda u
režimu CX (41 % vs. 29 %, p = 0,03).
Toxicita vychází v obou studiích bez výrazných rozdílů. Obě studie
dostatečně prokázaly, že u pokročilých gastroezofageálních nádorů
může kontinuální infuze 5-FU být bezpečně nahrazena capecitabinem.
Detailní údaje ze studií REAL-2 a ML17032 jsou uvedené v Tabulce č.
1.
Tabulka 1: Porovnání výsledků studií REAL-2 a ML 17032
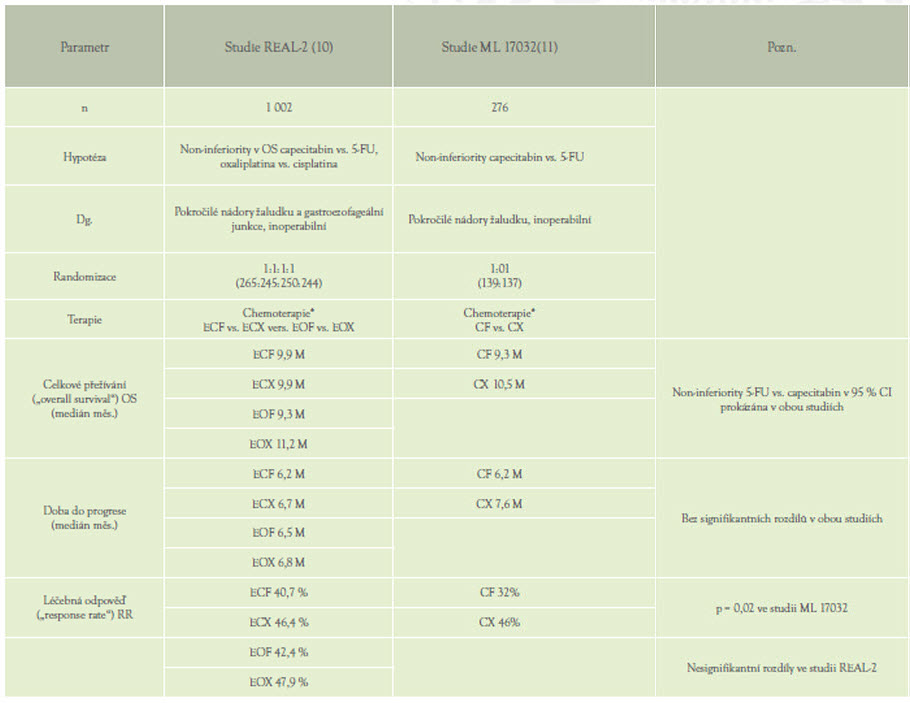
*Schemata chemoterapie:
ECF epirubicin 50 mg/m2 d1, CDDP 60 mg/m2
d1,
5-FU 200 mg/m2 CI d 1-21, q21d
ECX epirubicin 50 mg/m2 d1, CDDP 60 mg/m2
d1,
capecitabin 625 mg/m2 2xd d1-21, q21d
EOF epirubicin 50 mg/m2 d1, oxaliplatina 130
mg/m2,
5-FU 200 mg/m2 CI d1-21, q21d
EOX epirubicin 50 mg/m2 d1, oxaliplatina 130
mg/m2,
capecitabin 625 mg/m2 2xd d1-21, q21d
CF CDDP 80 mg/m2 d1, 5-FU 800 mg/m2 CI
d1-5
CX CDDP 80 mg/m2 d1, capecitabin 1000 mg/m2
2xd d 1-14
Následná poněkud neobvyklá metaanalýza dvou uvedených
studií(12) opět potvrzuje ´non-inferiority´ capecitabinu
vs. kontinuální infuze 5-FU. Navíc ještě prokazuje určitou výhodu
capecitabinových režimů v parametru celkového přežívání medián 322
dní vs. 285 dní, p = 0,027. Tento výsledek má nevýznamný praktický
dopad. Navíc je ale patrný signifikantní rozdíl v počtu dosažených
odpovědí (response rate) 45,6 % vs. 38,4 %, p = 0,006. Ten již má
praktický výstup pro neoadjuvantní chemoterapii. Podíl odpovědí lze
interpretovat i tak, že významná část nemocných, kteří dosáhli
odpovědi na léčbu, mohou také dosáhnout operability, tzn. dospět ke
kurativní terapii.
Toxicita jednotlivých režimů nepřekročila rizika evidovaná z
předchozích studií a neomezuje užití kteréhokoliv z režimů. V
capecitabinových režimech podle očekávání dominuje hand-foot
syndrom (st. III a IV 3,1 %-10,3 %), neutropenie (st. III a IV 27,6
%-41,7 %) a tromboembolizmus (5,6 %-6,1 %). Kromě výskytu hand-foot
syndromu není mezi režimy signifikantní rozdíl.
Při zřejmé ekvipotenci capecitabinu a 5-FU ve standardních režimech
byl capecitabin zařazen i do studií ověřujících benefit dalšího
rozšíření chemoterapie, a to o biologickou léčbu. Variabilní údaje
o expresi HER2 (6-35 %) vedly ke screeningu v rámci studie ToGA u 3
807 nemocných s pokročilými gastroezofageálními
nádory.(13) HER2-pozitivita (imunohistochemicky
semikvantitativně 3+ nebo FISH pozitivita) je patrná ve 22,1 %. Je
signifikantní rozdíl mezi pozitivitou u nádorů gastroezofageální
junkce a nádorů distálně od kardie (33,2 %, resp. 20,1 %). 594
nemocných s HER2-pozitivitou bylo randomizováno k chemoterapii
(CDDP + capecitabin nebo 5-FU) s trastuzumabem (podáváným do
progrese) nebo k chemoterapii samotné. V parametru celkového
přežívání je patrný signifikantní rozdíl ve prospěch terapie s
trastuzumabem.(14) Podobně ve studii AVAGAST je 774
nemocných randomizováno k chemoterapii (CDDP + capecitabin nebo
5-FU)s bevacizumabem nebo k chemoterapii samotné.(15) V
parametrech přežívání bez progrese a podílu odpovědí (response
rate) je patrný signifikantní rozdíl ve prospěch kombinace s
bevacizumabem. V parametru celkového přežívání signifikantní rozdíl
není. Údaje z obou studií jsou uvedeny v Tabulce č. 2.
Tabulka 2: Data ze studií ToGA a AVAGAST
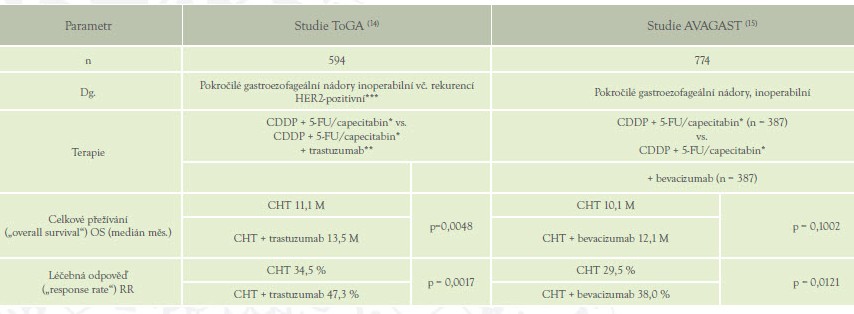
* Režimy s 5-FU nebo capecitabinem jsou zahrnuty jako
rovnocenné
** Trastuzumab podáván trvale do progrese onemocnění
*** Pozitivita imunohistochemicky +++ (HercepTest®) nebo FISH
pozitivní
Obě studie fáze III zařazují capecitabin jako zaměnitelný
ekvivalent 5-FU. Obě studie jsou v souladu s dalším trendem v léčbě
gastroezofageálních nádorů. Ten směřuje k zavádění biologické
terapie spíše než k rozšiřování cytostatické terapie. Studie fáze
II s látkami, jakými jsou everolimus nebo sunitinib zatím
nepřinesly jednoznačné výsledky.(16) V tomto kontextu
již není nutné dále porovnávat dosud zavedené orální vs. infuzní
formy fluoropyrimidinů. Ekvipotence je verifikována dostatečně,
případná výhoda jedné z forem je pravděpodobně málo významná a
obtížně prokazatelná. Navíc by průkaz potenciálně malého benefitu
neměl žádný efekt. Pokud nejsou signifikantní rozdíly ani v
toxicitě, zůstává hlavní rozdíl v compliance nemocného a ta je
jednoznačně ve prospěch orální formy nad kontinuální infuzí. Orální
formy jsou výhodné i proto, že další zkoušené prostředky biologické
terapie jsou také v orální formě a aplikační schémata se
zjednodušují.
Chemoradioterapie gastroezofageálních nádorů
Základem kurativní léčby gastroezofageálních nádorů je radikální
resekční výkon. Vysoké riziko mtachronního relapsu formou lokální
recidivy nebo vzdálených metastáz vedlo již před 20 lety k otevření
studií adjuvantní chemoterapie. Do současnosti se výhody jakékoliv
adjuvantní chemoterapie nepodařilo formou randomizované studie fáze
III prokázat. První standardní adjuvantní léčbou se stala
chemoradioterapie na základě studie ´Intergroup-0116
study´.(1) Ta prokázala signifikantní benefit
pooperačního ozáření lůžka žaludku a spádových lymfatik v kombinaci
s chemoterapií FUFA, a to v parametru snížení rizika lokální
recidivy v parametru délky přežívání.
Přestože se pooperační chemoradiace na základě této studie rychle
stala standardem v západním světě, vyvolává stále řadu
kontroverzí.
Prvořadá je otázka, zda přínos pooperační chemoradiace lze nahradit
rozsáhlejší resekcí v oblasti lymfatik. Odvíjí se od analýzy
provedených resekcí ve studii Intergroup-0116, kde D2 resekce
tvořila pouze 10% podíl. V asijských zemích, zejm. v Japonsku, kde
jsou resekce lymfatik vedené velmi precizně a ve větším rozsahu
pooperační chemoradiace, nikdy standardem nebyla. Naproti tomu
studie nizozemských autorů neprokázaly(17,18) benefit D2
resekce ve smyslu délky přežívání, což je zřejmě dáno vyšší
morbiditou a mortalitou v souvislosti s výkonem. A v neposlední
řadě v souboru nemocných po D2 resekci korejských
autorů(19) byl prokázán benefit pooperační chemoradiace
s 5-FU, a to v parametru délky přežívání. Zásadním předmětem
kritiky ve studii Intergroup-0116 je toxicita, která umožnila
dokončit terapii, a tudíž vstoupit do hodnocení, pouze 63 %
nemocných, což tvoří zásadní výběrové bias.
Další kontroverzí je schéma aplikované chemoradiace ve studii
Intergroup-0116. Konkomitantní chemoterapie je podávána pouze první
čtyři a poslední tři dny ozařování a navíc jsou 3 pětidenní cykly
chemoterapie FUFA, 1 před a 2 po chemoradiaci. Není použita
kontinuální infuze 5-FU, ale starší bolusové režimy
NCCTG.(20) Techniky radioterapie lze obtížně posuzovat
na základě informace z publikace, kde jejich popis chybí. Nicméně
studie byla vedena v letech 1991-1998, kdy standardem bylo
ozařování podjaterní krajiny, resp. lůžka žaludku ze 2 protilehlých
polí, takže není pochyb o tom, že současnými technikami lze
dosahovat menší morbidity.
Fluorované pyrimidiny v chemoradiaci gastroezofageálních
nádorů
Podobně jako u nádorů rekta se jako nejúčinnější režim chemoradiace
nabízí kontinuální infuze 5-FU po celou dobu ozařování. Její
účinnost nikdy samostatnou randomizovanou studií ověřována nebyla.
U gastroezofageálních nádorů se vyvíjejí další režimy zahrnující
více účinných látek a obsahujících i chemoradiaci vycházející z
kontinuální infuze 5-FU jako standardního základu. V několika
studiích je zahrnuta v chemoradiaci současně s paclitaxelem nebo
cisplatinou (PCF režim, PF režim).(21,22) Tyto studie
zatím přinášejí informace zejména o toxicitě, ke standardnímu
pooperačnímu, případně neoadjuvantnímu režimu nedospěly. Otázka
nahrazení kontinuální infuze 5-FU capecitabinem v chemoradiaci
formou randomizované studie také řešena nebyla a pravděpodobně
nebude. Proveditelnost u gastroezofageálních nádorů byla ověřena v
několika studiích fáze I a II,(23,24) které potvrdily
dávkování obdobné jako u nádorů rekta (825 mg/m2 2x
denně ) a bezpečnost režimu v intencích známého profilu toxicity.
Retrospektivní nerandomizovaná studie autorů ze
Singapuru(25) analyzovala výsledky: a/ Chemoradiace s
capecitabinem 825 mg/m2 2x denně, včetně následujících 6
cyklů capecitabinu. b/ Chemoradiace bolusovým režimem FU FA (schéma
podle studie ´Intergroup 0116´). c/ Chemoterapie samotné, blíže
nespecifikované. U všech nemocných předcházela gastrektomie D2.
Nejde o přímé porovnání kontinuální infuze a capecitabinu. Kromě
toho, že poskytuje zejména zajímavou statistickou hříčku, je
patrné, že v parametru mediánu doby přežívání bez relapsu ani
celkové doby přežívání není signifikantní rozdíl. Navíc orální
forma,
capecitabin, je dobře snášena i po gastrektomii. Toxicita st. 3-4
je pouze v 5 % a u capecitabinu jsou podle předpokladu dominující
průjmy. Statistické údaje a výsledky studie jsou sumarizovány v
Tabulce č. 3. Určitě zajímavý nález představuje nesignifikantní
rozdíl mezi chemoradioterapií a chemoterapií samotnou, zvláště za
stavu, kdy žádné porovnání chemoradiace a chemoterapie samotné
formou randomizované studie neexistuje. Nespecifikované režimy
chemoterapie v retrospektivní a nerandomizované studii ale brání
jakýmkoliv dalším rozvahám.
Tabulka 3: Výsledky retrospektivní studie pooperační chemoradiace
vs. chemoterapie(25)
| Parametr | Chemoradiace 5-FU | Chemoradiace capecitabin* | Chemoterapie |
| n | 52 | 33 | 23 |
| Celkové přežívání (´overall survival´)OS (medián měd.) | 54 | 53 | 44 |
| Hazard ratio v 95% CI** | 0,89(0,428-1.856) p=0,8 | 1 | 1,19(0,494-2,882) p=0,7 |
| Přežívání bez relapsu (´recurrence free survival´) RFS (medián měs.) | 35 | 52 | 25 |
| Hazard ratio v 95% CI** | 0,97(0,477-1,966) p=0,9 | 1 | 1.03(0,433-2,444) p=0,9 |
* Referenční režim
** Porovnání s referenčním režimem
O ekvipotenci, resp. zaměnitelnosti kontinuální infuze 5-FU a
capecitabinu zřejmě u chemoradiace gastroezofageálních nádorů
pochybovat nelze, byť z hlediska ´evidence based medicine´ by
randomizovaná studie prokazující ´non-inferiority´ byla vhodná. Ta
ale pravděpodobně vedena a ukončena nikdy nebude. Analogická
situace je u podstatně častější indikace předoperační chemoradiace
ca rekta. V prostředí, kdy je naléhavou otázkou výzkumu zařazení
dalších účinných látek, včetně biologické terapie, měla nekonečná
studie NSABP R-04, porovnávající capecitabin a kontinuální infuzi
5-FU s cílem průkazu ´non-inferiority´, problémy se zařazováním
nemocných, byť uzavření studie bylo předpokládáno na konec května
2010.(26)
Závěry
Fluorované pyrimidiny jsou standardní součástí chemoterapie nádorů
zažívacího traktu, včetně gastroezofageálních. Běžná schémata
chemoterapie byla vyvíjena s původní látkou 5-FU. Nevýhoda
parenterální aplikace 5-FU se obnažila po ověření vyšší účinnosti
kontinuální aplikace v 90. letech předchozího století. Proto byly
vyvinuty a klinicky zkoušeny orální varianty buď prekurzory,
capecitabin, nebo kombinované preparáty s modifikovaným
metabolismem 5FU (S1 a UFT). Všechny mají farmakokinetické i
farmakodynamické předpoklady ke stejnému nebo vyššímu efektu jako
5-FU. Randomizovanými studiemi byla ´non-inferiority´ ověřena a
byla vyvinuta standardní aplikační schémata, gastroezofageální
nádory nevyjímaje. Režimy ECX, CX, DCX, DOX patří do základního
armamentária. V oblasti chemoradiace je ekvipotence orálních forem
zkoumána méně, předmětem zájmu je pouze capecitabin. Randomizované
studie ´non-inferiority´ chybějí a v rychlém rozvoji dalších
chemoradiačních schémat současně s rozvojem ozařovacích technik
není čas ani prostor je provádět. Přesto ale orální formy, resp.
capecitabin do standardní chemoradiace nádorů GITu, včetně
gastroezofageálních evidentně patří.
Literatura
- Mcdonald JS, Smalley SR, Benedetti J, Scott A, et al. Chemoradiotherapy after surgery compared with surgery alone for adenocarcinoma of the stomach or gastroesophageal junction. N Engl J Med 2001;345:725-730.
- Rougier P, Buyse M, Ryan L, Hansen R, et al. Meta-analysis of all trials comparing intravenous bolus administration to continuous infusion of 5-fluorouracil in patients with advanced colorectal cancer. Proc. ASCO 1997;Abst. 946.
- Coustére C, Mentré E, Sommadossi JP, Diasio RB, et al. A mathematical model of the kinetics of 5-FU and its metabolites in cancer patients. Cancer Chemother Pharmacol 1991; 28:123-9.
- Schueller J, Cassidy J, Dumont E, Ross B. Preferential activation of capecitabine in tumor following oral administration to colorectal cancer patients. Cancer Chemother Pharmacol 2000;45:291-297.
- Ishikawa T, Sekiguchi F, Fukase Y, et al. Positive correlation between the efficacy of capecitabine and doxifluridine and the ratio of thymidine phosphorylase to dihydropyrimidinedehydrogenase activities in tumors in human cancer xenografts. Cancer Res 1998;58:685-690.
- Terashima M, Fujiwara H, Takagane A, et al. Role of thymidine phosphorylase and dihydropyrimidinedehydrogenase in tumor progression and sensitivity do doxifluridine in gastric cancer patients. Eur J Cancer 2002;38:2375-2381
- Blanquicett C, Gillespie Y, Nabors LB, Miller CR, et al. Induction of thymidine phosphorylase in both irradiated and shielded, contralateral human U87MG glioma xenografts: Implications for a dual modality treatment using capecitabine and irradiation. Molecular Cancer Therapeutics 2002;1:1139-1145.
- Yu EJ, Lee Y, Rha SY, Kim TS, et al. Angiogenic factor tymidine phosphorylase increases cancer cell invasion activity in patients with gastric adenocarcinoma. Mol Cancer Res 2008;6:1554-1566.
- Saito J, Tsujitani S, Oka S, Kondo A, et al. The expression of thymidine phosphorylase correlated with angiogenesis and the efficacy of chemotherapy using fluorouracil derivatives in advanced gastric carcinoma. Br J Cancer 1999;81:484-489.
- Cunningham D, Starling N, Rao S, Iveson T, et al. Capecitabine and Oxaliplatin for Advanced Esophagogastric Cancer. N Engl J Med 2008;358:36-46.
- Kang YK, Shin DB, Chen J, et al. Randomized phase III trial of capecitabine/cisplatin (XP) vs. continuous infusion of 5-FU/cisplatin as first-line therapy in patients with advanced gastric cancer. Proc. ASCO 2006, LBA 4108.
- Okines AFC, Norman AR, McCloud P, Kang YK, et al. Meta-analysis of the REAL-2 and ML17032 trials: Evaluating capecitabine-based combination chemotherapy and Infused 5-fluorouracil-based combination chemotherapy for the treatment of advanced oesophago-gastric cancer. Ann Oncol 2009;20:1529-1534.
- Bang Y, Chung H, Xu J, Lordick F. Pathological features of advanced gastric cancer (GC): Relationship to human epidermal growth factor receptor 2 (HER2) positivity in the global screening programme of the ToGA trial. Proc. ASCO 2009, Abst. 4556.
- Van Cutsem E, Kang YK, Chung H, Shen L. Efficacy results from the ToGA trial: A phase III study of trastuzumab added to standard chemotherapy in first-line human epidermal growth factor receptor 2 (HER2)-positive advanced gastric cancer. Proc. ASCO 2009, LBA 45009.
- Kang YK, Ohtsu A, Van Cutsem E, Rha SY. AVAGAST: A randomized,
double-blind, placebo-controlled, phase III study of first-line
capecitabine and cisplatin plus
bevacizumab or placebo in patients with advanced gastric cancer. Proc. ASCO 2010, LBA 4007. - Rosati G, Ferrara D, Manzione L. New perspectives in the treatment of advanced or metastatic gastric cancer. World J. Gastroenterol. 2009;15:2689-2692.
- Bonenkamp JJ, Hermans J, Sasako M, van de Velde CJ, et al. Extended lymf-node dissection for gastric cancer. N Engl J Med 1999;340:908-914.
- Hartgrink HH, van de Velde CJ, Putter H, Bonenkamp JJ. et al. Extended lymph-node dissection for gastric cancer: Who may benefit? Final results of the randomized Dutch gastric cancer group trial. J Clin Oncol 2004;22:2069-2077.
- Kim S, Lim DH, Lee J, Kang YK, et al. An observational study suggesting clinical benefit for adjuvant postoperative chemoradiation in a population of over 500 cases after gastric resection with D2 nodal dissection for adenocarcinoma of the stomach. Int J Radiat Oncol Bio. Phys 2005;63:1279-1285.
- Poon MA, O´Connell, Moertel CG, et al. Biochemical modulation of fluorouracil: Evidence of signifiant improvememnt of survival and quality of life in patients with advanced colorectal carcinoma. J Clin Oncol 1989;7:1407-1418.
- Schwartz GK, Winter K, Minsky BD, Crane C, et al. Randomized phase II trial evaluating two paclitaxel and cisplatin containing chemoradiation regiment as adjuvant therapy in resected gastric cancer (RTOG-0114). J Clin Oncol 2009;27:1956-1962.
- Ajani JA, Mansfield PF, Crane CH, Wu TT, et al.
Paclitaxel-based chemoradiotherapy in localized gastric carcinoma:
degree of pathologic response
and not clinical parameters dictated patient outcome. J Clin Oncol 2005;23:1237-1244. - Jansen EP, Boot H, Saunders MP, Crosby TD, et al. A phase I-II study of postoperative capecitabine-based chemoradiotherapy in gastric cancer. Int J Radiat Oncol Biol Phys 2007;69:1424-1428.
- Lee HS, Choi Y, Hur WJ, Kim HJ, et al. Pilot study of postoperative adjuvant chemoradiation for advanced gastric cancer: Adjuvant 5-FU/cisplatin and chemoradiation with capecitabine. World J Gastroenterol 2006;12:603-607.
- Tham CK, Choo SP, Poon DYH, Toh HC, et al. Capecitabine with radiation is an effective adjuvant therapy in gastric cancers. World J. Gastroenterol. 2010; 16:3709-3715.
- http://www.cancer.gov/clinicaltrials/NSABP-R-04
MUDr. Pavel Vítek, Ph.D.
MUDr. Petra Holečková
MUDr. Miroslav Pála
MUDr. PharmDr. Jan Dvořák
Ústav radiační onkologie FN Na Bulovce, 1. LF UK,
Praha
e-mail: vitekp@fnb.cz
Datum přednesení příspěvku: 28. 1. 2011
