Konference: 2011 XXXV. Brněnské onkologické dny a XXV. Konference pro sestry a laboranty
Kategorie: Kolorektální karcinom
Téma: Diagnostika a léčba kolorektálního karcinomu
Číslo abstraktu: 031
Autoři: prof. MUDr. Igor Kiss, Ph.D., MBA; MUDr. Jiří Tomášek, Ph.D.; MUDr. Jana Halámková, Ph.D.
Další indikací chemoterapie je léčba paliativní či neadjuvantní, pro inoperabilní metastázy klinického stadia IV (TX NX M1), která až donedávna měla za cíl pouze prodloužené přežití pacientů. V posledních 10 letech jsou do rutinní praxe zavedena cytostatika nové generace (irinotekan, oxaliplatina), která v kombinaci s biologickou léčbou (bevacizumab, cetuximab, panitumumab) rozšířila možnosti chirurgie a intervenční radiologie. Cíle paliativní chemoterapie jsou v řadě případů podobné jako cíle neoadjuvantní chemoterapie, tj. navození sekundární operability primárně inoperabilního či hraničně operabilního onemocnění. Správné načasování a individuální přístup při stanovení léčebného postupu je v tomto případě možné pouze za velmi úzké mezioborové spolupráce – multidisciplinární indikační komise. Efekt chemoterapie je vyhodnocován průběžně jak ve smyslu tolerance a toxicity, tak i z pohledu efektivity léčby. Největší efektivitu v současné době dosahuje kombinovaná chemoterapie na bázi oxaliplatiny či irinotekanu se srovnatelným efektem (FOLFOX, CAPOX, FOLFIRI), vykazující až 50% léčebných odpovědí provázených prodlouženým mediánem přežití pacientů kolem 20 měsíců a s popisovanou sekundární operabilitou primárně inoperabilního onemocnění kolem 2-4%. Všechny režimy lze podat sekvenčně (FOLFOX/FOLFIRI nebo FOLFIRI/FOLFOX). Léčba oxaliplatinou je často provázena kumulativní neurotoxicitou. Tato komplikace je pak důvodem k ukončení, přerušení nebo změně léčby. Ve studii OPTIMOX1 bylo prokázáno, že po 6 cyklech FOLFOX 7 lze přerušit podávání oxaliplatiny a pokračovat jen v kombinaci FUFA. V případě progrese nemoci je pak možné znovu zahájit aplikaci oxaliplatiny u nemocných, kteří původně dosáhli kombinací FOLFOX léčebné odpovědi. Tyto výsledky byly příznivější než úplné přerušení chemoterapie, jak prokázala studie OPTIMOX2.
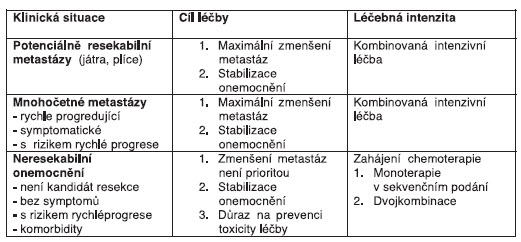
Tabulka 1: Strategie léčby metastatického kolorektálního karcinomu (ESMO 2010)
Při kombinaci chemoterapie s biologickou léčbou
(bevacizumab, cetuximab) dochází k nárůstu sekundární operability
na 6 až 7%, přičemž pro podskupiny pacientů s metastatickým
postižením pouze v oblasti jater, dosahuje tato sekundární
operabilita až 10%. U podskupiny pacientů s metastazami pouze do
jater a za přítomnosti wild type KRAS (wt KRAS) léčených
chemoterapií v kombinaci s cetuximabem, dosahovaly léčebné odpovědi
(kompletní a parciálné remise) až 60-70% se sekundární operabilitou
až v 34%. Ve studii MACRO byla testována otázka udržovací léčby
bevacizumabem. Pacienti v I.linii léčby metastatického onemocnění
byli po 6 cyklech chemoterapie XELOX/bevacizumab randomizováni k
pokračování léčny XELOX/bevacizumab či pouze k udržovací terapii
bevacizumabem. Medián doby do progrese byl pro obě léčebné možnosti
srovnatelný, tj.11 a 10 měsíců, signifikantní rozdíl však byl
pozorován v dosaženém mediánu přežití, který byl 25,3 ku 20,7
měsíců ve prospěch pokračující kombinované léčby.
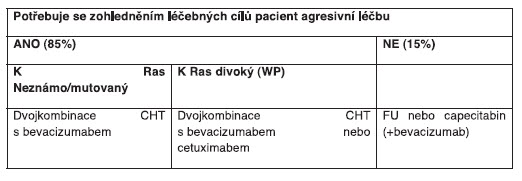
Tabulka 2: Rozhodovací algoritmus strategie léčby v I. linii
metastatického kolorektálního karcinomu (ESMO 2010)
Předoperační chemoterapie je zvažovaná i v
případech primárně operabilního metastatického onemocnění.
Chemoterapie FOLFOX zlepšuje výsledky 3 leté doby do progrese o
7-8%. Předoperační chemoterapie je doporučována na maximální dobu 3
měsíců a po resekci pokračuje chemoterapie další 3 měsíce. I
případné zahájení chemoterapie v této indikaci musí být
konzultováno v rámci multidisciplinární komise, zvláště se
zaměřením na lokalizaci všech metastáz pro případ, že by vlivem
chemoterapie bylo dosaženo takového efektu, kdy metastázy vymizí.
Bylo prokázáno v rámci randomizované studie, že i při dosažení
radiologem stanovené kompletní remise, tj. vymizení metastáz dle
zobrazovacích metod, je vhodné tyto původní místa v jaterním
parenchymu resekovat, protože až v 80% případů budou v resekátu
nalezeny aktivní nádorové buňky z kterých dojde postupem času k
relapsu onemocnění. V současné době nejsou k dispozici žádné
výsledky, podporující použití razantnější chemoterapie (tripletů)
či chemoterapie v kombinaci s biologickou léčbou v indikaci léčby
primárně resekabilního onemocnění.
Vlastní zkušenosti s chemoterapií v kombinaci s
biologickou léčbou vyplývají z lékových registrů, kde je registrace
každého pacienta podmínkou úhrady ze strany plátce zdravotní péče.
Celkem je hodnocen 1294 pacientů v léčbě 1. linií a výsledky této
nákladné léčby mírně převyšují výsledky velkých klinických studií,
medián přežití 29,5 měsíce, doba do progrese 12 měsíců.
Literatura
- Adam R, Wicherts DA, de Haas RJ, et al: Patient wit initially
unresectable colorectal liver metastase: is there a posibility of
cure? J Clin Oncol 2009, 27, 1829-1835
- Bismuth H, Adam R, Levi F et al: Resection of nonresectable
liber metastase from colorectal cancer after neoadjuvant
chemotherapy. Ann Surg 1996, 224, 509-522
- Bokemeyer C, Bondarenko I, Makhson A, et al: Fluorouracil,
leucovorin and oxaliplatin with and without cetuximab inthe first
line treatment of metastatic colorectal cancer. J Clin Oncol, 2009,
27, 663-671.
- Cassidy J., Clarke S, Diaz-Rubio E., et al: Randomized phase
III study of capecitabine plus oxaliplatin compared with
fluorouracil/folinic acid plus oxaliplatin as first-line therapy
for metastatic colorectal cancer. J Clin Oncol 2008, 26,
2006-2012.
- De Gramont A., Figer A., Seymour M., et al: Leucovorin and
fluorouracil with or without oxaliplatin as first line treatment in
advanced colorectal cancer. J Clin Oncol 2000, 18,
2938-2947
- Douillard J.Y., Cunningham D., Roth A.D. et al: Irinotecan
combined with fluorouracil compared with fluorouracil alone as
first line treatment for metastatic colorectal cancer: a
multicentre randomized trial. Lancet 2000, 355,
1041-1047
- Chibaudel B., Maindrault-Goebel F., Liedo G. et al: Can
chemotherapy by discontinued in unresectable metastatic colorectal
cancer ? The GERCOR OPTIMOX2 study. J Clin Oncol 2009, 27,
5727-5733
- Grothey A., Sargent D., Goldberg R., Schmoll H.J. Survival of
patients with advaced colorectal cancer improves with the
availability of fluorouracil-lecovorin, irinotecan, and oxaliplatin
in the course of treatment. J Clin Oncol 2004, 22,
1209-1214
- Koopman M, Antonini N.F., Douma J.: Sequential versus
combination chemotherapy with capecitabine, irrinotecan, and
oxaliplatin in advanced colorectal cancer (CAIRO): a phase III
randomised controlled trial. Lancet 2007, 370, 135-142
- Kubala E, Bartoš J., Petruželka L, et al: Safety and
effectivness of bevacizumab in combination with chemotherapy in
patients with metastatic colorectal cancer in eldery
population:updated results from a large Czech observational
registry. ASCO GI 2010
- Nordlinger B, Skrbte H, Glimelius B, et al.: Preoperative
chemotherapy whith FOLFOX4 and surgery versus surgery alone for
resectable liver metastases from colorectal cancer (EORTC
Intergroup trial 40983): a randomized controlled trial. Lancet
2008, 371, 1007-1016
- Saltz LB, Clarke S, Díaz-Rubio E, et al.: Bevacizumab in
combination wit oxaliplatin based chemotherapy as first line
therapy in metastatic colorectal cancer: a randomized phase III
study. J Clin Oncol 2008, 26, 2013-2019.
- Seymour M., Maughan T., Ledermann J et al: Different strategie
sof sequential and combination chemotherapy for patients with poor
prognosis advaced colorectal cancer: a randomised controlled trial.
Lancet 2007, 370, 143-152
- Tournigand C., Andre T., Achille E at. Al: FOLFIRI followed by
FOLFOX 6 or the reverse sequence in advaced colorectal cancer: a
randomised GERCOR study. J Clin Oncol 2004, 22, 229-237
- Van Cutsen E., Hoff P.M., Harper P et al: Oral capecitabine vs
intravenous 5-fluorouracil and leucovorine: integrated efficacy
data and novel analyses from two large randomised phase III trials.
Brit J Cancer 2004, 90, 1190-1197
- Van Cutsen E., Kohne CH, Hitre E, et al: Cetuximab and
chemotherapy as initial treatment for metastatic colorectal cancer.
N Engl J Med, 2009, 360, 1408-1417.
- Vyzula R. a spol: Počty pacientů v lékových registrech ČOS-průběžná zpráva stav k dubnu/květnu 2010, Forum Onkologů, Brno
Datum přednesení příspěvku: 21. 4. 2011
