Konference: 2006 XIII. Jihočeské onkologické dny
Kategorie: Zhoubné nádory prsu
Téma: Léčba časného karcinomu prsu
Číslo abstraktu: 013
Autoři: prof. MUDr. Jiří Petera, Ph.D.
Prs šetřící léčba se stala standardním
postupem u I. a II. stadia karcinomu prsu. Zahrnuje prs
zachovávající chirurgický výkon (lumpectomii, kvadrantectomii) a
ozáření celého prsu do dávek 45-50 Gy. Dvě velké randomizované
studie /Lyonský trial (1) a EORTC trial 2281/10882 (2)/ prokázaly
efekt lokálního zvýšení dávky záření na lůžko tumoru (boost), kde
vzniká nejvíce lokálních recidiv (cca 80 %). V EORTC studii byl
výskyt lokálních recidiv 4,3 % ve skupině s boostem vs. 6,8 % ve
skupině bez boostu, tento rozdíl byl statisticky vysoce
signifikantní. Benefit byl nejvyšší pro pacientky mladší 40 let (9
% vs. 20 %).
Lokální kontrola je u karcinomu prsu významným faktorem pro celkové přežití, což bylo opakovaně prokázáno (3,4, 5, 6).
Boost je možné aplikovat zevně fotonovým nebo elektronovým svazkem nebo intersticiální brachyterapií. Od 80. let do poloviny 90. let pokleslo užívání intersticiálního boostu o 60 %, což souviselo s nahrazováním kobaltových ozařovačů lineárními urychlovači a rostoucí popularitou boostu elektronového. K tomu přistoupily přísnější požadavky na radiační ochranu, což vytlačovalo manuální afterloading.
Proč vůbec uvažovat o intersticiálním boostu, který je pracnější a náročnější než elegantní boost elektronový? Je několik teoretických důvodů, proč by měl být intersticiální boost výhodnější. Intersticiální boost je schopen léčit plánovací cílový objem (PTV) více konformě a redukovat objem ozářené prsní tkáně. V EORTC studii byl PTV pro boost v průměru 60 cm3 pro brachyterapii, 144 cm3 pro elektrony a 288 cm3 pro fotony.
Tato výhoda je zřejmá především pro tumory uložené hlouběji než 28 mm pod epidermis, které vyžadují použití elektronového svazku s energií >9 MeV, což zvyšuje dávku na kůži, vyvolává angiectasie a zhoršuje kosmetický efekt (7) a dále tam, kde je třeba aplikovat vyšší dávky, tj. 20 Gy při těsných či pozitivních okrajích.
Intersticiální boost má rovněž radiobiologické předpoklady k vyššímu efektu na nádorové buňky a to díky krátkému času, ze který je dávka aplikována a vysokým dávkám uvnitř PTV v důsledku heterogenní dávkové distribuce.
Publikovaná data však nejsou takto jednoznačná. Především chybí randomizovaná studie porovnávající zevní a intersticiální boost.
EORTC studie boost versus no boost zahrnovala 2661 pacientek randomizovaných do skupiny s boostem, buďto se zevním boostem 16 Gy nebo s intersticiálním boostem 15 Gy. 63 % pacientek bylo léčeno elektrony, 29 % fotony a 9 % brachyterapií. Intersticiální boost byl spojen s nesignifikantně vyšší lokální kontrolou a měl stejné výsledky ve smyslu fibrózy a kosmetického efektu jako zevní boost.
Od r. 1990 bylo publikováno 10 komparativních studií porovnávajících lokální kontrolu a kosmetický efekt zevního a intersticiálního boostu: De la Rochefordiere (8), Mansfield (9), Touboul (10), Perez (11), Wazer (12), Hammer (13), Polgar (14), Sarin (15), Frazier (15), Berberich (16).
Hodnocení těchto komparativních studií je nesnadné. Již výběr pacientek k brachyterapii či zevnímu boostu se liší. V Perezově studii byly k brachyterapii indikovány pacientky s tumorem v hloubce > 4 cm pod kůží či v přítomnosti pozitivních či neurčených resekčních okrajů. Ve studii Frazieriově byly pro brachyterapii indikovány případy s pozitivními nebo těsnými okraji, s extenzivní intraduktální komponentou, G3 tumory či velkými prsy. Wazer vybíral pro brachyterapii pacientky vyžadující boost 20 Gy. V Touboulově multicentrické studii jedna nemocnice léčila všechny pacientky intersticiálním boostem, ostatní pouze zevním ozářením. V ostatních studiích indikace k brachyterapii nejsou stanoveny.
Následující tabulka 1 prezentuje souhrnné výsledky komparativních studií:
Tab 1: Výsledky komparativních studií
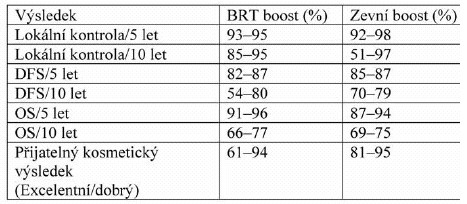
Lokální kontrola:
Většina prací (Frazier, Polgar, De la Rochefordiere, Perez, Berberich ) udává stejnou lokální kontrolu pro intersticielní i zevní boost. Ve Wazerově studii je uváděn nesignifikantně horší výsledek u intersticiální brachyterapie po 7 letech sledování, ale pacientky s intersticiálním boostem byly signifikantně mladší (51 let) než pacientky se zevním boostem (62 let) (p = 0,00001), přičemž je známo, že nižší věk je rizikovější z hlediska rizika lokálních recidiv.
Lepší lokální kontrola s brachyterapií je popsána Mansfieldem a Hammerem. Touboul uvádí nesignifikantně lepší lokální kontrolu u intersticiálního boostu, přičemž věkový průměr pacientek s brachyterapií byl opět signifikantně nižší než ve skupině se zevním boostem a pacientky podstoupily méně často kvadrantectomii.
Kosmetický efekt:
Práce z 80. let /Ray and Fish (18), Fowble (19), Olivotto (20)/ uváděly horší kosmetické výsledky s intersticiálním boostem, obsahovaly však malý počet pacientů, technika brachyterapie byla nedokonalá a byla rozdílná doba sledování pacientek s brachyterapií a intersticiálním boostem.
Z prací publikovaných po roce 1990 uvádí horší výsledky brachyterapie Berberich a Touboul. V první práci však byl celý prs pacientek s brachyterapií ozařován kobaltovým ozařovačem zatímco u pacientek s elektronovým boostem lineárním urychlovačem. Rovněž v publikaci Berberichově byly pacientky s intersticiálním boostem ozařovány na kobaltu dávkou na jednu frakci 2,5 Gy, zatímco pacientky se zevním boostem byly léčeny na lineárním urychlovači hyperfrakcionací 2x1,5 Gy denně. Medián sledování u pacientek s brachyterapií byl 9,4 roku a u pacientek se zevním boostem 4,2 roku.
Žádný rozdíl v kosmetickém efektu nezaznamenali De la Rochefordiere, Perez, Frazier, Polgar, Mansfield. Signifikantně lepší kosmetické výsledky s brachyterapií uvádějí Sarin, Wazer a Hammer.
Ve svém review z dubna 2006 uzavírá P. Graham, že není podstatný rozdíl ve výsledcích zevního či intersticiálního boostu, ale že intersticiální brachyterapie je výhodnější pro hlouběji uložené nádory.
LDR versus HDR:
Většina publikovaných prací užívala pro intersticiální boost brachyterapii s nízkým dávkovým příkonem a dávkami
15-20 Gy. Na řadě pracovišť je brachyterapie s nízkým dávkovým příkonem (LDR) nahrazována automatickými afterloadingovými přístroji s vysokým dávkovým příkonem (HDR), který má odlišnou radiobiologii. Zvláště velké jednotlivé frakce teoreticky zvyšují pravděpodobnost pozdních postradiačních změn a ztrácí se nezávislost na kyslíkovém efektu typická pro LDR. Proto vzniká otázka, zda použití HDR umožňuje dosažení stejných výsledků jako měla LDR brachyterapie.
Počet studií s HDR intersticiálním boostem u karcinomu prsu je limitovaný.
Tab. 2: Studie a HDR boostem:
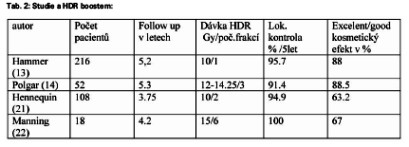
Dvě studie porovnávaly výsledky LDR a HDR boostu.
Reschová (23) porovnávala výsledky u 136 pacientek léčených LDR boostem 20 Gy a 274 pacientek léčených HDR boostem 10 Gy. Follow up bylo 8,7 roku. Pravděpodobnost desetileté lokální kontroly byla 98,5 % ve skupině s LDR i HDR. Kosmetický efekt nebyl porovnán.
V Guixově (24) studii byly porovnávány výsledky u 291 pacientek léčených LDR boostem a 284 pacientek léčených HDR. Pacientky s negativním okrajem 10 mm a bez intraduktální komponenty obdržely dávky 20 Gy LDR či 18 Gy HDR, s pozitivní intraduktální komponentou nebo okraji 5-10 mm 25 Gy LDR či 20 Gy HDR, pacientky s extenzivním carcinoma in situ nebo okraji < 5 mm dostaly 30 Gy LDR či 22 Gy HDR. HDR brachyterapie byla frakcionována do jednotlivých dávek 2-2,5 Gy.
Devítiletá lokální kontrola byla 87,5 % ve skupině s LDR a 91,4 % ve skupině HDR. Excelentní/dobrý kosmetický efekt byl 82 % pro LDR a 96 % pro HDR.
Lze uzavřít, že LDR i HDR boost mají výsledky obdobné. American Brachytherapy Society doporučuje intersticiální boost v následujících situacích:
těsné, pozitivní nebo neznámé okraje
přítomnost EIC
mladší pacientky (pod 40 let)
Řada autorů udává pozitivní okraje jako významný rizikový faktor pro lokální recidivu. V několika studiích s intersticiálním boostem byl tento negativní vliv pozitivních okrajů eliminován (Vicini, Polgar, Resch). Wazer nalezl stejnou lokální kontrolu u pacientek s okraji 2 mm a méně po zevním i intersticiálním boostu 20 Gy, pacientky s BRT měly signifikantně lepší kosmetický efekt.
Rovněž přítomnost EIC a mladší věk představují vyšší riziko lokální recidivy, které může být sníženo použitím intersticiálního boostu.
Pro lokální kontrolu a dobrý kosmetický efekt je vždy nutné respektovat několik základních pravidel:
Target volume pro boost je definován jako lůžko tumoru s okrajem 1-2 cm, při nekompletní resekci až 3 cm. Použití
6 chirurgických svorek v kombinaci s CT je patrně optimální metoda k určení cílového objemu, protože svorky a hranice lůžka mohou být vizualizovány řez od řezu. Vicini a Polgár zavedli 3D virtuální plánování BRT u karcinomu prsu založené na dvou seriích CT scanů před a poimplantačních. Jinou možností je zavedení afterloadingových kateterů intraoperačně, tato metoda však neprokázala ani lepší lokální kontrolu ani kosmetický efekt.
Kritické jsou dávky na kůži, měly by být co nejnižší jako prevence vzniku teleangiectasií. U LDR dávka předepsaná pro PTV musí být hlouběji než 5 mm od povrchu kůže, u HDR vzdálenost první a poslední pozice zdroje od kůže by měla být nejméně 10 mm.
Při referování o intersticiálním boostu by neměly chybět údaje o:
Mean Central Dose: aritmetický průměr minimálních dávek mezi zdroji v centrální rovině jednorovinného implantátu nebo uprostřed mezi trojúhelníky či čtverci vícerovinného implantátu.
Minimum Target Dose: dávka zvolená jako adekvátní pro PTV, tj. všechny body PTV by měly obdržet minimálně tuto dávku.
Reference Volume: objem zaujatý referenční isodosou, která je definována vztahem k Mean Central Dose. V Pařížském systému je to 85 % Mean Central Dose.
V150: objem zaujatý v 150 % Mean Central Dose.
Dose Homogeneity Index: poměr Minimum Target Dose a Mean Central Dose.
Samostatná brachyterapie:
Koncept zrychleného částečného ozáření prsu (accelerated partial breast irradiation APBI) vychází ze současných dat o nálezu lokálních recidiv v operovaném prsu. Řada prací potvrzuje, že lokální recidiva se objevuje ve většině případů
(60-80%) v původním lůžku nádoru. Vezmeme-li v úvahu, že procento lokálních recidiv po prs šetřících výkonech bez radioterapie je zhruba 35 % a z toho 80 % je v původním lůžku tumoru, vychází nám, že ozařování celého prsu je overtreatment pro 93 % pacientek.
Klinické studie se samostatnou brachyterapií po prs šetřících výkonech zahrnují jeden randomizovaný klinický trial /Polgar (25)/, tři kohortní studie s kontrolami /Vicini (26), King (27), Fentiman (28)/ a několik dalších retrospektivních či prospektivních studií bez kontrol.
Polgárova studie randomizovala 126 pacientů do skupiny léčené ozářením celého prsu do dávky 50 Gy a skupiny léčené radioterapií samotného lůžka tumoru, z toho 46 pacientů bylo léčeno HDR BT 7x 5,2 Gy a 17 pacientů elektronovým polem dávkou 50 Gy. Vstupní kriteria zahrnovala ženy se T1N0 karcinomem s negativními resekčními okraji a byly vyloučeny ženy s EIC. S mediánem sledování 57 měsíců nebyl signifikantní rozdíl v recidivách a kosmetickém efektu mezi oběma rameny.
V roce 2002 Polgár (29) publikoval komparativní studii porovnávající APBI vs. ozáření celého prsu, vs. ozáření celého prsu + boost s dobou sledování 81 měsíců (APBI) a 83 měsíců (kontrolní skupina). Vstupní kritéria zahrnovala pacientky s T1N0 N1mi (mikroskopické postižení) nelobulárním karcinomem bez přítomnosti extenzivní intraduktální komponenty a s negativními okraji. APBI spočívala v HDR BT 30,3 Gy a 36,4 Gy v 7 frakcích/4 dny. Sedmiletá pravděpodobnost recidivy byla bez signifikantního rozdílu ve všech 3 skupinách (9 %, 14,8 %, 9,5 %). Excelentní/dobré kosmetické výsledky byly
84,4 % ve skupině s APBI a 68,3 % v kontrolní skupině.
Rovněž Vicini (pětileté výsledky) a King (šestileté) neudávají statisticky významné rozdíly v lokoregionální kontrole ani kosmetických výsledcích mezi pacienty léčenými ozářením celého prsu nebo brachyterapií lůžka tumoru.
APBI nelze v současné době chápat jako standardní postup, protože nejsou k dispozici dostatečně dlouhodobé údaje. Každopádně dosavadní výsledky jsou slibné a nelze vyloučit, že budoucnu APBI nenahradí standardní ozáření celého prsu u selektovaných pacientek s nízkým rizikem. Pro APBI se používají dávky 45-50 Gy LDR/PDR nebo kolem
32-36 Gy frakcionované HDR BT. Pokud se provádí BT prsu samostatně, klade to mimořádné požadavky na kvalitu používané techniky léčby.
MammoSite:
MammoSite je nový brachyterapeutický aplikátor který významně zjednodušuje provedení brachyterapie. Principem je malý balónový kateter, který se zavede do resekční dutiny po tumorectomii. Je spojen s AFL přístrojem.
Technika provedení: po lumpectomii se zavede nenaplněný aplikátor do resekční dutiny. Poté je balónek aplikátoru naplněn fysiologickým roztokem a kontrastní látkou. Naplněný aplikátor těsně přiléhá k okrajům resekční dutiny. Dávka se předepisuje 1 cm od povrchu balonového kateteru, pohybuje se kolem 34 Gy v 10 frakcích 2x denně. Zdrojem záření je AFL přístroj.
Metoda si získává velkou popularitu. Proběhlé studie mají dosud krátkou dobu sledování (řádově v měsících) a demonstrují slibnou lokální kontrolu a kosmetické výsledky, ale vyšší výskyt akutní toxicity (30, 31, 32)
Závěry:
Intersticiální boost je indikován u pacientek s vyšším rizikem lokální recidivy a u nádorů lokalizovaných více než 28 mm pod kůží. LDR a HDR brachyterapie mají srovnatelné výsledky.
Samostatná brachyterapie pro parcial breast irradiation se jeví jako slibná metoda u pečlivě vybraných pacientek s nízkým rizikem lokální recidivy. Není však dosud standardní léčbou a měla by se používat jen v rámci studií.
MammoSite aplikátor představuje jednoduchou alternativu intersticiální brachyterapie u selektovaných pacientek, ale dosud chybí data na dostatečných souborech pacientek s delší dobou sledování.
Literatura:
Lokální kontrola je u karcinomu prsu významným faktorem pro celkové přežití, což bylo opakovaně prokázáno (3,4, 5, 6).
Boost je možné aplikovat zevně fotonovým nebo elektronovým svazkem nebo intersticiální brachyterapií. Od 80. let do poloviny 90. let pokleslo užívání intersticiálního boostu o 60 %, což souviselo s nahrazováním kobaltových ozařovačů lineárními urychlovači a rostoucí popularitou boostu elektronového. K tomu přistoupily přísnější požadavky na radiační ochranu, což vytlačovalo manuální afterloading.
Proč vůbec uvažovat o intersticiálním boostu, který je pracnější a náročnější než elegantní boost elektronový? Je několik teoretických důvodů, proč by měl být intersticiální boost výhodnější. Intersticiální boost je schopen léčit plánovací cílový objem (PTV) více konformě a redukovat objem ozářené prsní tkáně. V EORTC studii byl PTV pro boost v průměru 60 cm3 pro brachyterapii, 144 cm3 pro elektrony a 288 cm3 pro fotony.
Tato výhoda je zřejmá především pro tumory uložené hlouběji než 28 mm pod epidermis, které vyžadují použití elektronového svazku s energií >9 MeV, což zvyšuje dávku na kůži, vyvolává angiectasie a zhoršuje kosmetický efekt (7) a dále tam, kde je třeba aplikovat vyšší dávky, tj. 20 Gy při těsných či pozitivních okrajích.
Intersticiální boost má rovněž radiobiologické předpoklady k vyššímu efektu na nádorové buňky a to díky krátkému času, ze který je dávka aplikována a vysokým dávkám uvnitř PTV v důsledku heterogenní dávkové distribuce.
Publikovaná data však nejsou takto jednoznačná. Především chybí randomizovaná studie porovnávající zevní a intersticiální boost.
EORTC studie boost versus no boost zahrnovala 2661 pacientek randomizovaných do skupiny s boostem, buďto se zevním boostem 16 Gy nebo s intersticiálním boostem 15 Gy. 63 % pacientek bylo léčeno elektrony, 29 % fotony a 9 % brachyterapií. Intersticiální boost byl spojen s nesignifikantně vyšší lokální kontrolou a měl stejné výsledky ve smyslu fibrózy a kosmetického efektu jako zevní boost.
Od r. 1990 bylo publikováno 10 komparativních studií porovnávajících lokální kontrolu a kosmetický efekt zevního a intersticiálního boostu: De la Rochefordiere (8), Mansfield (9), Touboul (10), Perez (11), Wazer (12), Hammer (13), Polgar (14), Sarin (15), Frazier (15), Berberich (16).
Hodnocení těchto komparativních studií je nesnadné. Již výběr pacientek k brachyterapii či zevnímu boostu se liší. V Perezově studii byly k brachyterapii indikovány pacientky s tumorem v hloubce > 4 cm pod kůží či v přítomnosti pozitivních či neurčených resekčních okrajů. Ve studii Frazieriově byly pro brachyterapii indikovány případy s pozitivními nebo těsnými okraji, s extenzivní intraduktální komponentou, G3 tumory či velkými prsy. Wazer vybíral pro brachyterapii pacientky vyžadující boost 20 Gy. V Touboulově multicentrické studii jedna nemocnice léčila všechny pacientky intersticiálním boostem, ostatní pouze zevním ozářením. V ostatních studiích indikace k brachyterapii nejsou stanoveny.
Následující tabulka 1 prezentuje souhrnné výsledky komparativních studií:
Tab 1: Výsledky komparativních studií

Lokální kontrola:
Většina prací (Frazier, Polgar, De la Rochefordiere, Perez, Berberich ) udává stejnou lokální kontrolu pro intersticielní i zevní boost. Ve Wazerově studii je uváděn nesignifikantně horší výsledek u intersticiální brachyterapie po 7 letech sledování, ale pacientky s intersticiálním boostem byly signifikantně mladší (51 let) než pacientky se zevním boostem (62 let) (p = 0,00001), přičemž je známo, že nižší věk je rizikovější z hlediska rizika lokálních recidiv.
Lepší lokální kontrola s brachyterapií je popsána Mansfieldem a Hammerem. Touboul uvádí nesignifikantně lepší lokální kontrolu u intersticiálního boostu, přičemž věkový průměr pacientek s brachyterapií byl opět signifikantně nižší než ve skupině se zevním boostem a pacientky podstoupily méně často kvadrantectomii.
Kosmetický efekt:
Práce z 80. let /Ray and Fish (18), Fowble (19), Olivotto (20)/ uváděly horší kosmetické výsledky s intersticiálním boostem, obsahovaly však malý počet pacientů, technika brachyterapie byla nedokonalá a byla rozdílná doba sledování pacientek s brachyterapií a intersticiálním boostem.
Z prací publikovaných po roce 1990 uvádí horší výsledky brachyterapie Berberich a Touboul. V první práci však byl celý prs pacientek s brachyterapií ozařován kobaltovým ozařovačem zatímco u pacientek s elektronovým boostem lineárním urychlovačem. Rovněž v publikaci Berberichově byly pacientky s intersticiálním boostem ozařovány na kobaltu dávkou na jednu frakci 2,5 Gy, zatímco pacientky se zevním boostem byly léčeny na lineárním urychlovači hyperfrakcionací 2x1,5 Gy denně. Medián sledování u pacientek s brachyterapií byl 9,4 roku a u pacientek se zevním boostem 4,2 roku.
Žádný rozdíl v kosmetickém efektu nezaznamenali De la Rochefordiere, Perez, Frazier, Polgar, Mansfield. Signifikantně lepší kosmetické výsledky s brachyterapií uvádějí Sarin, Wazer a Hammer.
Ve svém review z dubna 2006 uzavírá P. Graham, že není podstatný rozdíl ve výsledcích zevního či intersticiálního boostu, ale že intersticiální brachyterapie je výhodnější pro hlouběji uložené nádory.
LDR versus HDR:
Většina publikovaných prací užívala pro intersticiální boost brachyterapii s nízkým dávkovým příkonem a dávkami
15-20 Gy. Na řadě pracovišť je brachyterapie s nízkým dávkovým příkonem (LDR) nahrazována automatickými afterloadingovými přístroji s vysokým dávkovým příkonem (HDR), který má odlišnou radiobiologii. Zvláště velké jednotlivé frakce teoreticky zvyšují pravděpodobnost pozdních postradiačních změn a ztrácí se nezávislost na kyslíkovém efektu typická pro LDR. Proto vzniká otázka, zda použití HDR umožňuje dosažení stejných výsledků jako měla LDR brachyterapie.
Počet studií s HDR intersticiálním boostem u karcinomu prsu je limitovaný.
Tab. 2: Studie a HDR boostem:

Dvě studie porovnávaly výsledky LDR a HDR boostu.
Reschová (23) porovnávala výsledky u 136 pacientek léčených LDR boostem 20 Gy a 274 pacientek léčených HDR boostem 10 Gy. Follow up bylo 8,7 roku. Pravděpodobnost desetileté lokální kontroly byla 98,5 % ve skupině s LDR i HDR. Kosmetický efekt nebyl porovnán.
V Guixově (24) studii byly porovnávány výsledky u 291 pacientek léčených LDR boostem a 284 pacientek léčených HDR. Pacientky s negativním okrajem 10 mm a bez intraduktální komponenty obdržely dávky 20 Gy LDR či 18 Gy HDR, s pozitivní intraduktální komponentou nebo okraji 5-10 mm 25 Gy LDR či 20 Gy HDR, pacientky s extenzivním carcinoma in situ nebo okraji < 5 mm dostaly 30 Gy LDR či 22 Gy HDR. HDR brachyterapie byla frakcionována do jednotlivých dávek 2-2,5 Gy.
Devítiletá lokální kontrola byla 87,5 % ve skupině s LDR a 91,4 % ve skupině HDR. Excelentní/dobrý kosmetický efekt byl 82 % pro LDR a 96 % pro HDR.
Lze uzavřít, že LDR i HDR boost mají výsledky obdobné. American Brachytherapy Society doporučuje intersticiální boost v následujících situacích:
těsné, pozitivní nebo neznámé okraje
přítomnost EIC
mladší pacientky (pod 40 let)
Řada autorů udává pozitivní okraje jako významný rizikový faktor pro lokální recidivu. V několika studiích s intersticiálním boostem byl tento negativní vliv pozitivních okrajů eliminován (Vicini, Polgar, Resch). Wazer nalezl stejnou lokální kontrolu u pacientek s okraji 2 mm a méně po zevním i intersticiálním boostu 20 Gy, pacientky s BRT měly signifikantně lepší kosmetický efekt.
Rovněž přítomnost EIC a mladší věk představují vyšší riziko lokální recidivy, které může být sníženo použitím intersticiálního boostu.
Pro lokální kontrolu a dobrý kosmetický efekt je vždy nutné respektovat několik základních pravidel:
Target volume pro boost je definován jako lůžko tumoru s okrajem 1-2 cm, při nekompletní resekci až 3 cm. Použití
6 chirurgických svorek v kombinaci s CT je patrně optimální metoda k určení cílového objemu, protože svorky a hranice lůžka mohou být vizualizovány řez od řezu. Vicini a Polgár zavedli 3D virtuální plánování BRT u karcinomu prsu založené na dvou seriích CT scanů před a poimplantačních. Jinou možností je zavedení afterloadingových kateterů intraoperačně, tato metoda však neprokázala ani lepší lokální kontrolu ani kosmetický efekt.
Kritické jsou dávky na kůži, měly by být co nejnižší jako prevence vzniku teleangiectasií. U LDR dávka předepsaná pro PTV musí být hlouběji než 5 mm od povrchu kůže, u HDR vzdálenost první a poslední pozice zdroje od kůže by měla být nejméně 10 mm.
Při referování o intersticiálním boostu by neměly chybět údaje o:
Mean Central Dose: aritmetický průměr minimálních dávek mezi zdroji v centrální rovině jednorovinného implantátu nebo uprostřed mezi trojúhelníky či čtverci vícerovinného implantátu.
Minimum Target Dose: dávka zvolená jako adekvátní pro PTV, tj. všechny body PTV by měly obdržet minimálně tuto dávku.
Reference Volume: objem zaujatý referenční isodosou, která je definována vztahem k Mean Central Dose. V Pařížském systému je to 85 % Mean Central Dose.
V150: objem zaujatý v 150 % Mean Central Dose.
Dose Homogeneity Index: poměr Minimum Target Dose a Mean Central Dose.
Samostatná brachyterapie:
Koncept zrychleného částečného ozáření prsu (accelerated partial breast irradiation APBI) vychází ze současných dat o nálezu lokálních recidiv v operovaném prsu. Řada prací potvrzuje, že lokální recidiva se objevuje ve většině případů
(60-80%) v původním lůžku nádoru. Vezmeme-li v úvahu, že procento lokálních recidiv po prs šetřících výkonech bez radioterapie je zhruba 35 % a z toho 80 % je v původním lůžku tumoru, vychází nám, že ozařování celého prsu je overtreatment pro 93 % pacientek.
Klinické studie se samostatnou brachyterapií po prs šetřících výkonech zahrnují jeden randomizovaný klinický trial /Polgar (25)/, tři kohortní studie s kontrolami /Vicini (26), King (27), Fentiman (28)/ a několik dalších retrospektivních či prospektivních studií bez kontrol.
Polgárova studie randomizovala 126 pacientů do skupiny léčené ozářením celého prsu do dávky 50 Gy a skupiny léčené radioterapií samotného lůžka tumoru, z toho 46 pacientů bylo léčeno HDR BT 7x 5,2 Gy a 17 pacientů elektronovým polem dávkou 50 Gy. Vstupní kriteria zahrnovala ženy se T1N0 karcinomem s negativními resekčními okraji a byly vyloučeny ženy s EIC. S mediánem sledování 57 měsíců nebyl signifikantní rozdíl v recidivách a kosmetickém efektu mezi oběma rameny.
V roce 2002 Polgár (29) publikoval komparativní studii porovnávající APBI vs. ozáření celého prsu, vs. ozáření celého prsu + boost s dobou sledování 81 měsíců (APBI) a 83 měsíců (kontrolní skupina). Vstupní kritéria zahrnovala pacientky s T1N0 N1mi (mikroskopické postižení) nelobulárním karcinomem bez přítomnosti extenzivní intraduktální komponenty a s negativními okraji. APBI spočívala v HDR BT 30,3 Gy a 36,4 Gy v 7 frakcích/4 dny. Sedmiletá pravděpodobnost recidivy byla bez signifikantního rozdílu ve všech 3 skupinách (9 %, 14,8 %, 9,5 %). Excelentní/dobré kosmetické výsledky byly
84,4 % ve skupině s APBI a 68,3 % v kontrolní skupině.
Rovněž Vicini (pětileté výsledky) a King (šestileté) neudávají statisticky významné rozdíly v lokoregionální kontrole ani kosmetických výsledcích mezi pacienty léčenými ozářením celého prsu nebo brachyterapií lůžka tumoru.
APBI nelze v současné době chápat jako standardní postup, protože nejsou k dispozici dostatečně dlouhodobé údaje. Každopádně dosavadní výsledky jsou slibné a nelze vyloučit, že budoucnu APBI nenahradí standardní ozáření celého prsu u selektovaných pacientek s nízkým rizikem. Pro APBI se používají dávky 45-50 Gy LDR/PDR nebo kolem
32-36 Gy frakcionované HDR BT. Pokud se provádí BT prsu samostatně, klade to mimořádné požadavky na kvalitu používané techniky léčby.
MammoSite:
MammoSite je nový brachyterapeutický aplikátor který významně zjednodušuje provedení brachyterapie. Principem je malý balónový kateter, který se zavede do resekční dutiny po tumorectomii. Je spojen s AFL přístrojem.
Technika provedení: po lumpectomii se zavede nenaplněný aplikátor do resekční dutiny. Poté je balónek aplikátoru naplněn fysiologickým roztokem a kontrastní látkou. Naplněný aplikátor těsně přiléhá k okrajům resekční dutiny. Dávka se předepisuje 1 cm od povrchu balonového kateteru, pohybuje se kolem 34 Gy v 10 frakcích 2x denně. Zdrojem záření je AFL přístroj.
Metoda si získává velkou popularitu. Proběhlé studie mají dosud krátkou dobu sledování (řádově v měsících) a demonstrují slibnou lokální kontrolu a kosmetické výsledky, ale vyšší výskyt akutní toxicity (30, 31, 32)
Závěry:
Intersticiální boost je indikován u pacientek s vyšším rizikem lokální recidivy a u nádorů lokalizovaných více než 28 mm pod kůží. LDR a HDR brachyterapie mají srovnatelné výsledky.
Samostatná brachyterapie pro parcial breast irradiation se jeví jako slibná metoda u pečlivě vybraných pacientek s nízkým rizikem lokální recidivy. Není však dosud standardní léčbou a měla by se používat jen v rámci studií.
MammoSite aplikátor představuje jednoduchou alternativu intersticiální brachyterapie u selektovaných pacientek, ale dosud chybí data na dostatečných souborech pacientek s delší dobou sledování.
Literatura:
- Romestaing P., Lehingue Y., Carrie C.: Role of 10 Gy boost in the conservative treatmnent of early breast cancer: Results of a randomized clinical trial in Lyon, France, J. Clin Oncol 1997, 15, 963-968.
- Poortmans .P., Bartelink .H, Horiot J. C.: The influence of the boost technique on local control in breast copnserving treatment in the EORTC boost versus no boost randomised trila. Radiothe Oncol 2004, 72, 25-33.
- Fisher .B, Anderson .S, Redmond C. K., et al.: Reanalysis and results after 12 yeary of follow up in a randomized clinical trial comparing total mastectomy with lumpectomy with or without irradiation in the treatment of breast cancer. N Engl J Med 1995, 333, 156 162
- Koscielny S., Tubiana M.: The link between local recurrence and
distant metastasis in human breast cancer. Int J Radiat
Oncol Biol Phys 1999, 1, 11-24. - Overgaard M., Hansen P. S., Overgaard J., et al.: Postopeerative radiotherapy in high risk premenopausal women with breast cancer who receive adjuvant chemotherapy. N Engl Med 1997, 337, 949-955.
- Sauer R.: Influence of local control to overall survival a#fter
breast conseving therapy of breast cancer. Strahlenther Onkol 1996,
172, 181-185.
- Van Limbergen .E, Reynders .A, Van den Bogaert .W: The useful boost range concep judges the ballistic selectivity of electron beams versus brachytherapy in the boost technique of breast conserving therapy Eur J Cancer 1998, 34 (suppl 5), 57.
- De la Rochefordiere .A, Abner A. L., Silver B., et al.: Are cosmetic results following conservative surgery and radiation therapy for early breast cancer dependent on technique? Int J Radiat Oncol Biol Phys 1992, 23, 925-931.
- Mansfield C. M., Komarnicky L. T., Schwartz G. F., et al.: Ten year results in 1070 patients with stages I and II breast cancer treated by conservative surgery and radiation therapy Cancer 1995, 75, 2328-2336.
- Touboul E., Belkacemi Y., Lefranc J. P., et al.: Early breast
cancer: influence of type of boost (electrons vs iridium -192
implant) on local control and cosmesis after conservative surgery and radiation therapy . Radiother Oncol 1995, 34, 105-113. - Perez C. A., Taylor M. E., Halverson K., et al.: Brachytherapy or electron beam boost in conservation therapy of carcinoma of the breast: A non-randomized comparison. Int J radiat Oncol Biol Phys 1996, 34, 995-1007.
- Wazer D. E., Kramer B., Schmid C., et al.: Factors determining outcome in patients treated with interstitial implantation as a radiation boost for breast conservation therapy. Int J radiat Oncol Biol Phys 1997, 39, 381-393.
- Hammer J., Seewald D. H., Track C., et al.: Breast cancer : primary treatment with external beam-radiation therapy and high-dose-rate iridium implantation. Radiology 1994, 193, 573-577
- Polgar C., Fodor J., Orosz Z., et al.: Electron and high-dose-rate brachytherapy boost in the conservative treatment of stage I-II breast cancer . First resuslts of the randomized Budapest boost trila. Strahlenther Onkol 2002, 178,. 615-623.
- Sarin R., Dinshaw K. A., Shrivastava, et al.: Therapeutic
factor influencing the cosmetic outome and late complications in
the conservative management of early breast cancer. Int J Radiat
Oncol Biol Phys 1993, 27, 285-292.
- Frazier R. C., Kestin L. L., Kini V., et al.: Ompact of boost technique on outome in early-stage breast cancer patients with breast-conserving therapy. Am J Clin Oncol, 2001, 24, 26-32.
- Berberich W., Schnabel K., Berg D.: Boost irradiation of breast carcinoma: teletherapy vs brachytherapy: Eur J Obstet Gynecol Reprod Bio, 2001, 94, 276-282.
- Ray G. R., Fish V. J.: Biopsy and definitive radiation therapy in stage I and II adenocarcinoma of the female breast: analysis of cosmesis and the role of electron beam supplementation. Int J Radiat Oncol Biol Phys 1983, 9, 813-818.
- Fowble B., Solin L. J., Martz K. L., et al.: The influence of the type of boost (electrons vs implant) on local control and cosmesis in patients with stages I and II breast cancer undegoing conservative surgery and radiation Int J Radiat Oncol Biol Phys 1986, 12, 150 (abstract).
- Olivotto I. A., Rose M. A., Osteen R. T., et al.: Late cosmetic outciome after conservative surgery and radiotherapy: analysis of causes of cosmetic failure. Int J Radiat Oncol Biol Phys 1989, 17, 747-753.
- Hennequin C., Durdux C., Espi M., et al.: High dose rate
brachytherapy for early breast cancer: an ambulatory technique. Int
J Radiat Oncol Biol Phys 1999, 45, 85-90.
- 22. Manning M. A., Arthur D. W., Schmidt-Ullrich R. K., et al.: Interstitial high doserate brachytherapy boost: the feasibility and cosmetic outcome of a fractionated outpatient delivery scheme. Int J Radiat Oncolo Biol Phys 2000, 48, 1301-1306.
- Resch A., Potter R., Limbergen E., et al.: Long-term results (10 year) of intensive breast conserving therapy including a high-dose and large-volume interstitial brachytherapy boost (LDR/HDR) for T1/2 breast cancer. Radioth Oncol 2002, 63, 47-58.
- Guix B, Finestres F, Henríquez I: Comparison between LDR and HDR brachytherapy boost to the tumor bed in the conservative treatment of stage I and II breast cancer. Int J Radiat Oncolo Biol Phys 2001, 51, 4-6.
- Polgár C., Sulyok Z., Fodor J., et al.: Sole brachytherapy of the tumor bed after conservative surgery for T1 breast cancer: Five year results of phase I II study and initial finding of a randomized phase III trial. Journal of Surgical Oncology, 2002, 80, 121-128.
- Vicini F. A., Baglan K. L., Kestin L. L.: Accelerated treatment of breast cancer. J Clin Oncol, 2001, 19, 1993-2001.
- 27. Kong T. A., Bolton J. S., Kuske R. R.: Long term results of wide-field brachytherapy as the sole method of radiation therapy after segmental mastectomy for T(is, 1, 2) breast cancer. Am J Surg 2000, 180, 299-304.
- Fentiman I. S., Poole C., Tong D., et al.: Iridium implant treatment without external radiotherapy for operable breast cancer: a pilot study. Eur J Cancer 1991, 27, 447-450.
- Polgar C., Major T., Fodor J., et al.: High-dose-rate brachytherapy alone versus whole breast radiotherapy with or without tumor bed boost after breast conserving surgery: Seven year results of a comparative study. Int J Radiat Oncol Biol Phys 2004, 60, 1173-1181.
- Dowlatshahi K., Snider H. C., Gittleman M. A.: Early experience with balloon brachytherapy for breast cancer . Arch Surg 2004, 139, 603-608.
- Keisch M., Vicini F., Scroggins T.: Thirty month results with the MammoSite breast brachytherapy applicator: cosmesis, toxicity and local control uin partial breast irradiation, Int J Radiat Oncolo Biol Phys 2004, 60, 272.
- 32. Vicini F. A., Beitsch P. D., Quiet C. A.: First analysis of patient demographics, technical reproducibility, cosmesis and early toxicity: results of the American Society of Breast Surgeons MammoSite breast brachytherapy trial, Cancer 2005, 104, 1138-1148.
Datum přednesení příspěvku: 20. 10. 2006
