Konference: 2004 XXVIII. Brněnské onkologické dny a XVIII. Konference pro sestry a laboranty
Kategorie: Onkologická diagnostika
Téma: Molekulární a laboratorní diagnostika nádorů
Číslo abstraktu: 44
Autoři: J. Zelená; Jan Vacek; Mgr. Jitka Petrlová, Ph.D.; J. Hradecký; doc.Ing. René Kizek, Ph.D.
Kalibrační křivka byla lineární (y = 0,5582x m+ 3,0414) v rozsahu 4 až 200 µg MT/ml s R2 = 0,9989. Vyvinutá metodika významně přispívá k možnostem detekce MT markeru pomocí průtokové analýzy s elektrochemickou detekcí.
Klíčová slova
metalothionein, nadměrná exprese, prognostický marker, stanovení MT, elektrochemické metody, průtoková injekční analýza, FIA, chronopotenciometrická rozpouštěcí analýza, elektrochemický detektor
Zkratky
MT: metalothionein, hMT: lidský metalothionein, SH: sulfhydrylová skupina, HPLC: vysoko-účinná kapalinová chromatografie, DPV: diferenční pulzní voltametrie, AdTS CPSA: adsorptivní přenosová technika kombinovaná s chronopotenciometrickou rozpouště cí analýzou za konstantního proudu, ED: elektrochemický detektor, TFA: kys. trifluorooctová, ACN: acetonitril, FIA: průtoková injekční analýza.
1. Úvod
Metalothioneiny (MT) patří do skupiny intracelulárních na cystein bohatých proteinů o molekulové hmotnosti od 6 do 10 kDa. Díky své vysoké afinitě k zinku, mědi nebo kadmiu, je jejich hlavní funkcí homeostatická kontrola a detoxikace iontů těžkých kovů na buněčné úrovni. MT jsou rozděleny do tříd MT-I a MT-II s ohledem na jejich primární strukturu a organismus, ze kterého byly izolovány. Třída MT-I zahrnuje savčí metalothioneiny tvořené 61-68 aminokyselinami. V těchto proteinech nejsou přítomny aromatické aminokyseliny a 20 cysteinů se v primární sekvenci vyskytuje nejčastěji v těchto repeticích: Cys-X-Cys, Cys-Cys-X-Cys-Cys, Cys-X-Cys-Cys (X: jiná aminokyselina než abcystein). MT se skládají ze dvou vazebných domén (α, β), které jsou složeny z cysteinových molekul přičemž kovalentní vazby atomů kovů se účastní sulfhydrylové (SH) zbytky. N-terminální bčást peptidu je označena jako β-doména a má tři vazebná místa. V případě α-domény (C-terminální části) byla potvrzena schopnost vyvázat čtyři ionty kovů (obr.1) (Kägi and Kojima, 1987).
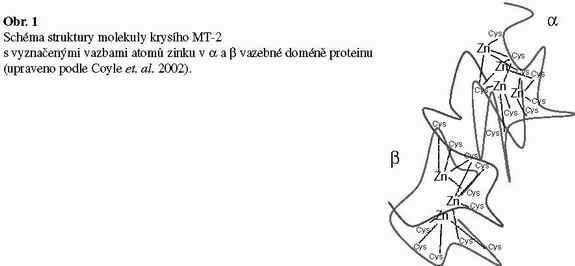
Isoformy metalothioneinů a jejich exprese v lidské tkáni
Lidské MT jsou kódovány rodinou genů vytvářejících 10 isoforem. Vzniklé proteiny jsou rozděleny do čtyř skupin: hMT-1, hMT-2, hMT-3 a hMT-4. V organismu dospělých jedinců jsou nejvíce zastoupeny isoformy hMT-1a a hMT-2a, které se exprimují ve většině lidských tkáních (Vašák and Hasler, 2000). Tyto isoformy jsou obvykle exprimovány ve velmi malých koncentracích a jejich exprese výrazně stoupá při indukci mnoha exogenními a endogenními faktory jako jsou těžké kovy (Cd, Cu, Pt, Zn, Pb aj.), stresové hormony, kyslíkové radikály, cytokininy a nejrůznější xenobiotika (Kägi, 1993).
Spojitost nadměrné exprese hMT s progresí onemocnění
V posledních deseti letech je zkoumána nadměrná exprese (overexprese) hMT v nádorových tkání. Tato exprese je převážně spojena s maligními nádory a je studována jako nový prognostický marker v progresi onemocnění, přežití pacientů, korelací s histologickým typem nádoru a nádorovým gradingem. (Cardoso et. al. 2002; Douglas-Jones et. al. 1995; Weinlich et. al. 2003; Jasani and Schmid 1997; Joseph et. al. 2001; Kuo and Lo 1997) Overexprese hMT je nejčastěji detekována imunohistochemicky v parafínových řezech s použitím monoklonální myší protilátky E9 proti isoformám hMT-1a a hMT-2a (Jasani and Elmes 1993). Hladina těchto isoforem převážně stoupá u maligních, více gradingovaných nádorů u karcinomu prsu, u kožních karcinomů a melanomů, cervikálních karcinomů, akutní lymfoblastické leukémie, karcinomů pankreatu a je významně spojena s progresí a horší prognózou v nádorovém onemocnění (Jasani and Schmid 1997). Naopak nadměrná exprese hMT sdružená s méně gradingovanými nádory byla určena u karcinomu tlustého střeva, karcinomu močového měchýře a fibroblastických kožních nádorů (Jasani and Schmid 1997).
Stanovení MT
Ke stanovení MT je využíváno široké spektrum metod chemické analýzy (Dabrio et. al. 2002), viz. obr. 2. K separaci MT se nejčastěji využívají chromatografické metody, které lze rozdělit na dvě skupiny. Jednak jde o metody využívající separace za vyššího tlaku (HPLC). Jako stacionární fáze se zde často využívá reverzních fází s chemicky vázaným oktylem nebo oktadecylem v kombinaci s polární mobilní fází. Pro detekci se obvykle využívá UV-Vis detektor diodového pole. Druhou skupinu představuje metoda nízkotlaké chromatografie: FPLC (vylučovací chromatografie), kde separace probíhá na základě rozdílné molekulové hmotnosti látek obsažených ve vzorku. Kromě nejběžněji používané UV-Vis detekce lze úspěšně stanovit nízké koncentrace MT elektrochemickými metodami. Elektrochemické metody jako je voltametrie zapojená v diferenčním pulzním módu (DPV) nebo derivativní chronopotenciometrie s konstantním proudem (CPSA) umožň ují stanovení nanomolárních koncentrací MT. Tyto analytické postupy vycházejí z elektrodových reakcí, které jsou provázeny vylučováním vodíku ze složek základního elektrolytu. CPSA v kombinací s technikou adsorptivního přenosu (AdTS) umožň uje stanovovat koncentrace MT na úrovni femtomolů ve velmi malých mobjemech (jednotky µl) vzorku.
Obr. 2.
Analytické instrumentální metody používané pro separaci a detekci MT. Více podrobností je uvedeno v práci.
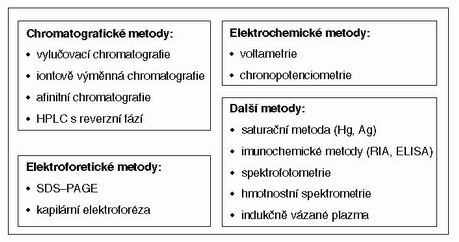
V naší práci jsme se zaměřili na stanovení MT pomocí chronoptenciometrické rozpouštěcí analýzy na rtuťové kapkové elektrodě a průtokové injekční analýzy s elektrochemickou detekcí.
2. Materiál a metody
Chemikálie
Acetonitril (ACN) a kyselina trifluorooctová (TFA) byly získány od firmy Merck (Darmstadt, Germany). Zásobní roztoky standardu metalothioneinu (MT-1a, izolát z králičích jater, Mr 7120 Da) v mkoncentraci 400 g/ml byly připraveny v ACS vodě (Aldrich, USA) a uchovány při –20°C. Pracovní roztoky byly ze zásobního připravovány každý den nové.
Elektrochemická analýza
Chronopotenciometrická rozpouštěcí analýza (CPSA) byla prováděna pomocí elektrochemického analyzátoru AUTOLAB (EcoChemie, Netherlands) v zapojení s tříelektrodovou celou VA-Stand 663 (Metrohm, Switzerland). Pracovní elektroda – HMDE (plocha rtuťové kapky: 0.4 mm2), referenční elektroda (Ag/AgCl, 3M KCl) a platinový drátek jako pomocná elektroda. Získaná data byla upravena matematickou korekcí podle algoritmů navržených Savitzkym a Golayem implementovaných do GPES softwaru (EcoChemie). Experimenty byly prováděny při laboratorní teplotě. Jako základní elektrolyt jsme použili borátový pufr pH 7,6 (0,05 mM Na2B4O7 + 0,1 M H3BO3). Parametry měření: rozpouštěcí proud –1 µA, doba akumulace 120 s, kondiční potenciál –0,1 V.
Průtoková analýza (FIA-ED)
FIA-ED systém byl složen ze dvou chromatografických pump (Model 582, ESA, USA), 1 m dlouhé reakční smyčky a osmikanálového CoulArray elektrochemického detektoru (Model 5600A, ESA, USA). Detektor je složen z průtočné analytické komůrky (Model 6210, ESA, USA) obsahující referenční, pomocnou (Pd) a osm porézních grafitových elektrod. Čištění povrchu elektrod od produktů elektrolýzy bylo prováděno elektrochemicky vkládáním pozitivních potenciálu na všechny elektrody (1 V) za vyššího průtoku mobilní fáze (1 ml/min). V samostatném modulu je uložena reakční smyčka, elektrochemický detektor, prostor je termostatovaný (35°C). mVzorek (5 µl) byl injektován manuálně přes dávkovací ventil.
3. Výsledky a diskuse
Současný vývoj analytických metod využívaných pro stanovení MT byl popsán v souhrnné práci Dabrio, M. et al.. V klinické praxi je nejvíce rozšířená analýza MT pomocí imunologických technik (ELISA, RIA). Metodou ELISA je možné stanovovat kolem 100 ng mMT/100 µl vzorku (Tang et. al. 1999). Vzhledem k problematické přípravě protilátek je snaha vyvíjet metody, které by byly stejně selektivní ke stanovovaným isoformám MT jako je ELISA. Jednou z možností je využití kapalinové chromatografie a nebo kapilární elektroforézy. (Minami et. al. 2002) Podle našich předešlých elektrochemických studií s proteiny (Kizek et. al. 2001; Kizek et. al. 2004; Strouhal et. al. 2003; Trnkova et. al. 2002), předpokládáme, že využití FIA nebo HPLC v kombinaci s elektrochemickou detekcí výrazně zlepší možnosti citlivé detekce MT v biologických vzorcích.
Elektrochemické měření
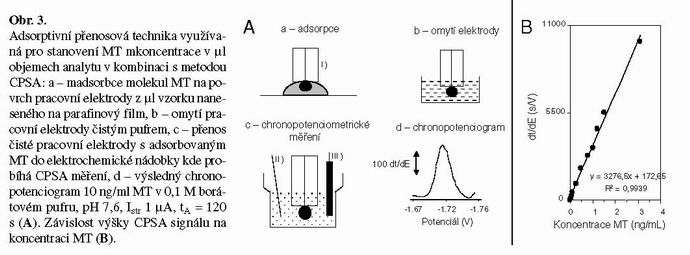
Elektroanalytické stanovení studovaného analytu má řadu výhod, mezi které zcela jistě patří rychlost, velmi dobrá citlivost, reprodukovatelnost a finanční nenáročnost metody. V našich dřívějších experimentech jsme se zabývali stanovením MT pomocí elektrochemické metody CPSA ve spojení s adsorptivní přenosovou technikou (AdTS) (Kizek et. al. 2001; Strouhal et. al. 2003; Trnkova et. al. 2002). MT byl nejdříve akumulován na pracovní povrch rtuťové elektrody, interferující látky odmyty roztokem pufru a elektroda s adsorbovaným MT je přenesena do základního elektrolytu kde probíhá samotné stanovení (Obr. 3A). Při měření 10 ng MT/ml poskytuje metoda AdTS CPSA velmi dobře vyvinutý a symetrický katalytický signál (Obr. 3A-d). Jak je patrno na obrázku 3B je závislost koncentrace MT na výšce signálu lineární (y = 3276,5x + 172,65; R2 = 0,9939). Cílem této práce bylo stanovení MT v průtokovém systému ve spojení s elektrochemickým detektorem (FIA-ED). Multi-elektrodový elektrochemický detektor obsahuje osm porézních grafitových elektrod zapojených v tandemovém uspořádání a na každou z těchto elektrod je možné vložit konstantní potenciál. V tomto zapojení bylo možné studovat oxidační signály MT. Je známo, že na uhlíkových elektrodách proteiny poskytují oxidační signály. (Dabrio et. al. 2002)
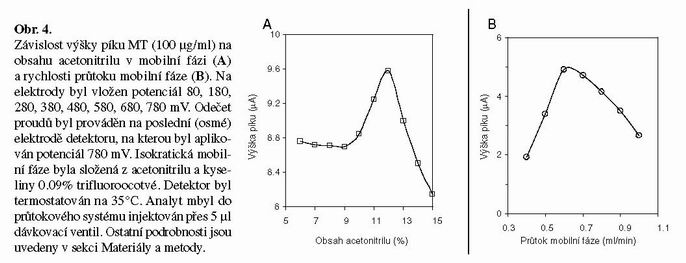
Vliv celkového průtoku mobilní fáze a koncentrace acetonitrilu
Pomocí FIA-ED bylo provedeno základní studium chování králičího MT-1a na uhlíkových porézních elektrodách elektrochemického detektoru. Protože klasické elektrochemické stanovení vyžaduje přítomnost elektrolytu (Březina and Zuman 1952), testovali jsme vliv poměru acetonitrilu a 0,09% kyseliny trifluorooctové na elektrochemickou odpověď analytu. ACN a TFA jsou často používanou součástí mobilní fáze při HPLC separaci, proto je vhodné testovat jejich vliv na elektrodové děje probíhající na elektrodovém systému detektoru. Získaná závislost poměru acetonitrilu a 0,09% TFA ve FIA mobilní fázi ukazuje maximální odpověď na detektoru při obsahu 11-12% ACN. Negativní vliv vyšší koncentrace acetonitrilu na studovaný signál může být způsoben změnou struktury MT a případným zhoršením elektrochemického chování studované látky (Obr. 4A). Důležitým parametrem pro získání maximální odezvy na elektrochemickém detektoru je celkový průtok mobilní fáze. Testovali jsme průtok mobilní fáze od 0,3 do 1 ml. Maximální odezvy jsme získali při průtoku 0,6 ml/min. Při vyšším průtoku se již proudová odezva snižuje a to pravděpodobně díky omezenému času prekoncentrace molekul MT na povrchu pracovních elektrod. Naproti tomu proudové odezvy zaznamenané v oblasti 0,6 ml/min rychlosti průtoku pravděpodobně souvisí s možností saturace aktivního povrchu elektrody čímž dochází ke zvýšení sledovaného signálu (obr. 4B).
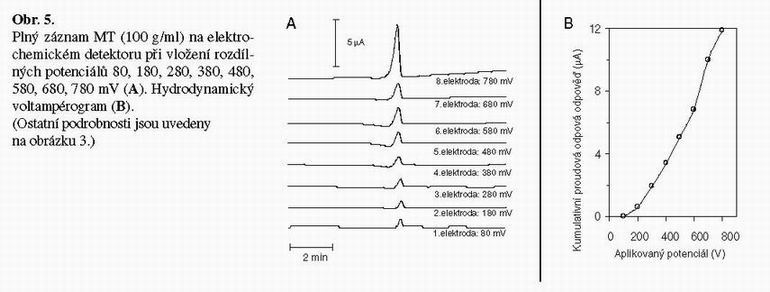
Vliv aplikovaného potenciálu na pracovní elektrody
Byl studován vliv aplikovaného potenciálu na pracovní elektrody při již známém průtoku mobilní fáze 0,6 ml/min, vhodném poměru mobilní fáze (12% ACN a 88% 0,09% TFA) a teplotě detektoru 35°C. Pro nalezení vhodného potenciálu oxidace stanovovaného MT byl na grafitové porézní elektrody detektoru vkládán potenciál 80, 180, 280, 380, 480, 580, 680 a 780 mV. Získané elektrochemické signály 100 ng MT/ml na jednotlivých elektrodách detektoru jsou ukázány na obrázku 5A. Z uvedených signálů byla odečtena proudová maxima z nichž byl sestrojen hydrodynamický voltampérogram, který vypovídá o elektrochemickém chování stanovované látky v průtokovém uspořádání (Obr. 5B). Pro měření jednotlivých vzorků se volí potenciál v místě největšího proudového rozdílu a nejmenšího potenciálového rozdílu hydrodynamického voltampérogramu. V našem případě bylo vybráno 780 mV jako nejvhodnější potenciál, který byl vložen na poslední elektrodu detektoru.
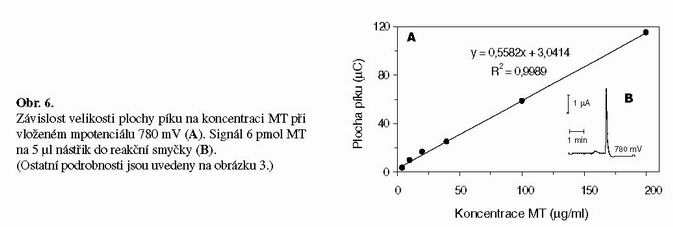
Stanovení koncentrace MT
Při nastavení všech optimálních parametrů metody jsme sestavili kalibrační křivku pro MT a určili limit detekce FIA-ED stanovení. Závislost plochy píku, osmé elektrody (780 mV) detektoru, na koncentraci MT byla lineární a relativní střední chyba
(R.S.D.) se pohybovala kolem 5% (n = 5). Rovnice kalibrační přímky a hodnota spolehlivosti závislosti elektrochemické odpovědi na koncentraci byla y = 0,55x + 3,04; R2 = 0,9989 (viz. Obr. 6A). Na obrázku 6B je ukázán signál, naměřený na elektrodě s pracovním potenciálem 780 mV, 6 pikomolů mMT v 5 µl nástřiku. Limit detekce metody FIA-ED byl určen jako 280 nM resp. 1,4 pmol/5 µl.
4. Závěr
V této práci byl studován metalothionein, jakožto potenciální možný marker pro celou skupinu nádorových onemocnění, metodou FIA-ED. Pro stanovení bylo využito multi-kanálového CoulArray elektrochemického detektoru. Analytický postup jsme optimalizovali pro dosažení co nejvyšší odezvy za použití mobilní fáze ACN/TFA. Závislost na koncentraci MT byla lineární ma stanovený limit detekce byl 1,4 pmol na 5 µl nástřik.
Literatura
- BŘEZINA, M., and P. ZUMAN, 1952 Polarografie v lékařství,
biochemii a farmacii. SZN, Praha.
- CARDOSO, S. V., H. M. BARBOSA, I. M. CANDELLORI, A. M. LOYOLA
and C. F. AGUIAR, 2002 Prognostic impact of metallothionein on oral
squamous cell carcinoma. Virchows Arch. 441: 174–178.
- COYLE, P., J. C. PHILCOX, L. C. CAREY and A. M. ROFE, 2002
Metallothionein: The multipurpose protein. Cell. Mol. Life Sci. 59:
627–647.
- DABRIO, M., A. R. RODRÍGUEZ, G. BORDIN, M. J. BEBIANNO, M. DE
LEY et al., 2002 Recent developments in quantification methods for
metallothionein. J. Inorg. Biochem. 88: 123–134.
- DOUGLAS-JONES, A. G., K. W. S. SCHMID, B. BIER and E. AL., 1995
Metallothionein expression in duct carcinoma in situ of the breast.
Hum. Pathol. 26: 217-222.
- JASANI, B., and M. E. ELMES, 1993 Immunohistochemical detection
of metallothionein. Metallobiochemistry Part B: Metallothionein and
relatd molecules. Methods Enzymol. 205: 95-107.
- JASANI, B., and K. W. S. SCHMID, 1997 Significance of
metallothionein overexpression in human tumors.
Histopathology
31: 211-214. - JOSEPH, M. G., D. BANERJEE, W. KOCHA, R. FELD, L. W. STITT et
al., 2001 Metallothionein expression in patients with small cell
carcinoma of the lung. Cancer 92: 836-842.
- KÄ GI, J. H. R., 1993 Overview of metallothionein.
Metallobiochemistry Part B: Metallothionein and related molecules.
Methods Enzymol. 205: 613-626.
- KÄ GI, J. H. R., and Y. KOJIMA, 1987 Biochemistry of
Metallothionein. Experientia. Suppl. 52: 25–61.
- KIZEK, R., L. TRNKOVÁ and E. PALEČEK, 2001 Determination of
metallothionein at the femtomole level by constant current
stripping chronopotentiomentry. Anal. Chem. 73:
4801–4807.
- KIZEK, R., J. VACEK, L. TRNKOVÁ, B. KLEJDUS and L. HAVEL, 2004
Využití katalytických reakci na rtuťové elektrodě pro
elektrochemické stanovení metalothioneinů. Chem. Listy 96:
100.
- KOJIMA, Y., 1991 Definitions and nomenclature of
metallothioneins. Methods Enzymol. 205: 8–10.
- KUO, T., and S. K. LO, 1997 Immunohistochemical metallothionein
expression in thymoma: correlation with histological types and
cellular origin. Histopathology 30: 243-248.
- MINAMI, T., S. ICHIDA and K. KUBO, 2002 Study of
metallothionein using capillary zone electrophoresis. J. Chrom. B
781: 303-311.
- STROUHAL, M., R. KIZEK, J. VACEK, L. TRNKOVÁ and M. NĚMEC, 2003
Electrochemical study of heavy metals and metallothionein in yeast
Yarrowia lipolytica. Bioelectrochem. 60: 29–36.
- TANG, W. F., T. KIDO, W. A. GROSS, K. NOGAWA, E. SABBIONI et
al., 1999 Measurement of cadmium-induced metallothionein in urine
by ELISA and prevention of overestimation due to polymerization. J
Anal Toxicol 23: 153-158.
- TRNKOVÁ, L., R. KIZEK and J. VACEK, 2002 Catalytic signal of
rabbit liver metallothionein on a mercury electrode: combination of
derivative chronopotentiometry with adsorptive transfer stripping.
Bioelectrochem. 56: 57–61.
- VAŠÁK, M., and D. W. HASLER, 2000 Metallothioneins: new
functional and structural insights. Current Optinion in Chem. Biol.
4: 177-183.
- WEINLICH, G., W. BITTERLICH, V. MAYR, P. O. FRITSCH and B.
ZELGER, 2003 Metallothionein-overexpression as a prognostic factor
for progression and survival in melanoma. A prospective study on
520 patients. Brith. J. of Dermatol. 149: 535-541.
Poděkování
Práce na této publikaci byla financována z dlouhodobého záměru Agronomické fakulty MZLU č. 4321 00001, Grantu 525/04/P132 od GA ČR a IGA MZLU 3/2004 a FRVŠ 164/2004.
Datum přednesení příspěvku: 26. 5. 2004
