Konference: 2005 XXIX. Brněnské onkologické dny a XIX. Konference pro sestry a laboranty
Kategorie: Nádorová biologie/imunologie/genetika a buněčná terapie
Téma: Vitamíny a nutraceutika
Číslo abstraktu: 241
Autoři: P. Hanuštiak; R. Mikelová; A. Kučerová; prof. RNDr. Petr Hodek, CSc.; prof. RNDr. Marie Stiborová, DrSc.; doc.Ing. René Kizek, Ph.D.
1. Úvod
Podle údajů WHO je nádorové onemocnění tkáně gastrointestinálního traktu, především střev a konečníku, v celosvětovém měřítku příčinou téměř 1/10 úmrtí na nádorová onemocnění a meziroční nárůst incidence se blíží k 10%. Česká republika spolu s Maďarskem a Polskem zaujímá přední místa ve světových statistikách výskytu tohoto zhoubného onemocnění. Rakovina tohoto typu postihuje až 2x více mužskou část populace, kde po 75 roku věku je nejčastější příčinou úmrtí. Z řady faktorů, které zvyšují pravděpodobnost výskytu, jmenujme alespoň tyto: genetická dispozice, některé zdravotní problémy (záněty střev, polypy, odstranění žaludku) a v neposlední řadě také stravovací návyky spojené se složením potravy. Konzumace velkého množství stravy bohaté na tuky s nedostatečným příjmem vlákniny, alkoholické nápoje (destiláty) a kouření, konzumace pyrolyzátů bílkovin, a naopak nízký příjem ovoce a zeleniny a dále i vápníku, to všechno patří mezi rizikové faktory (Janout et al., 2004; KarimianTeherani et al., 2001).
1.1 Nutraceutika
Naopak vhodným složením denní stravy lze výrazně pozitivně ovlivňovat metabolické procesy v trávícím traktu člověka. Kromě obecných potravních návyků, jako je zvýšená konzumace ovoce a zeleniny, luštěnin a obilovin, se také často mluví o potravinách, které se nazývají nutraceutika (Modrianský et al., 2003). Nutraceutika jsou potraviny, které mají pozitivní fyziologické účinky na lidský organismus. Bylo prokázáno, že mají vliv na celkový zdravotní stav člověka a mohou výrazně podporovat fyziologický výkon či snižovat riziko vzniku některých nemocí (Dixon, 2004). Mezi významné patří rozdílné skupiny metabolitů rostlin, jako fenolové kyseliny, lignany, fytosteroly, karotenoidy, glukosinoláty a mnoho dalších skupin, mezi které náleží i flavonoidy (Modrianský et al., 2003).
1.2 Flavonoidy
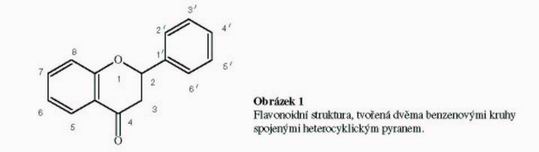
Flavonoidy jsou velice rozsáhlou skupinou rostlinných fenolů. V současné době je známo více než 4000 flavonoidních látek a stále se nacházejí další sloučeniny. Jsou odvozeny od kyslíkaté heterocyklické sloučeniny flavanu, tvořeného dvěma benzenovými kruhy spojenými heterocyklickým pyranem (Obr. 1). Běžně bývají všechny tři kruhy substituovány hydroxyskupinami nebo methoxyskupinami a jednotlivé deriváty se liší pouze stupněm substituce a oxidace. Rozeznáváme následující základní struktury flavonoidů: katechiny, leukoanthokyanidiny, flavanony, flavononoly, flavony, flavonoly a anthokyanidiny. Přírodní flavonoidy se nejčastěji vyskytují ve formě O-glykosidů, obsahují tedy ve své molekule necukernou součást (aglykon) a cukernou složku. Volné aglykony se vyskytují pouze zřídka. V některých případech (při technologickém zpracování při vyšších teplotách a v kyselém prostředí) může docházet k hydrolýze glykosidů a vzrůstu koncentrace aglykonů (Klejdus et al., 2003; Williams & Grayer, 2004).
1.3. Vztah flavonoidů k nádorovým onemocněním
Pokud jde o význam flavonoidů vzhledem k nádorovým onemocněním, názory vědců se výrazně odlišují. Někteří uvádějí, že v rámci studií na zvířecích modelech a v pokusech in vitro je zjišťován antikarcinogenní účinek, který však v epidemiologických studiích nebyl prokázán (Komprda, 2003; Modrianský et al., 2003; Scalbert & Williamson, 2000; Slanina & Táborská, 2004). Uvádějí, že antikarcinogenní působení flavonoidů lze odvodit z jejich chemické struktury a projevuje se jak v iniciační, tak v promoční fázi karcinogeneze. Diskutovány jsou v tomto kontextu následující mechanizmy: i) inhibice „prooxidačních“ enzymů fáze I (PIE), ii) indukce konjugačních, detoxifikačních enzymů fáze II, iii) přímá interakce s DNA, iv) indukce apoptózy (programovaná buněčná smrt), v) inhibice buněčné proliferace, vi) antioxidativní působení, vii) modulace imunitního systému.
Enzymy fáze I (PIE) jsou mikrozomální, především jaterní enzymy, jejichž funkcí je vnášet do (původně hydrofobní) molekuly hydrofilní funkční skupiny (např. hydroxyl) nebo vsunout kyslíkový atom mezi vazby uhlík-vodík nebo dusík-vodík. Typickým příkladem je enzym cytochrom-P-450-monooxygenáza. V tomto smyslu působí PIE pro-oxidačně a tedy pro-iniciačně. Iniciace je tak podporována metabolickou aktivací prokarcinogenů působením PIE. Naopak enzymy fáze II katalyzují konjugaci xenobiotik, předem upravených působením PIE s endogenními polárními ligandy (např. glutathion, glukuronát, sulfát). Touto konjugací vzniká metabolicky neaktivní produkt, který může být vyloučen z těla (Komprda, 2003).
Na druhou stranu však existují vědci, kteří jsou přesvědčeni o karcinogenním působení některých flavonoidů (Ferguson, 2001; Hodek et al., 2002). Tvrdí, že použití vysokých dávek flavonoidů, které sice účinně brání např. vzniku některých aduktů s DNA, má současně genotoxický účinek a navozují indukci cytochromů P450, např. cytochromu P450 1A2. Dalo by se namítnout, že vysoké koncentrace flavonoidů není možné bez konzumace potravních doplňků dosáhnout, ale faktem je, že vzhledem k omezené resorpci v tenkém střevě a resorpci vody v tlustém střevě může koncentrace dosáhnout vysokých hodnot řádově mmol.l–1 (Scalbert & Williamson, 2000; Slanina & Táborská, 2004).
Množství flavonoidů ve stravě je důležitým faktorem vzhledem k nádorovým onemocněním, ať už mají charakter ochranný či karcinogenní. V naší práci jsme se zaměřili na vypracování přesné elektroanalytické metody na stanovení některých flavonoidů, konkrétně quercetinu, quercitrinu, rutinu, diosminu a chrysinu.
Experimentální část
2. Materiál a metody
Chemikálie
NaH2PO4, Metanol, Diosmin, Chrysin, uhlíkový prášek a minerální olej byly dodány firmou Sigma Aldrich Corp. (USA). Rutin trihydrat a Quercitrin dihydrat byly dodány firmou Roth GmbH, Karlsruhe (Ger.). Na2HPO4 byla dodaná firmou Merck, Darmstadt (Ger.). Quercetin dihydrat byl dodán firmou Fluka chemie AG (USA). Všechny chemikálie byly ACS čistoty, stejně tak i voda (Sigma), ve které byly připraveny pracovní roztoky.
Elektrochemická analýza
Square-wave voltametrie byla prováděna pomocí elektrochemického analyzátoru AUTOLAB (EcoChemie, Netherlands) v zapojení s tříelektrodovou celou VA-Stand 663 (Metrohm, Switzerland). Byla použita pracovní uhlíková pastová elektroda, referenční (Ag/AgCl, 3 M KCl) elektroda, a jako pomocná elektroda byla použita uhlíková tyčka. Získaná data byla upravena matematickou korekcí podle algoritmů navržených Savitzkym a Golayem implementovaných do GPES softwaru (EcoChemie). Experimenty byly prováděny při laboratorní teplotě. Měření bylo prováděno v potenciálovém rozsahu od –0,1 V do 1,2 V s těmito parametry: potenciálový krok 1,95 mV, pulzní amplituda 49,85 mV. Jako základní elektrolyt jsme použ ili fosfátový pufr o pH = 7,0. Uhlíková pasta (asi 0,5 g) byla vyrobena z uhlíkového prášku a minerálního oleje (bez DNáz, RNáz, and proteáz). Poměr uhlíkového prášku a minerálního oleje byl 70/30 (w/w). Pasta byla vložena do teflonového těla elektrody s průměrem plochy elektrody 2,5 mm. Před každým měřením byla elektroda vždy obnovena, tedy očištěna od nečistot pomocí filtračního papíru.
3. Výsledky
Analytické stanovení flavonoidů se v současné době provádí především metodami chromatografickými (Franke et al., 2004; Robards, 2003; Smyth & Brooks, 2004) a kapilární elektroforézou s různými typy detekce. Pouze málo autorů se zabývá možností stanovení flavonoidů metodami elektrochemickými (Brett & Ghica, 2003; Zoulis & E., 1996). Ovšem elektrochemické metody mají velkou výhodu v miniaturizaci a následném použití v praxi. Umožňují například detekci látek in vivo bez usmrcení organismu. Naším cílem je tedy vyvinout spolehlivou elektrochemickou metodu stanovení quercetinu, rutinu, quercitrinu, chrysinu a diosminu v biologických vzorcích.
Nedávno byla v literatuře publikována metoda na elektrochemické stanovení quercetinu pomocí elektrody ze skelného uhlíku, kde je nevýhodou příprava pracovního povrchu (leštění aluminou, ultrazvuk) (Brett & Ghica, 2003). Proto jsme navrhli metodu využívající uhlíkovou pastovou elektrodu pro stanovení quercetinu, rutinu, quercitrinu, chrysinu a diosminu pomocí squarewave voltametrie v fosfátovém pufru. Velkou výhodou uhlíkové pastové elektrody je mnohem jednodušší příprava pracovního povrchu, kdy stačí pracovní plochu připravit vyleštěním na filtračním papíře.
Fenoly se obecně špatně rozpouštějí v polárních rozpouštědlech (voda), výrazně lepší rozpustnost je pozorována v nepolárních rozpouštědlech (metanol). Hledali jsme proto optimální rozpouštědlo, ve kterém by se všechny námi studované flavonoidy rozpustily. Jako vhodné rozpouštědlo byl nalezen metanol. Avšak vysoký podíl organické složky zhoršuje elektrochemickou analýzu. Při našich experimentech byl však podíl organické fáze v základním elektrolytu (2 ml) jen 0,1%.
Po přídavku flavonoidů do základního elektrolytu byly pozorovány na DPV voltamogramech oxidační signály. Brettová popisuje signály pík 1 a pík 2 jako oxidace hydroxylové skupiny v poloze 7 flavonoidního skeletu (Obr.1) (Brett & Ghica, 2003). Při našich experimetech byly pozorovány další dva signály píky 3 a 4, které budou pravděpodobně soviset s oxidací hydroxylové skupiny v poloze 5 flavonoidního skeletu.
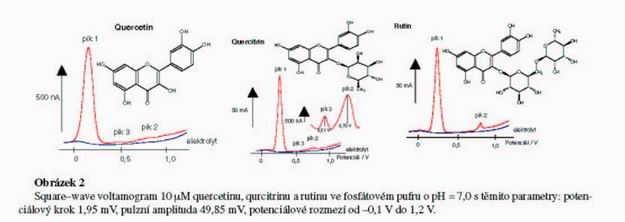
Jak je na obrázku 2 ukázáno, poskytují studované flavonoidy oxidační signály při potenciálech 0,25 V, 0,51 V a 0,78 V (Obr. 2). Z těchto našich výsledků je také patrný vliv sacharidu na elektrochemický signál. Elektrochemické signály u chrysinu a diosminu byly výrazně potlačeny. Menší elektrochemická odezva bude pravděpodobně souviset s rozdílnou chemickou strukturou. Nejvšší vliv navázaného sacharidu byl pozorován u diosminu (Obr. 3). Na základě těchto výsledků bylo možné určit limity detekce jednotlivých flavonoidů jako 3 S/N (signál/šum), viz. Tab.1.

4. Závěr
Flavonoidní látky mají pravděpodobně vztah k nádorovým onemocněním. Bez řádných klinických studií je zatím nemožné prohlásit, zda je tento účinek pozitivní či negativní, a je potřebné tyto látky běžně a rychle stanovit v biologickém vzorku. Pro tento účel se velmi dobře hodí použití elektrochemických metod. Vyvinutá metoda nám umožnila stanovit rutin, quercetin, quercitrin, chrysin a diosmin pomocí square-wave voltametrie na uhlíkové pastové elektrodě s limity mdetekce řádově desítek nmol/l, u diosminu jednotek mol/l.
Flavonoidní látky LOD(nM)
Quercetin 20
Quercitrin 35
Rutin 35
Chrysin 40
Diosmin 2700
Tabulka č. 1 Přehled limitů detekce (LOD, 3S/N) pro stanovované flavonoidy
Literatura
- Brett, A.M.O. & Ghica, M.E. (2003). Electroanalysis, 15,
1745-1750.
- Dixon, R.A. (2004). Ann. Rev. Plant. Biol., 55,
225-261.
- Escarpa, A. & Gonzales, M.C. (2001). Crit. Rev. Anal.
Chem., 2, 57-139.
- Ferguson, L.R. (2001). Mut. Res., 475, 89-111.5. Franke, A.A.,
Custer, L.J., Arakaki, C. & Murphy, S.P. (2004). J. Food
Compos. Anal., 1, 1-35.
- Hodek, P., Trefil, P. & Stiborová, M. (2002). Chem. Bio.
Int., 139, 1-21.
- Janeiro, P. & Brett, A.M.O. (2004). Anal. Chim. Acta, 518,
109-115.
- Janout, V., Siroky, P., Novak, J., Cizek, L., Koukalova, H.
& Beska, F. (2004). Onkologie, 27, 376-379.
- Karimian-Teherani, D., Vutuc, C. & Janout, V. (2001).
Neoplasma, 48, 257-261.
- Klejdus, B., Sterbova, D., Stratil, P. & Kuban, V. (2003).
Chem. Listy, 97, 530-539.
- Komprda, T. Základy výživy člověka. MZLU Brno.
- Modrianský, M., Valentová, K., Přikrylová, V. & Walterová,
D. (2003). Chem. Listy, x-y.
- Robards, K. (2003). J. Chrom. A, 1-2, 657-691.
- Scalbert, A. & Williamson, G. (2000). J. Nutr., 8,
2073S-2085S.
- Slanina, J. & Táborská, E. (2004). Chem. Listy,
239-245.
- Smyth, W.F. & Brooks, P. (2004). Electrophoresis, 10-11,
1413-1446.
- Suntornsuk, L. (2002). J. Pharmaceut. Biomed., 5,
679-698.
- Williams, C.A. & Grayer, R.J. (2004). Nat. Prod. Rep., 21,
539-573.
- Zoulis, N.E. & E., E.C. (1996). Anal. Chim. Acta, 255-261.
Poděkování
Příspěvek vznikl za podpory grantů RASO 2005, FRVŠ 2348/F4a a GAČR 525/04/P132
Datum přednesení příspěvku: 26. 5. 2005
