Konference: 2011 2. pražské mezioborové onkologické kolokvium
Kategorie: Maligní lymfomy a leukémie
Téma: Prezentace
Číslo abstraktu: 002
Autoři: MUDr. Hana Klamová, CSc.
Souhrn
Dasatinib, tyrozinkinázový inhibitor (TKI) druhé generace, je in
vitro zatím nejúčinnější blokátor tyrozinové kinázy Bcr-Abl, který
je 325krát účinnější než imatinib (IM) a 16krát než nilotinib.
Indikací k jeho podávání je u dospělých pacientů s Ph+ CML
rezistence (selhání) nebo netolerance léčby předchozí, včetně
terapie imatinibem.
Referujeme o prvních zkušenostech s léčbou dasatinibem u 71
nemocných s chronickou myeloidní leukémií (CML) v 6
hematoonkologických centrech v České republice, kterým byl
dasatinib podáván v chronické fázi (CP) a také v pokročilejším
stadiu nemoci (AP). U nemocných v CP, léčených dávkou 100 mg denně,
bylo dosaženo 97 % kompletních hematologických remisí (CHR), 77 %
velkých cytogenetických odpovědí (MCgR) a v 67 % kompletních
cytogenetických remisí (CCgR). Velké molekulární odpovědi (MMoR)
bylo dosaženo v mediánu 10 měsíců u 19/31 pacientů. U nemocných v
AP onemocnění byla míra CHR 77 %, MCgR 39 % a CCgR 33 %. U 15
pacientů byl vstupně zaznamenán výskyt mutací v kinázové doméně
BCR-ABL, u většiny z nich došlo v průběhu léčby k jejich vymizení.
Očekávané přežití bez progrese (PFS) po 12 měsících léčby u
pacientů v CP bylo 97 ± 3 %, u AP 62 ± 21 %, očekávané celkové
přežití pak u CP 97 ± 3 % a u AP 58 ± 23 %. Mediánu OS nebylo u CP
dosaženo, u AP byl medián OS 22,3 měsíce. Naše zkušenosti potvrdily
vysokou účinnost a dobrý bezpečnostní profil dasatinibu zvláště u
nemocných v CP CML rezistentních na léčbu předchozí, včetně
nemocných s mutacemi v kinázové doméně BCR-ABL.
Klíčová slova:
chronická myeloidní leukémie, dasatinib, cytogenetická odpověď,
mutace
Úvod
Nové poznatky v molekulární biologii a patofyziologii chronické
myeloidní leukémie (CML) výrazně změnily pohled na možnosti její
léčby. Do klinické praxe vstoupily tyrozinkinázové inhibitory
(TKI), látky, blokující funkci proteinu Bcr-Abl, který je pro
duktem fúzního genu BCR-ABL, a tedy i podstatou
CML.(1,2) První v klinické praxi používaný TKI imatinib
(IM) výrazně zvýšil pravděpodobnost dlouhodobého přežívání
nemocných. Nicméně i přes jeho vysokou účinnost, zvláště v první
linii, existuje skupina nemocných, kteří jsou vůči němu rezistentní
nebo jej netolerují. Mezi velmi časté důvody rezistence na IM patří
mutace v kinázové doméně BCR-ABL a také aktivace na BCR-ABL
nezávislých signálních drah, např. příslušníky rodiny Src kináz.
Intenzivní výzkum v této oblasti však brzy představil další
inhibitor tyrozinových kináz, TKI druhé generace dasatinib.
Dasatinib
(Sprycel®, původně označovaný BMS-354825) inhibuje aktivitu BCR-ABL
kinázy a kináz ze skupiny SRC a také řadu dalších onkogenních kináz
včetně c-KIT, kináz efrinového receptoru (EPH) a receptoru
PDGFbeta. Váže se jak na neaktivní, tak i aktivní konformaci enzymu
BCR-ABL a je silným subnanomolárním inhibitorem BCR-ABL kinázy s
účinností při koncentraci 0,6-0,8 nM. In vitro byla prokázána jeho
schopnost překonat rezistenci na IM vyplývající z BCR-ABL
overexprese, doménových mutací BCR-ABL kinázy, aktivace
alternativních signálních drah zahrnujících kinázy ze skupiny SRC
(Lyn, Hck) a overexprese genu multilékové rezistence.(3)
In vitro je zatím také nejúčinnějším blokátorem tyrozinové kinázy
Bcr-Abl, 325x účinnějším než IM a 16x účinnějším než nilotinib,
další tyrozinkinázový inhibitor druhé generace.
Prvnímu pacientovi byl dasatinib podán v roce 2003, první výsledky
klinických studií fáze I a II byly zveřejněny v roce 2004.
Zcela zásadními byly výsledky pěti klinických studií nazvaných
START (Src/ABL tyrosine kinase inhibitor activity: research trials
of dasatinib), do kterých byli zařazeni pacienti s akcelerovanou
nemocí (START-A), blastickou fází (START-B), Ph+ akutní
lymfoblastickou leukémií (START-L), chronickou fází (START-C) a
rezistentní chorobou (START-R), kdy byl porovnáván efekt léčby
dasatinibem s vysokou dávkou IM 800 mg denně. Studie velmi podrobně
hodnotily účinnost léčby ve všech stadiích CML a také Ph+
ALL.(4)
V ČR byly zkušenosti s léčbou dasatinibem získávány od prosince
2005, v souvislosti s účastí několika hematologických center v
klinických studiích CA180034 a CA180035, kdy byl dasatinib podáván
pacientům v chronické fázi (CP), akcelerované fázi (AP) a
blastickém zvratu (BZ), rezistentních na předchozí léčbu IM, nebo
jej netolerujících.(6)
Od listopadu 2006 je dasatinib registrován v Evropské unii a České
republice pod obchodním názvem Sprycel a je dostupný v potahovaných
tabletkách obsahujících 70, 50 a 20 mg dasatinibu. Optimálním
dávkováním léčby je 100 mg jednou denně pro CP a 140 mg jednou
denně pro AP a BZ.(5) U pacientů léčených v chronické
fázi je po 12 měsících dosahováno 91 % hematologických remisí a
více než 60 % velkých cytogenetických odpovědí. Kompletní
cytogenetické remise pozorovány u 40 % léčených. Bez progrese
onemocnění dlouhodobě přežívá více než 92 % pacientů. Projevy
nežádoucích účinků, většinou mírné až střední intenzity, jsou
častější u pokročilejších stadií nemoci, celkově však
tolerovatelné. Vysoká účinnost je patrná zvl. u nemocných s
přítomnými mutacemi v kinázové doméně BCR-ABL.(7)
Indikací k léčbě dasatinibem je v současné době CML ve všech fázích
nemoci při rezistenci nebo netoleranci léčby předchozí, včetně
léčby imatinibem a rezistence nebo netolerance předchozí terapie
Ph+ ALL.
Zde referujeme o našich prvních zkušenostech s léčbou dasatinibem u
nemocných s Ph+ CML v běžné klinické praxi, léčených v 6
hematoonkologických centrech v České republice. Data celkem 84
nemocných jsou registrována v databázích INFINITY (tyrosine kinase
Inhibitors iN FIrst aNd followIng CML Treatment) (n = 52) a CAMELIA
(Chronic MyEloid LeukemIA) (n = 19). Hodnoceno celkem 71 nemoc ných
(31 mužů a 40 žen ve věku 21 až 70 let, s mediánem věku při
stanovení diagnózy 58 let, 60 pacientů bylo v CP, 25 v AP nebo BZ).
Důvodem k zahájení léčby dasatinibem byla primární nebo sekundární
rezistence na IM, progrese nemoci, u 3 pacientů netolerance léčby
předchozí. Studie byla prováděna v souladu s Helsinskou deklarací.
Podle kritérií European LeukemiaNet (ELN)(8.9) jsme
hodnotili rychlost a kvalitu dosažení hematologické, cytogenetické
a molekulární odpovědi, nežádoucí účinky léčby (hodnoceno podle NCI
CTC Version 3.0) stupněm 1 až 4 a také celkové přežití (OS) a
přežití bez progrese (PFS). Naše výsledky jsme také porovnali s
výsledky studií START, pozornost jsme věnovali rovněž výskytu
mutací v kinázové doméně BCR-ABL.
Výsledky
Medián doby od stanovení diagnózy do zahájení léčby dasatinibem byl
39 měsíců (v rozmezí 3-276), předchozí léčbou u všech pacientů byl
IM (v mediánu 26 měsíců), u 54 % z nich také interferon alfa (INF).
Hodnoceno celkem 40 žen a 31 mužů s mediánem věku 58 let. (21-70).
45 nemocných bylo v CP a 25 v pokročilejších fázích onemocnění (AP
a BZ). Léčba dasatinibem trvala 4 týdny až 30 měsíců (medián 8
měsíců), jak ukazuje tabulka 1.
U pacientů, léčených v CP počáteční dávkou 100 mg dasatinibu denně,
bylo dosaženo 97 % kompletních hematologických remisí (CHR) s
mediánem dosažení 21 dní, 77 % velkých cytogenetických odpovědí
(MCgR) a 67 % kompletních cytogenetických remisí (KCgR). Velká
molekulární odpověď (MMoIR) byla patrná u 61 % léčených v mediánu
10 měsíců. U pokročilejších stadií nemoci (AP a BP) při
terapeutické dávce 140 mg dasatinibu denně bylo docíleno 77 % CHR,
39 % MCgR v mediánu 6 měsíců a 33 % CCgR, MMoIR u 11 % pacientů,
viz tabulku 2.
Mutační analýza provedena u 52 nemocných, mutace nalezeny u 25 %
(9/36) pacientů v CP a u 6/16 pacientů (37 %) v AP před zahájením
léčby dasatinibem. 11 různých typů mutací detekováno u 15 nemocných
před zahájením léčby s nejčastějším výskytem mutací Y253H, F311I,
H396R a F359V. U 7 pacientů došlo v průběhu léčby dasatinibem k
vymizení mutací (v mediánu 4 měsíců), u 3 pacientů nebyly
ovlivněny, u 3 nemocných došlo k vymizení původních, ale současně k
záchytu 3 jiných, nových mutací (T315A, F317L a K271R).
Nežádoucí účinky léčby: nehematologická toxicita jakéhokoliv stupně
u pacientů v CP pozorována u 42 %, nejčastější byl průjem a nauzea,
závažnější, tedy stupně 3 až 4 u 7 % léčených, z toho u 2 z nich
pleurální efúze. Cytopenie, hematologická toxicita přítomna u 66 %
nemocných, trombocytopenie 3.-4. stupně u 28 %. U pacientů v AP byl
zaznamenán větší počet cytopenií, stupně 3-4 u 62 %. Projevy
nehematologických nežádoucích účinků byly přítomny u 33 % léčených.
Přerušení léčby z důvodu její toxicity provedeno u 15 % pacientů v
CP a 26 % v pokročilejších fázích nemoci, jak znázorňuje tabulka
3.
Očekávané celkové přežití (OS) po 12 měsících léčby bylo 97 ± 3 % u
CP a 58 ± 23 % u AP a BP. Mediánu OS u pacientů v CP nebylo
dosaženo, u AP a BP byl medián OS 22,3 měsíce, viz graf 1.
Očekávané přežití bez progrese (PFS) ve 12 měsících bylo 97 ± 3 % u
CP a 62 ± 21 % u pokročilejších stadií nemoci. Medián doby do
progrese byl 20,1 měsíců u AP, u pacientů v CP mediánu dosaženo
nebylo.(10)
Závěr
Naše výsledky potvrdily vysokou účinnost dasatinibu v dosažených
počtech hematologických i cytogenetických odpovědí u pacientů v CP
CML rezistentních nebo netolerujících imatinib, a to jak u pacientů
s přítomnou mutací, tak bez mutace v kinázové doméně BCR-ABL.
Efektivním lékem byl také u pacientů v pokročilejších fázích
nemoci. Nežádoucí účinky léčby byly většinou zvládnuty
symptomatickou léčbou.
Dasatinib má tedy v současné době s ohledem na excelentní účinnost
a zvládnutelné nežádoucí účinky zcela jednoznačně své místo ve
všech obecně uznávaných doporučeních léčebných postupů CML, kterými
jsou ELN (European LeukemieNet), NCCN (National Comprehensive
Cancer Network Practice Guidelines on Oncology)
http://www.nccn.org, nebo ESMO Guidelines Working Group a také v
doporučení ČHS (České hematologické
společnost).(8,11)
Článek vznikl s podporou společnosti Bristol-Myers Squibb.
Literatura
- Goldman JM, Melo JV. Chronic myeloid leukemia - advances in biology and new approaches to treatment. N Engl J Med 2003; 349: 1451-1456.
- Hehlmann R, Hochhaus A, Baccarani M. Lancet 2007;370:342-350.
- Tokarski JS, Newitt JA, Chang CYJ, et al. The structure of dasatinib (BMS-354825) bound to activated ABL kinase domain elucidates its inhibitory activity against imatinib-resistant ABL mutants. Cancer Res 2006; 66: 5790-5795.
- Shah NP, Kim DW, Kantarjian HM, et al. Dasatinib 50 mg or 70 mg BID compared to 100 mg or 140 mg QD in patiens with CML in chronic phase who are resistant or intolerant to imatinib: results of CA180034. J Clin Oncol 2007; 25 (Suppl 18): Abstr 7004.
- Shah NP, Kantarjian HM, Kim DW, et al. Intermitent targe inhibition with dasatinib 100 mgpnce daily preserves efficacy and improves tolerability in imatinib-resistant and intolerant CP-CML. J Clin Oncol 2008;26:3204-3212 Abstr 7004.
- Apperley JF, Cortes JE, Kim DW, et al. Dasatinib in the treatment of chronic myeloid leukemia in accelerated phase After umatinib failure. The START A trial. J Clin Oncol 009;27:3472-3479.
- Hochhaus A, Kantarjian HM, Baccarani M, et al. Dasatinib induces notable hematologic and cystogenetic response in chronic-phase chronic myeloid leukemia after failure of imatinib therapy. Blood 2007; 109: 2303-2309.
- Baccarani M, Saglio G, Goldman J, et al. Evolving concepts in the management of chronic myeloid leukemia: recommendations from an expert panel on be half of the European LeukemiaNet. Blood 2006;108: 1809-1820.
- Muller MC, Cross NC, Erben P, et al. Harmonization of molecular monitoring of CML therapy in Europe. Leukemia 2009;23:1957-1963.
- Klamova H, Faber E, Zackova D, et al. Dasatinib in imatinib-resistant or -intolerant CML patients: data from the clinical practice of 6 hematological centers in the Czech Republic. Neoplasma 2010;57:355-359.
- Klamova H, Voglova J. Chronická myeloidní leukemie. Transfuze Hematol.dnes 2010;16:17-20.
MUDr. Hana Klamová, CSc. a spoluautoři Ústav hematologie a krevní transfúze, Praha
e-mail: Hana.klamova@uhkt.cz
Tabulka 1 Charakteristika pacientů před zahájením léčby dasatinibem
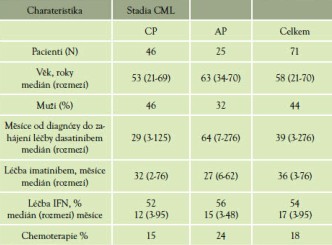
Vysvětlivky: IFN - interferon, CP - chronická fáze,AP - akcelerovaná fáze a blastický zvrat, N - počet pacientů
Tabulka 2 Odpověď na léčbu dasatinibem
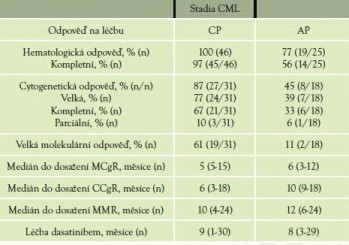
Vyvětlivky:
CCgR - kompletní cytogenetická remise,MCgR - velká cytogenetická odpověď,MMR - velká molekulární odpověď, AP - pokročilé stadium nemoci - akcelerovaná fáze a blastický zvrat CML
Tabulka 3 Vedlejší účinky léčby dasatinibem (toxicita)
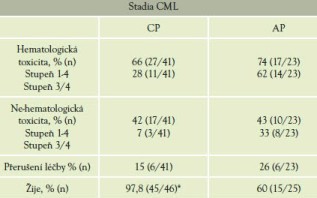
*1x smrt ne z důvodu progrese CML
Graf 1 Celkové přežití (OS) a přežití bez progrese (PFS) - analýza podle Kaplan-Meiera

Datum přednesení příspěvku: 28. 1. 2011
