Konference: 2011 XXXV. Brněnské onkologické dny a XXV. Konference pro sestry a laboranty
Kategorie: Kolorektální karcinom
Téma: Chemoterapie, biologická a hormonální terapie
Číslo abstraktu: 014
Autoři: doc. MUDr. Ilona Kocáková, Ph.D.
Karcinom tlustého střeva a konečníku je v České republice jedním z nejčastějších nádorových onemocnění, v celoevropském měřítku jsme ve výskytu této diagnózy u mužů na prvním a u žen na druhém místě. Kolorektální karcinom zároveň patří i k nejčastějším příčinám úmrtí na maligní onemocnění u nás. Incidence nádorů kolorekta stoupla za posledních 20 let o 190 %. Ročně je v naší republice zachyceno zhruba 7 450 nových případů kolorektálního karcinomu, na tuto diagnózu ročně umírá 4 400 pacientů. Kolorektální karcinom tak znamená závažný medicínský a ekonomický problém, který znepokojuje jak pacienty, tak poskytovatele léčebné péče a společnost jako celek.
Účinnou zbraň v boji s metastatickým karcinomem tlustého střeva a konečníku představuje monoklonální protilátka cetuximab, která je cíleně namířená proti receptoru pro epidermální růstový faktor (EGF nebo transformační růstový faktor-a, TGF a).
Na základě pozitivních výsledků studií, především studie BOND (BOND: Bowel Oncology with erbitux antibody), byl cetuximab schválen EMEA (Evropské komise pro hodnocení léčivých přípravků, European Agency for the Evaluation of Medicinal Products) a doporučen v kombinaci s irinotecanem pro léčbu pacientů s metastazujícím kolorektálním karcinomem exprimujícím receptor EGF po selhání cytotoxické léčby zahrnující irinotecan. Cetuximab v kombinaci s irinotecanem byl poprvé uveden na trh ve Švýcarsku v prosinci 2003, pro léčbu pacientů s metastatickým onemocněním byl zaregistrován od února 2004 také ve Spojených státech a od 1. července 2005 i v České republice, kde je k dispozici pod obchodním označením Erbitux®.
REGISTR ERBITUX
Tento projekt se řadí do kategorie lékových registrů, podporovaných výborem České onkologické společnosti. Je zaměřen na sledování účinnosti léčby cetuximabu v současné době používaného pro indikace metastazujícího kolorektálního karcinomu a lokálně pokročilého spinocelulárního karcinomu hlavy a krku. On-line systém registru je uzpůsoben pro sběr specifických klinických dat projektu ERBITUX a je přístupný uživatelům pomocí internetového prohlížeče. Získané informace mohou být využity lékařskými institucemi a specialisty podílejícími se na registru výhradně pro vědecké a profesionální lékařské účely v odborných listech a na konferencích.
Primární cíle:
- Sledování celkového počtu pacientů s metastatickým kolorektální karcinomem léčených Erbituxem v České republice
- Hodnocení bezpečnosti léčby
- Hodnocení efektivity léčby
- Analýza přežívání pacientů ve vztahu k sledovaným klinickým faktorům
- Analýza souboru pacientů léčených Erbituxem ve vztahu k referenčním populačním datům ČR
Časový plán sledování
Sledování zahrnuje jak retrospektivní, tak prospektivní pacienty. Retrospektivní pacienti byli zadáváni v první fázi projektu od zaregistrování přípravku pro léčbu metastatického onemocnění, prospektivně jsou pacienti zadáváni od 1. 10. 2008, a to po prozatím nedefinovanou dobu.
Validace dat
Všichni pacienti registru ERBITUX s kolorektálním karcinomem musí mít dostatečně založený záznam, tedy záznam musí obsahovat tyto údaje:
- Datum stanovení histologie
- Lokalizace primárního nádoru
- Histologický typ
- Linie léčby pokročilého onemocnění, ve které je poprvé podáván Erbitux
- Datum aktualizace + současný stav
- Datum zahájení léčby Erbituxem
Spolupracující centra – nemocnice a kliniky
Všeobecná FN Praha, FN Motol, Praha, Nemocnice České Budějovice, FN Hradec Králové, NSPCV Chomutov, FN Nemocnice Jihlava, Nemocnice s poliklinikou v Novém Jičíně, FN Olomouc, Baťova nemocnice, Zlín, MOÚ Brno, FN Plzeň, Krajská nemocnice Liberec, FN Ostrava, FN u sv. Anny v Brně, Fakultní Thomayerova nemocnice, Praha, FN Brno, FN Na Bulovce, Praha, Nemocnice Pardubice, Masarykova nemocnice Ústí nad Labem
Stav registru k datu 17. 1. 2011
K tomuto datu je v registru Erbitux 657 pacientů, z toho u 618 pacientů je dostatečně vyplněný záznam.
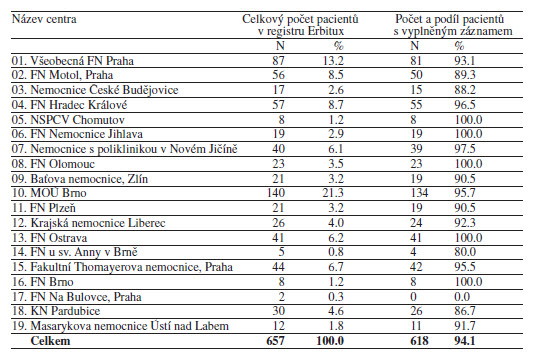
Charakteristika 618 pacientů léčených cetuximabem
- V souboru převažují muži: 64,2 % (N=397), ženy: 35,8 % (N=221), medián věku sledovaného souboru je 61 roků (rozmezí 20-84 roků).
- Cetuximab byl nejčastějí podáván jako 3. a další linie léčby pro metastatický kolorektální karcinomu.
- Stav K-ras: divoký typ K-ras nalezen u 345 pacientů, u 21 nemocných průkaz mt K-ras, u 252 pacientů nestanoven.
- K datu 17. 1. 2011 494 pacientů (79,9 %) ukončilo léčbu cetuximabem, přičemž nejčastějším důvodem ukončení byla progrese onemocnění.
- Medián doby podávání cetuximabu u pacientů s ukončenou léčbou byl 4,4 měsíce (min. 0,2-34,3 měsíců).
- Nejlepší dosažená léčebná odpověď na léčbu cetuximabem byla:
kompletní remise: 5,8 %, parciální remise: 19,6 %, stabilizace
onemocnění: 31,4 %, progrese nemoci: 18,8 %. Léčebnou odpověď nelze
hodnotit nebo není uvedena u 24,4 % léčených pacientů.
- Přežití pacientů bylo hodnoceno metodikou podle Kaplana-Meiera. Celkové přežití od data zahájení léčby je 16,4 měsíců. Jednoleté přežití 66,3 %, dvouleté přežití 30,4 %.
- Medián přežití bez známek progrese od data zahájení léčby cetuximabem byl 6,7 měsíců, jednoletý PFS 27,5 %, dvouletý PFS: 10,7 měsíců.
- Nežádoucí účinky (nejčastěji kožní toxicita)stupně 3 a 4 se vyskytla u 19,6 % léčených pacientů
Závěr
Data z našeho registru prokazují významnou protinádorovou účinnost cetuximabu u pacientů s chemorezistentním kolorektálním karcinomem, bylo dosaženo 25,4 % léčebných odpovědí, klinický benefit (CR+PR+SD) byl dokumentován u 56,8 % pacientů a přežití bez známek progrese 6,7 měsíců. Tato data jsou plně konsistentní s daty studie BOND (RR: 22,9 %, linický benefit: 55,5 % léčených, PFS: 4,1 měsíců.
Podrobná analýza 140 pacientů léčených cetuximabem v Masarykově onkologickém ústavu od roku 2005 bude sdělena ústně.
Klinická studie CRYSTAL (CRYSTAL: Cetuximab combined with iRinotecan in first line therapY for metaSTatic colorectAL cancer) je klinická studie fáze III, které se zúčastnilo přes tisíc pacientů s metastatickým kolorektálním karcinomem. Přinesla nezvratné důkazy o bezpečnosti a účinnosti použití cetuximabu v kombinované protinádorové léčbě pacientů s nepředléčeným onemocněním. Přidání anti-EGFR cílené léčby k chemoterapii prokázalo statisticky významné prodloužení času do nádorové progrese, bylo dosaženo vyššího počtu celkových léčebných odpovědí a bylo rovněž zaznamenáno vyšší procento kompletních remisí. Studie prokázala jednoznačnou superioritu kombinace cetuximab a FOLFIRI oproti kombinaci FOLFIRI, která tvořila do té doby zlatý standard protinádorové léčby 1. linie. Tyto výsledky tak daly reálný předpoklad pro další rozšíření indikace tohoto přípravku.
Cetuximab je v České republice registrován pro léčbu pacientů s metastazujícím kolorektálním karcinomem exprimujícím receptor epidermálního růstového faktoru a vykazujícím gen KRAS divokého typu a to:
- v kombinaci s chemoterapií
- v monoterapii u pacientů, u kterých selhala léčba na bázi oxaliplatiny a irinotecanu a kteří irinotecan nesnáší.
Poděkování za analýzu dat všem zaměstnancům IBA a všem lékařům podílejícím se na diagnostice a léčbě pacientů s kolorektálním karcinomem
Datum přednesení příspěvku: 21. 4. 2011
