Konference: 2005 10. ročník odborného sympózia na téma Onkologie v gynekologii a mammologii
Kategorie: Zhoubné nádory prsu
Téma: Terapie pokročilého karcinomu prsu. II. Blok: Systémová terapie pokročilého karcinomu prsu
Číslo abstraktu: 032
Autoři: MUDr. Zdeněk Mechl, CSc.; MUDr. Renata Neumanová, Ph.D., MBA; MUDr. Vladimír Spurný, CSc.
Panel soudí, že optimální adjuvantní hormonální terapie pro postmenopauzální ženy s karcinomem prsu a positivními receptory představují inhibitory aromatáz, a to v úvodní terapii, nebo po léčbě tamoxifenem. ASCO Panel tak souhlasí, že 5leté podání tamoxifenu již
není optimální léčbou pro postmenopauzální ženy HR +.
Tamoxifen je stále nejčastěji používaným lékem v hormonální terapii karcinomu prsu a oznamně se podílí na na poklesu mortality karcinomu prsu. Byla provedena celá řada studií a meta-analýz, která prokázala, že tamoxifen podávaný po dva roky po mastektomii výrazně redukuje riziko recidivy a úmrtí.
Ve zprávě Early Breast Cancer Trialistś Collaborative Group z roku 1998 byly hodnoceny údaje 37.000 žen, které dostaly tamoxifen v léčbě časného karcinomu prsu. V této analýze se uvádí pro ženy s ER+:

Autoři upozorňují, že tyto výsledky není možno předpokládat ve skupině žen s negativními estrogenovými receptory.
Potenciální přínos tamoxifenu musí být dán do souvislosti s možnými vedlejšími účinky:
Benefit: prokázaná účinnost, ochranný účinek na kosti a lipidy, pokles rizika kardiovaskulárního postižení, redukce rizika kontralaterálního postižení.
Rizika: omezená účinnost pro pacienty s negativními ER, možný vývoj resistence, řada vedlejších účinků jako vaginální poruchy, nepravidelné menses, návaly, oční toxicita, leukopenie, poruchy jaterních enzymů. Nejzávažnější jsou venosní tromboembolie, cerebrální vaskulární postižení a riziko endometriálního karcinomu. Interakce s radioterapií může mít za následek potenciaci radiačně indukované plicní fibrosy.
I když tamoxifen zůstává stále v doporučení NCCN (National Comprehensive Cancer Network): T3,N1,M0 HR+ = tamoxifen 5 let ( + adjuvantní chemoterapie), ale v dovětku se uvádí:
První informace ze studie ATAC demonstrují vyšší DFS (disease free survival) a příznivější profil toxicity ve srovnání s tamoxifenem v adjuvantní terapii ER + postmenopauzálních žen. Proto v současné době lze zvažovat anastrozol jako možnou volbu proti tamoxifenu.
Nelze se tedy divit ze na ESMO 2004 uvádí Thuerliman ve výčtu nejvýznamnějších událostí v léčbě karcinomu prsu nové možnosti hormonální terapie = uvedení inhibitorů aromatas.
Inhibitory aromatas.
AIs způsobují selektivní a účinnou inhibici aromatásy s následnou supresí estrogenů u žen, které již nemají aktivní funkcí ovarií. U postmenopauzálních žen redukují hladinu cirkulujících estrogenů. Jsou indikovány pro léčbu BC postmenopauzálních žen. Jejich použití je kontraindikováno u žen s fungujícími vaječníky a nedoporučuje se u žen ER negativnich.
Třetí generace AIs představuje nový přístup k endokrinní léčbě BC: anastrozol, letrozol, vorozol (nesteroidní inhibitory) a exemestan (steroidní inhibitor). Jejich předností je příznivý profil toxicity ve srovnání s tamoxifenem. Prakticky žádné riziko venosního tromboembolismu a endometriálního karcinomu je negativně kompenzováno vlivem na kostní
densitu a menší měrou na hladinu sérových lipidů, což je důsledkem potlačené hladiny estrogenů.
Rozdíly mezi jednotlivými přípravky AIs třetí generace jsou minimální a neovlivňují klinickou účinnost. Pravděpodobně nejselektivnějším přípravkem je anastrozol, nemá androgenní vlastnosti nebo významnější vliv na profil lipidů a na hladinu nadledvinkových steroidů.
Otázka zní: nahradí AIs tamoxifen ?
První studie prokázaly stejný nebo lepší účinek AIs třetí generace vs. tamoxifen v první linii léčby pokročilého karcinomu prsu.
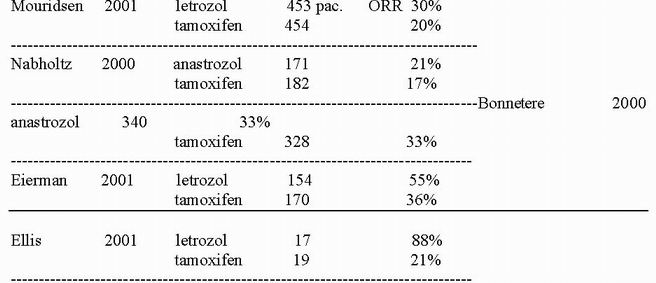
Zásadní náhled na účinnost a zařazení AIs do léčby postmenopauzálních ER+ žen přináší
výsledky 4 studií: ATAC, NCIC MA-17, INTERG EXEMESTAN a ITA.
Studie ATAC.
Od r. 2002 jsou průběžné výsledky této studie opakovaně prezentovány na všech předních jednáních o protinádorové terapii. Do studie bylo zařazeno v průběhu let 1996 – 2000 9.366 žen z 21 zemí a 380 center.
Indikací vstupu: postmenopauzální stav, HR +, po primární terapii operabilního invazivního BC. Pacienti byli zařazeni do 3 ramen: anastrozol 1 mg denně, tamoxifen 20 mg denně a v třetím ramenní kombinace obou přípravků, ve všech ramenech podání 5 let.
Ježto výsledky byly opakovaně prezentovány a komentovány, proto jen současné výsledky:
Nežádoucí události : sledování za 47 měsíců.
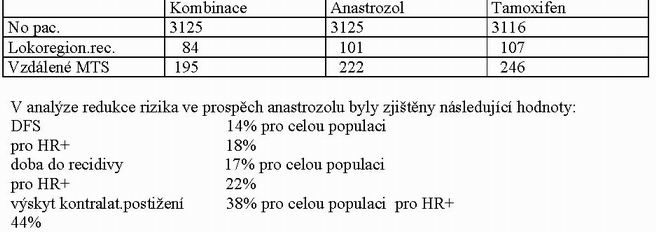
Významným bylo zjištění O´Reganové, že nejvyšších pozitivních výsledků bylo dosaženo u pacientek ER+ a PR-
(p = <.001). Překvapivé bylo zjištění selhání třetího ramena kombinační léčby, které nepřineslo lepší výsledky než samotný tamoxifen a jen lehce lepší než samotný anastrozol.
Vysvětlení spočívá zřejmě ve skutečnosti, že v estrogen deprimovaném prostředí je tamoxifen agonista, zatím co v prostředí bohatém na estrogen může tamoxifen rozvinout klasický antiestrogenní účinek.
Výsledky dle analýzy podskupin hormonálních receptorů: pro ER negativní je tamoxifen i anastrozol bez účinku, pro ER+PR- byl zaznamenán největší účinek, pro pacienty s N+ je účinek tamoxifenu a anastrozolu stejný.
Závěry: u postmenopauzálních žen s časným BC, s positivními hormonálními receptory vykazuje anastrozol ve srovnání s tamoxifenem lepší výsledky, měřeno hodnotami DFS a TTR. Anastrozol má výrazně lepší tolerabilitu než tamoxifen. Vztah benefit/riziko je jednoznačně ve prospěch anastrozolu.
Zajímavá diskuze vznikla ohledně kritiky zvýšeného počtu fraktur u žen léčených anastrozolem. EPOS (European Prospective Osteoporosis Study) uveřejnila v roce 2002 údaje o počtu končetinových fraktur u žen z 31 zemí. Uvádí u mužů 7,3/1000 osob/rok, u žen 19/1000 osob/rok. Tvrdí že i v normálních podmínkách dochází u 1 z 50 starších žen
k frakturám končetin. Čísla uváděna pro fraktury při podání anastrozolu tyto hodnoty nepřevyšují. Baum doporučuje u žen léčených anastrozolem pečlivě sledovat kostní denzitu a při podezření na demineralizaci použít bisfosfonáty.
Studie NCIC MA – 17.
Ve studii byla řešena otázka optimálního trvání endokrinní léčby a zda má smysl po 5 letech podávání tamoxifenu pokračovat v podání AIs. Do studie bylo zařazeno 5.187 postmenopauzálních žen.
Do studie MA-17 byly zařazeny ženy, které byly po 5letém podání tamoxifenu bez známek recidivy. Byla provedena randomizace: buď dostali placebo nebo dalších 5 let letrozolu. Studie byla předčasně ukončena pro výrazné zlepšení v DFS ve skupině léčené letrozolem. Autoři hovoří o vysokém morálním pozadí pro ukončení trialu. Ovšem objevila se kritika, konstatující, že tato studie nebude moci nikdy vyjádřit klinickou užitečnost v termínech přežití, nebo dát informace v analýze benefitu vs poškození. Příčina kritiky spočívala v tom, že v okamžiku ukončení studie pacientky, které dostávali placebo byly převedeny na letrozol. Další závažnou kritikou bylo, že výsledky byly nejprve publikovány v CNN a Washington Post, což se nepovažuje za vhodný kanál oznámení význačného pokroku. Ovšem řada autorů považuje ukončení studie za oprávněné, což dokládají výsledky za 36 měsíců:

ITA (Italian Tamoxifen Anastrozol Trial)
Otázka, kterou si italští autoři položili: je nutné podávat tamoxifen po dobu 5 let, nelze provést změnu na AI dříve? Studie byla založena na výsledcích dřívější studie Boccarda, který srovnával 5leté podání tamoxifenu vs. 2 – 3 podání tamoxifenu následované aminoglutetimidem. Ve studii bylo 426 pacientů a výskyt selhání byl 10 vs 26 ve prospěch kombinačního postupu.
Ve vlastní studii byli pacienti, kteří dostali 2 – 3 roky tamoxifen a byli randomizování pro další 2 – 3 roky podávání tamoxifenu nebo stejnou dobu podávání anastrozolu. Za poměrně krátkou dobu sledování – 36 měsíců - bylo zjištěno výrazné zlepšení ve skupině tamoxifen/anastrozol. Počet progredujících byl: tamoxifen vs tamoxifen/anastrozol 32 vs 12,
úmrtí 10 vs 4, nežádoucích účinků 45 vs 17.
Integroup Exemestan Study.
Studie koordinovaná Breast Internat. Group randomizovala pacientky buď pro 5 leté podávání tamoxifenu, nebo 2 roky podávala tamoxifenu následovaný 3 roky exemestanu. Po sledování za 3 roky ve studii s 5.000 sledovanými pacienty bylo dosaženo prokazatelně lepších výsledků ve skupině pacientů léčených kombinací tamoxifen + exemestan.
V současné době je aktivních více studií adjuvantního podání s AIs, které by mohly přinést definitivní odpověď na otázku účinnosti AIs:

Již v r 1992 bylo zjištěno, že přítomnost HER2 může mít vliv na resistenci na tamoxifen. Výsledky několika studií v této problematice přinesly konfliktní výsledky, což může být částečně vysvětleno rozdílnými metodami stanovení HER2. Ovšem v neoadjuvantním podání je několik prací, které ukazují, že BC HER2 + mohou být účinněji léčeny spíše AIs než tamoxifenem. Studie Ellise z roku 2001 prokazuje vyšší % remisí u
pacientů HER+ léčených letrozolem než tamoxifenem v neoadjuvanci. Studie IMPACT uvádí pro pacienty HER2+ 58% remisí léčených anastrozolem a 2% tamoxifenem.
Závěry:
Tamoxifen je stále standardem, ale již ne zlatým. Na základě současných výsledků lze extrapolovat následující indikace pro AIs:
• postmenopauzální ženy, ER+ PR –
• ženy s kontraindikací na tamoxifen
• HER2/neu +
Kdy :
- v první linii ( zatím není standard),
- po 2 – 3 letech podání tamoxifenu
Proč:- nižší riziko recidivy,
- vyšší účinnost,
- nižší výskyt vedlejších projevů.
Adjuvantní hormonální léčba časných stadií karcinomu prsu u postmenopauzálních žen se mění. Z terapie nespecifické, neselektivní, spojené s určitým rizikem se mění na terapii více přizpůsobenou biologickému charakteru nádorového onemocnění.
Datum přednesení příspěvku: 7. 1. 2005
