Konference: 2004 XXVIII. Brněnské onkologické dny a XVIII. Konference pro sestry a laboranty
Kategorie: Genitourinární nádory
Téma: Urologické nádory
Číslo abstraktu: 109
Autoři: MUDr. Petr Čoupek; MUDr. Ludmila Hynková, Ph.D.; Š. Košťáková
V léčbě lokalizovaného karcinomu prostaty se v současné době využívají 3 standardní metody – radikální prostatektomie (RAPE), zevní radioterapie a intersticiální brachyradioterapie. U časného karcinomu prostaty (T1, T2) jsou léčebné výsledky RAPE a zevní radioterapie srovnatelné (D’Amico A.V., Kupelian, P. Zelefsky). Pětileté přežití bez biochemického relapsu (PSA) bylo v obou skupinách obdobné (76% u nemocných léčených radioterapií, 75% u nemocných léčených RAPE). Oba léčebné přístupy se liší v počtu a závažnosti komplikací. U lokálně pokročilého nádoru (T3) je metodou volby zevní radioterapie. Zevní radioterapie u lokálně pokročilého nádoru nebo u karcinomu s vyšším rizikem (T2c, Gleason skore ≥8, vysoké PSA)se doporučuje aplikovat vždy současně v kombinaci s hormonální léčbou.
Adjuvantní radioterapie po provedené radikální prostatektomii je indikována při pozitivním okraji resekátu, při penetraci nádoru přes pouzdro prostaty, při infiltraci semenných váčků, při přetrvávající zvýšené hodnotě PSA i po RAPE. (Valicenti R. K., 1998)
Profylaktické ozáření pánevních uzlin do dávky 46 Gy má význam především u pacientů s vysokým rizikem – vyššípředléčebné PSA, vyšší Gleason skóre ≥6 a u větších nádorů (T2 b,c T3) (University of California San Francisko).
Na výsledky léčby – celkové přežití bez známek choroby, bez lokální i biochemické recidivy – má nejvyšší vliv výška celkové dávky aplikovaná do plánovaného cílového objemu.
Zelefsky M. J. prokázal v randomizované studii vliv dávky na lokální kontrolu choroby. Soubor 1100 pacientů byl rozdělen do několika ramen, ve kterých byla postupně zvyšována dávka záření po 5,4 Gy. Pětiletá lokální kontrola ověřená biopticky byla nejlepší u dávky 81 Gy (91%), dále ve srovnání 75,6 Gy (76%), 70,2 Gy (66%) a 64,8 Gy (48%). Vysoká dávka záření (vyšší než 75,6 Gy) měla nejlepší výsledky i při sledování biochemického relapsu (PSA). Význam vysoké dávky záření na lokální kontrolu choroby potvrzují i další autoři (Pollack A., Hanks G. E.) Ve studiích byly vytipovány 3 skupiny pacientů:
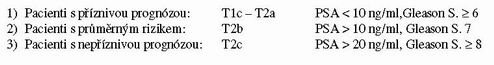
Konvenční dávky (65 – 70 Gy) nejsou pro většinu pacientů dostatečné. Vysokodávkovaná konformní radioterapie má největší přínos u pacientů s intermediární prognózou (PSA vyšší než 10 ng/ml). Dávky 75 – 80 Gy jsou nutné i u pacientů s nepříznivou prognózou. Tyto vysoké dávky záření mohou být aplikovány 3D konformní radioterapií (3D – CRT), případně nově zaváděnou radioterapií s modulovanou intenzitou svazku záření (IMRT). Úspěšná lokální terapie redukuje výskyt vzdálených metastáz (Kuks, Zagars).
Pro stanovení cílového objemu se běžně používá CT řezů, v budoucnu přichází v úvahu praktické využití magnetické rezonance (MR) a pozitronové emisní tomografie (PET). Objem prostaty definovaný pomocí magnetické rezonance bývá asi o 30% menší než objem definovaný pomocí CT řezů. MR je přesnější při stanovení lokalizace apexu prostaty, semenných váčků a dorsální části prostaty navazující na stěnu rekta. (Roach M., White S., Wefer A. E.)
Nověji se v procesu plánování radioterapie využívá i pozitronová emisní tomografie (PET), zejména spojení obrazu PET/CT. To jistě umožní zvýšit dávku v nádorové části prostaty zobrazené pomocí PET.
Konformní radioterapie je ozařovací technika, při které je přizpůsoben (tvarován) svazek záření trojrozměrnému objemu nádoru. V bezprostředním okolí plánovacího cílového objemu (PTV) dochází k prudkému poklesu dávky záření. To umožňuje aplikovat vysoké dávky záření v nádoru s maximálním šetřením okolních zdravých tkání.
Na simulátoru je pacient uložen do stabilní reprodukovatelné polohy (nejlépe s fixací dolních končetin), je lokalizován objem, který je následně podrobně vyšetřen pomocí CT řezů. V jednotlivých CT řezech jsou na plánovací konzole určeny plánovací objemy:
CTV – klinický cílový objem, který zaujímá prostatu a semenné váčky
PTV – plánovaný cílový objem je definován jako CTV + bezpečnostní lem (internal margin IM a set-up margin SM,lem pro nastavení polí)Většina autorů používá bezpečnostní lem 10 mm, někteří redukují dorsální lem vůči rektu na 6 mm. Kraniokaudálně bývá lem stanoven až 15 mm. Dále jsou stanoveny kontury kritických orgánů OAR (rektum, močový měchýř). Ozařovací předpis obsahuje požadavky na dávku a její homogenitu pro PTV. Celý PTV je pokryt 95% izodózou, doporučené kolísání dávky je v rozmezí 95 % – 107%.
Jednotlivá vstupní pole jsou simulována na simulátoru, provádí se verifikační snímky jednotlivých polí a přesnost nastavení je kontrolována i přímo pod ozařovacím přístrojem pomocí elektronického zobrazení polí (elektronic portal imaging). Při radioterapii prostaty používáme nejčastěji techniku 4 konvergentních polí s klíny (2 boční pole a 2 přední šikmá pole).
S vysokou dávkou záření je spojena i toxicita na zdravých tkáních. Trojrozměrná konformní radioterapie přináší výhodu lepší distribuce dávky a nižší expozici rekta a močového měchýře.
Akutní gastrointersticiální toxicita 2. stupně se pohybuje v rozmezí 15 – 60%, výskyt toxicity 3. a 4. stupně bývá nižší než 4%.
Akutní cystitida vyžadující medikaci (2. stupeň ) se vyskytuje u 13 – 40% pacientů, výskyt závažné urinární toxicity (stupeň 3 a 4) se pohybuje v rozmezí 0 – 7%. Zelefsky uvádí akutní urinární toxicitu 2. stupně u 37% nemocných, obtíže 3. a 4. stupně popisuje u 0,7% nemocných.
Chronická proktitida 2.stupně v průběhu 5 let sledování byla popsána v 11% a proktitida 3.stupně pouze v 0,75%.(Zelefsky). Podobně chronickou urinární toxicitu 2. stupně popisují jiní autoři v 7 – 10%, u 3. stupně ve 3%. Zvyšováním dávky nad 75 Gy míra chronických postradiačních změn stoupá (15 – 16%).
Toxicitu lze snížit:
- polohou pacienta na břiše, kdy stěna rekta obdrží nižší dávku záření. Rozdíl je markantní při ozařování v oblasti semenných váčků, které se v poloze na břiše oddálí od přední stěny rekta (Zelefsky).
- ozařováním při plném močovém měchýři; spoluozářený objem močového měchýře se zmenší a plný močový měchýř současně navíc oddálí kličky tenkého střeva
- technikou, která umožňuje dosáhnout lepší prostorovou distribuci dávky zejména u cílových orgánů konkávního tvaru.
Závěr
- Aplikace vyšší dávky u karcinomu prostaty zlepšuje významně výsledky léčby
- s modulovanou intenzitou svazku záření (IMRT) umožní eskalaci dávky v nádoru při maximálním šetření zdravých tkání a kritických orgánů
- Při plánování radioterapie je výhodné využívat nových zobrazovacích metod MRI a PET/CT
- PET a prostorová MRI spektroskopie umožní zobrazit biologicky aktivní oblasti (BTV), které lze pomocí IMRT cíleně ozářit vyšší dávkou
- Perspektivní se jeví kombinace zevní radioterapie s brachyradioterapií v oblasti prostaty.
Datum přednesení příspěvku: 26. 5. 2004
