Konference: 2010 XXXIV. Brněnské onkologické dny a XXIV. Konference pro sestry a laboranty
Kategorie: Radioterapie
Téma: Moderní trendy v radioterapii
Číslo abstraktu: 060
Autoři: Prof. MUDr. Radim Jančálek, Ph.D., MBA; prof. MUDr. Zdeněk Novák, CSc.; MUDr. Jan Chrastina, Ph.D.
Radioterapie je dnes již standardním postupem nejen v léčbě národů CNS vyššího gradingu, ale i lézí nenádorového původu, jako jsou například cévní malformace. Navzdory svému terapeutickému potenciálu může ovšem radioterapie působit jako spouštěcí mechanismus kancerogeneze. Použití léčebné radioterapie tak může s odstupem let zvýšit riziko rozvoje nového nádoru. Koncept radioterapií indukované onkogeneze formuloval Cahan již v roce 1948 (Cahan et al., 1998). Je ovšem nutné zdůraznit, že přínos radioterapie v léčbě nádorových onemocnění vysoce převyšuje riziko indukce nového nádoru. Navíc riziko rozvoje indukovaného nádoru je nejvyšší právě u nejdéle přežívajících onkologicky léčených pacientů, kde byl terapeutický efekt aplikované radioterapie nejlepší.
Individuální riziko radioterapií indukovaného nového nádoru je závislé na několika faktorech: typ a dávka aplikovaného záření, místo a velikost ozářené části těla, přirozená senzitivita tkání na ozáření a věk ozářeného. Publikované práce uvádějí riziko malignizace 1% až 3% po ozáření velkým polem (Breen et al., 1998). Riziko pozdější maligní transformace ozářených tkání se zdá být mnohem menší po stereoradiochirurgickém ozáření (Laws et al., 1999). Převážnou část nitrolebí tvoří nervová tkáň, která je považována za relativně radiorezistentní. Na druhou stranu meningeální tkáň je vysoce citlivá na působení ionizujícího záření a to obzvláště u dětí (Cantini et al., 1989). Většina radioterapií indukovaných nádorů v nitrolebí jsou tak meningiomy, ale byly popsány také gliomy, sarkomy a schwannomy (Dweik et al., 1995; Sznajder et al., 1996).
Hypotéza o efektu ionizujícího záření na nitrolební meningeomy byla formulována Munkem v roce 1969, který pozoroval zvýšený výskyt nitrolebních meningiomů po ozáření skalpu u pacientů léčených pro tinea capitis. Podle dávky aplikované radioterapie lze meningiomy lze rozdělit na 3 skupiny: meningiomy indikované ozáření vysokou dávkou (>20 Gy), střední dávkou (10-20 Gy) a nízkou dávkou (<20 Gy) (Hendee, 1993). Někteří autoři uvádějí již dávku nad 20 Gy jako vysokou (Musa et al.,1995).
Meningeomy indukované ionizujícím zářením se liší od spontánních meningiomů v několika aspektech. Průměrný věk pacientů s diagnostikovaným radiací indukovaným meningiomem je 30-38 let při ozáření vysokou dávkou záření a 45-58 let po ozáření malou dávkou, zatímco spontánní meningeomy se nejčastěji vyskytují v 5. a 6. dekádě věku. Incidence vícečetných meningiomů je zvýšená po ozáření jak s malou tak i vysokou dávkou záření a uvádí se v literatuře od 5 do 19%, kdežto výskyt vícečetných spontánních meningiomů se uvádí kolem 2,5% (Sadetzki et al., 2002). Radiací indikované meningiomy mají také specifické histologické rysy. Nacházíme u nich zvýšenou celularitu, nukleární pleomorfismus, zvýšenou mitotickou aktivitu, fokální nekrózy, invazi do okolní kosti a mozku. Radiací indukované meningiomy vykazují také více agresivní klinické chování než meningiomy spontánní včetně vyšší frekvence recidivy po chirurgické léčbě nebo ozáření. Na rozdíl od frekvence recidivy spontánních meningiomů kolem 11%, uvádí Rubinstein recidivu u téměř 26% pacientů po léčbě indukovaných meningiomů a u 12% z nich dokonce vícečetnou (Rubinstein et al., 1984).
Latence mezi expozicí ionizujícímu záření a klinickou diagnózou meningiomu závisí na dávce záření a věku ozařovaného. V literatuře se uvádí průměrná latence 35 let po ozáření malou dávkou (<10 Gy), 26 let po ozáření středně velkou dávkou (10-20 Gy) a 19 let po ozáření velkou dávkou (>20 Gy) (Harrison et al., 1991). Incidence indukovaných meningiomů po vysoké dávce záření je paradoxně nižší, což souvisí s relativně krátkou dobou přežití u těchto pacientů. Většina indukovaných meningiomů je tedy vyvolána ozářením nízkými dávkami (7-15 Gy) na oblast skalpu a tváře.
Chirurgická léčba meningeomů se jeví jako nejoptimálnější léčebná modalita (D‘Ambrosio et al., 2003), i když kompletní a bezpečná exstirpace nemusí být možná díky agresivnějšímu chování radiací indukovaných meningeomů s jejich invazi do okolních tkání (kosti, cévy, mozek). I přesto, že je původní příčina indukovaných meningiomů vystavení meningeomatózní tkáně účinkům ionizujícího záření, je v literatuře popisována také možnost stereoradiochirurgické terapie. U malých a středně velkých meningiomů bez mass-efektu je účinnost radiochirurgické léčby dokonce udávána jako rovnocenná léčbě chirurgické (Pollock et al., 2003). Stereoradiochirurgie se tak jeví jako metoda volby při progredujících meningiomech v lokalizacích nepříznivých pro chirurgickou léčbu, jako jsou například meningiomy sinus cavernosus (Liscak et al., 1999).
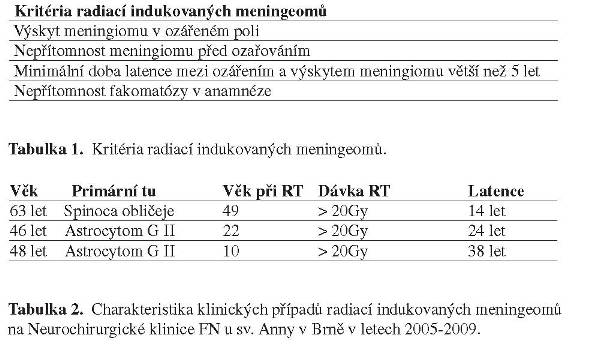
Neurochirurgická klinika FN u sv. Anny v Brně se zabývá mimo jiné také léčbou nitrolebních nádorů v plném rozsahu. Studiem pacientů operovaných za posledních 5 let jsme zjistily 3 případy, které splňovaly kritéria pro možnost zařazení do skupiny radiací indukovaných meningiomů (Tabulka 1). Základní charakteristika těchto případů je uvedena v Tabulace 2. Všechny tyto případy byly řešeny exstirpací meningiomu a v průběhu necelých 5 let po operaci se prozatím neobjevila na kontrolní MR recidiva tumoru.
Závěrem lze říci, že radiací indukované meningiomy tvoří zvláštní skupinu meningiomů, která se svými charakteristikami liší od meningiomů spontánních. Tyto odlišnosti je pak nutné mít na zřeteli při plánování léčby a také pooperačním období, jelikož tito pacienti vyžadují dlouhodobé sledování pro vyšší riziko recidivy.
Literatura
- BREEN, P.; FLICKINGER, J. C.; KONDZIOLKA, D. et al. 1998.
Radiotherapy for nonfunctional pituitary adenoma: analysis of
long-term tumor control. J Neurosurg, 1998, vol. 89, no. 6, p.
933-938.
- CAHAN, W. G.; WOODARD, H. Q.; HIGINBOTHAM, N. L. et al. 1998.
Sarcoma arising in irradiated bone: report of eleven cases. 1948.
Cancer, 1998, vol. 82, no. 1, p. 8-34.
- CANTINI, R.; GIORGETTI, W.; VALLERIANI, A. M. et al. 1989.
Radiation-induced cerebral lesions in childhood. Childs Nerv Syst,
1989, vol. 5, no. 3, p. 135-139.
- DAMBROSIO, A. L.; BRUCE, J. N. 2003. Treatment of meningioma:
an update. Curr Neurol Neurosci Rep, 2003, vol. 3, no. 3, p.
206-214.
- DWEIK, A.; MAHEUT-LOURMIERE, J.; LIORET, E. et al. 1995.
Radiation-induced meningioma. Childs Nerv Syst, 1995, vol. 11, no.
11, p. 661-663.
- HARRISON, M. J.; WOLFE, D. E.; LAU, T. S. et al. 1991.
Radiation-induced meningiomas: experience at the Mount Sinai
Hospital and review of the literature. J Neurosurg, 1991, vol. 75,
no. 4, p. 564-574.
- HENDEE, W. R. 1993. History, current status, and trends of
radiation protection standards. Med Phys, 1993, vol. 20, no. 5, p.
1303-1314.
- LAWS, E. R., JR.; VANCE, M. L. 1999. Radiosurgery for pituitary
tumors and craniopharyngiomas. Neurosurg Clin N Am, 1999, vol. 10,
no. 2, p. 327-336.
- LISCAK, R.; SIMONOVA, G.; VYMAZAL, J. et al. 1999. Gamma knife
radiosurgery of meningiomas in the cavernous sinus region. Acta
Neurochir (Wien), 1999, vol. 141, no. 5, p. 473-480.
- MUSA, B. S.; POPLE, I. K.; CUMMINS, B. H. 1995. Intracranial
meningiomas following irradiation--a growing problem? Br J
Neurosurg, 1995, vol. 9, no. 5, p. 629-637.
- POLLOCK, B. E.; STAFFORD, S. L.; UTTER, A. et al. 2003.
Stereotactic radiosurgery provides equivalent tumor control to
Simpson Grade 1 resection for patients with small- to medium-size
meningiomas. Int J Radiat Oncol Biol Phys, 2003, vol. 55, no. 4, p.
1000-1005.
- RUBINSTEIN, A. B.; SHALIT, M. N.; COHEN, M. L. et al. 1984.
Radiation-induced cerebral meningioma: a recognizable entity. J
Neurosurg, 1984, vol. 61, no. 5, p. 966-971.
- SADETZKI, S.; FLINT-RICHTER, P.; BEN-TAL, T. et al. 2002.
Radiation-induced meningioma: a descriptive study of 253 cases. J
Neurosurg, 2002, vol. 97, no. 5, p. 1078-1082.
- SZNAJDER, L.; ABRAHAMS, C.; PARRY, D. M. et al. 1996. Multiple schwannomas and meningiomas associated with irradiation in childhood. Arch Intern Med, 1996, vol. 156, no. 16, p. 1873-1878.
Datum přednesení příspěvku: 23. 4. 2010
