Konference: 2005 XXIX. Brněnské onkologické dny a XIX. Konference pro sestry a laboranty
Kategorie: Ostatní
Téma: Kolorektální karcinom - Pokroky v diagnostice a léčbě
Číslo abstraktu: 100
Autoři: K. Klocová; H. Koukalová; doc. MUDr. Ilona Kocáková, Ph.D.; prof. MUDr. Marek Svoboda, Ph.D.; Tamara Šmerdová; M. Havlová
Sledování enzymů zapojených do metabolismu 5-fluorouracilu umožnuje optimalizaci terapie fluoropyrimidiny, výběr vhodného preparátu a jeho dávkování. Detekcí exprese a aktivity těchto enzymů před zahájením terapie můžeme určit pacienty, kteří s velkou pravděpodobností na léčbu fluoropyrimidiny nebudou reagovat, nebo se u nich dokonce objeví vážná toxicita. V těchto případech by pak pacient nemusel být vystavován známému riziku toxicity a mohla by pro něj být navržena jiná forma terapie.
Tymidin fosforyláza (TP) je enzym nezbytný při aktivaci kapecitabinu (Xelody), který se využívá při léčbě kolorektálních nádorů. Kapecitabin je perorální fluoropyrimidinový derivát, pro-drug 5-fluorouracilu (5-FU). V játrech je přeměněn karboxylesterázou na 5’-deoxy-5-fluorouridin, ten je cytidin deaminázou konvertován na 5-deoxy-fluorouridin, který je pomocí tymidin fosforylázy přeměněn na 5-FU. Protože TP je v nádorových buňkách exprimována více než v ostatních buňkách, je zde Xeloda metabolizována přednostně. Účinek kapecitabinu by tedy měl být vyšší u pacientů s vyššími hladinami TP.[1]
Cytokin tumor nekrotizující faktor (TNF α) má široké spektrum účinků – od proliferace k zánětlivým účinkům, zprostředkování imunitních reakcí, účast na apoptóze a nekróze. Dále reguluje velké množství signálních procesů a aktivitu transkripčních faktorů, má angiogenní účinky. Předpokládá se i jeho účast při obraně organismu proti růstu nádorových buněk. Indukuje expresi některých genů, mimo jiné i TP.[2, 3]
Sawada a kol. pozorovali na úrovni enzymové aktivity, že po ozáření nádorové tkáně došlo ke zvýšení hladiny TNF α, následovala pozitivní regulace a nárůst aktivity tymidin fosforylázy a zvýšila se tak efektivita terapie kapecitabinem. Ozáření tedy mohlo zvýšit množství TP nepřímo prostřednictvím TNF α. Efektivita léčby byla podle Sawady vyšší u kombinace kapecitabinu s ozářením ve srovnání s jinými způsoby léčby. [4] V jiné studii nebylo zvýšení TNF α po ozáření potvrzeno, i když hladina TP v ozářené nádorové tkáni byla významně zvýšená.[5]
Naším cílem bylo srovnat expresi tymidin fosforylázy a tumor nekrotizujícího faktoru á ve zdravé a nádorové tkáni u pacientů s rektálním karcinomem odebrané před zahájením terapie a dva týdny po zahájení terapie a porovnat hladiny transkriptů s reakcí na léčbu.
Pacienti a metody
Do souboru bylo zařazeno 29 pacientů v pokročilém stádiu rektálního karcinomu, léčených konkomitantní radioterapií (celková dávka 50,4 Gy, frakcionace po 1,8 Gy denně) a chemoterapií Xelodou (dávka 825 mg/m2 denně, rozdělená do dvou dávek). Od každého pacienta byly získány vzorky nádorové tkáně a zdravé sliznice tlustého střeva před zahájením terapie a v období 2 týdnů po zahájení terapie (rozmezí bylo 8 – 14 dní, vzorky od jednoho pacienta byly odebrány až po 25 dnech, důvodem dlouhé prodlevy bylo přerušení radioterapie v období vánoc). Po izolaci RNA a reverzní transkripci byly metodou kvantitativní real-time PCR stanoveny hladiny mRNA tymidin fosforylázy (TP) a tumor nekrotizujícího faktoru α (TNF α). U všech vzorků byla stanovena i hladina referenčního housekeepingového genu pro glyceraldehyd-3-fosfát-dehydrogenázu (GAPDH), výsledky pak představují poměr mezi počtem kopií sledovaného genu (TP nebo TNF α) a referenčního GAPDH.
Pro statistickou analýzu byl použit software Statistica.
Výsledky a diskuze
Stanovené hodnoty (tabulka 1) byly nejdříve otestovány na normalitu pomocí Shapiro-Wilk testu. Hodnoty mají výrazně nenormální rozložení, a tedy pro další výpočty byly použity neparametrické testy. Tabulka č. 2 uvádí základní statistické parametry sledovaného souboru dat.
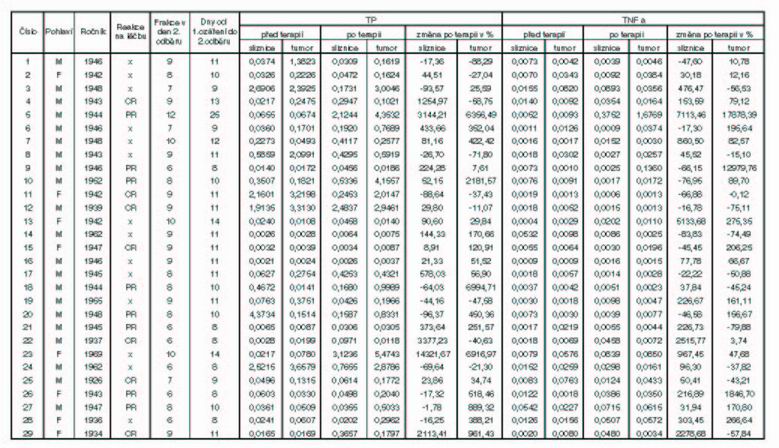
Tabulka 1 Výsledky
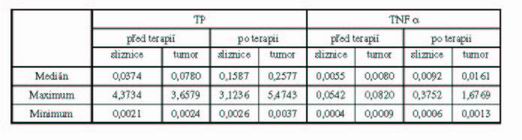
Tabulka 2 Základní statistické parametry
Srovnáním hodnot před terapií a po terapii pomocí Wilcoxonova párového testu jsme zjistili, že statisticky významný je pouze rozdíl hodnot před terapií/po terapii u TNF α ve zdravé sliznici tlustého střeva (p = 0,009). U ostatních skupin nebyl nalezen statisticky významný rozdíl (tab. 3). Otázkou je to, zda je vhodně načasován druhý odběr vzorků – vzorky byly odebírány v rozmezí 8 až 25 dní po zahájení radioterapie. V době druhého odběru vzorků nebyli tedy všichni pacienti ozářeni stejnou dávkou, ta se pohybovala v rozmezí 10,8 Gy – 21,6 Gy. Oguri a kol. při stanovení enzymatické aktivity TP v cervikálním karcinomu zjistili, že hladina TP se v nádorové tkáni nelišila před zahájením ozařování a po aplikaci dávky 10 Gy a 20 Gy, což je v souladu s naším pozorováním.[6] Rozdíl v aktivitě TP před a po ozáření zjištěný Sawadou byl nalezen v nádorových buňkách po jednorázové aplikaci dávky 2,5 nebo 5 Gy. Hladina TNF α byla podle jejich zjištění na maximu o několik dní dříve než hladina TP a poté začala klesat. [4] Blanquicett a kol. sledovali pomocí real-time PCR hladinu mRNA pro TP a TNF α v buňkách glioblastomu po aplikaci jednorázové dávky 8,5 Gy. Zjistili, že hladina TP mRNA vzrostla na maximum čtvrtý den po ozáření, hladina TNF α nebyla signifikantně změněná.[5]
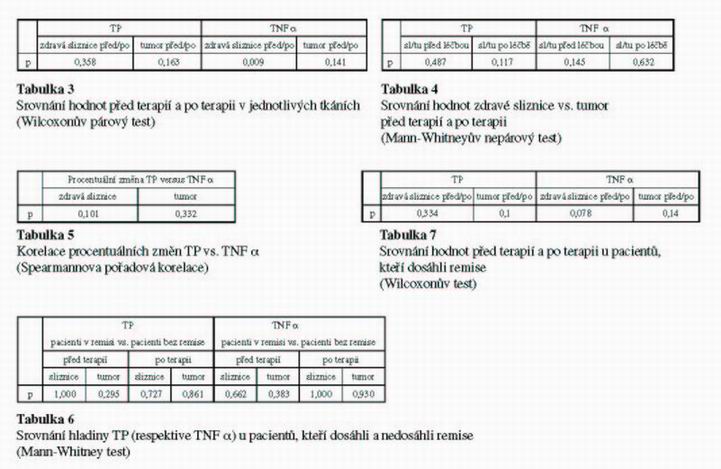
Pomocí Mann-Whitneyova testu bylo zjištěno, že exprese TP se statisticky významně nelišila v nádorové tkáni a ve zdravé sliznici před zahájením léčby (p=0,4869) ani po zahájení terapie (p=0,1168). U TNF α byla situace obdobná (p=0,1447 před léčbou a p=0,6322 po zahájení léčby) (tab. 4). Mediány u TP byly ale vyšší v nádorové tkáni (0,0780) ve srovnání se zdravou sliznicí (0,0374) před zahájením terapie, i po zahájení radioterapie (0,1587 v sliznici a 0,2577 v nádorové tkáni). U TNF α tomu bylo také tak (tab. 2).
Korelaci procentuálních změn hladiny TP s hladinou TNF α jsme stanovili pomocí Spearmannovy pořadové korelace, opět nebyla nalezena statisticky významná korelace mezi procentuální změnou hladiny TP a TNF α (tab. 5). Sawada a kol. pozorovali na úrovni enzymové aktivity zvýšení hladiny TNF α a následně indukované zvýšení aktivity TP po ozáření nádorové tkáně[4]. Naše zjištění by mohlo být vysvětleno už výše zmíněným pozorováním Sawady, který zjistil, že hladina TNF α byla na maximu o několik dní dříve než hladina TP a poté začala klesat. V době odběru vzorků po chemoterapii již tedy mohla zvýšená hladiny TNF α, pokud zvýšení bylo opravdu indukováno ozářením, klesnout a proto jsme nenalezli souvislost mezi hladinou mRNA pro TP a TNF α.
Pacienti byli dále rozděleni do dvou skupin podle toho, zda dosáhli během léčby remise (n=15) nebo nedosáhli (n=14). V tabulce 6 jsou shrnuty výsledky Mann-Whitneyova testování. Rozdíl v hladinách TP (respektive TNF α) u pacientů, kteří dosáhli remise a u pacientů, kteří remise nedosáhli, nebyl statisticky významný. Dále nás zajímalo, zda je u pacientů, kteří dosáhli remise, nějaký rozdíl v hladině TP (TNF α) před a po terapii. Opět nebyl nalezen statisticky významný rozdíl (tab. 7). Někteří pacienti neodpovídající na léčbu kapecitabinem mají oproti předpokladu vysoké hladiny TP mRNA a naopak někteří pacienti odpovídající na léčbu mají nízké hladiny TP. Vysoké hladiny TNF α a následně indukované zvýšení hladiny TP by podle předpokladu mohlo být spojeno s přednostní aktivací Xelody v nádoru a jeho selektivní likvidací. Bohužel situace není tak jednoduchá. Důvodem je mimo jiné skutečnost, že tymidin fosforyláza je zároveň angiogenním faktorem a stimuluje růst nádorových buněk, může také inhibovat indukci apoptózy nádorových buněk, navozenou cytostatiky. Vysoké hladiny proto tedy mohou přispívat k růstu nádoru a dokonce k jeho invazivnosti.[7, 8] TP ve skutečnosti není exprimována jen tumorovými buňkami, ale i tumor infiltrujícími makrofágy TIF, možná aktivita TP v TIF dokonce významně převažuje.[9] Na rezistenci nebo citlivosti vůči kapecitabinu se tedy mohou podílet i jiné než nádorové buňky.
Závěr
I když část pacientů vykazuje výsledky odpovídající předpokladu, že vysoké hladiny TP mRNA souvisí s rezistencí na fluoropyrimidiny, u části pacientů jsou hladiny TP mRNA nízké a přesto nádor dobře reaguje na léčbu kapecitabinem. Naopak u části pacientů byla v nádorové tkáni nalezena vysoká hladina TP mRNA a přesto mají dobrou odpověď na léčbu. Souvislost mezi ozářením a hladinou TNF α a TP mRNA se v našem souboru nepotvrdila, což mohlo být způsobeno nevhodným načasováním druhého odběru vzorků. K rezistenci nebo citlivosti na fluoropyrimidiny přispívají i další enzymy zahrnuté do metabolismu fluoropyrimidinů. Hladiny TP jsou z velké části určovány přítomností tumor infiltrujících mikrofágů, na rezistenci nebo citlivosti vůči fluoropyrimidinům se tedy mohou podílet i jiné než nádorové buňky. To vše naznačuje, že TP není jediným faktorem, který reakci na fluoropyrimidiny ovlivňuje. TP může být prediktivním a prognostickým faktorem, pokud se použije v kombinaci s dalšími markery, které je třeba dále zkoumat.
Literatura
- Ackland S.P., Peters G.J.: Thymidine phosphorylase: its role in
sensitivity and resistence to anticancer drugs. Drug Resist
Updat., 2 (4): 205 – 214, 1999. - Sherman M.L., Datta R., Hallahan D.E., Weichselbaum R.R., Kufe
D.W.: Regulation of tumor necrosis factor gene expression by
ionizing radiation in human myeloid leukemia cells and peripheral
blood monocytes. J. Clin. Invest., 87: 1794 – 1797,
1991.
- Eda H., Fujimoto K., Watanabe S., Ura M., Hino A., Tahala Y.,
Wada K., Ishitsuk H.: Cytokines induce thymidine phosphorylase
expression in tumor cells and make them more susceptible to
5’-deoxy-5-fluorouridine. Cancer Chemother Pharmacol., 32 (5): 333
– 8, 1993.
- Sawada N., Ishikawa T., Sekiguchi F., Tahala Y., Ishitsuka H.:
X-Ray irradiation induces thymidine phosphorylase and enhances the
efficacy of Capecitabine (Xeloda) in human cancer xenografts. Clin.
Cancer Res., 5: 2948 – 2953, 1999.
- Blanquicett C., Gillespie G.Y., Nabors L.B., Miller C.R.,
Bharara S., Buchsbaum D.J., Diasio R.B., Johnson M.R.: Induction of
Thymidine Phosphorylase in Both Irradiated and Shielded,
Contralateral Human U87MG Glioma Xenografts: Implications for Dual
Modality Treatment Using Capecitabine and Irradiation. Mol Cancer
Ther, 1: 1139 – 1145, 2002.
- Oguri H., Maeda N., Yamamoto Y., Kusume T., Fukala T.:
Thymidine phosphorylase expression is preserved after radiotherapy
in patiens with cervical squamous cell carcinoma. Cancer Chemother
Pharmacol, 53: 151 – 154, 2004.
- Sengupta S., Sellers L.A., Matheson H.B., Fan T.P.: Thymidine
phosphorylase induces angiogenesis in vivo and in vitro: an
evaluation of possible mechanisms. Br J Pharmacol. 139 (2): 219 –
31, 2003.
- Ikeda R., Furukawa T., Mitsuo R., Noguchi T., Kitazono M.,
Okumura H., Sumizawa T., Haraguchi M., Che X.F., Uchimiya H.,
Nakajima Y., Ren X.Q., Oiso S., Inoue I., Yamada K., Akiyama S.:
Thymidine phosphorylase inhibits apoptosis induced by cisplatin.
Biochem Biophys Res Commun., 301 (2): 358-63, 2003.
- Zhang J.M., Mizoi T., Shiiba K., Sasaki I., Matsuno S.: Expression of thymidine phosphorylase by macrophages in colorectal cancer tissues. World J Gastroenterol., 10 (4): 545 – 9, 2004.
Datum přednesení příspěvku: 26. 5. 2005
