Konference: 2006 XXX. Brněnské onkologické dny a XX. Konference pro sestry a laboranty
Kategorie: Kolorektální karcinom
Téma: Kolorektální karcinom
Číslo abstraktu: 113p
Autoři: doc. MUDr. Ilona Kocáková, Ph.D.; MUDr. Ivo Kocák, Ph.D.; MUDr. Stanislav Špelda; Doc.MUDr. Igor Penka, CSc.; doc. MUDr. Roman Šefr, Ph.D.; prof. MUDr. Pavel Šlampa, CSc.; prof. MUDr. Rostislav Vyzula, CSc.
Přínos pooperační (adjuvantní) chemoterapie (CHT) a radioterapie (RT) u karcinomu rekta klinického stadia II a III (≥T3), ve smyslu snížení rizika lokálních recidiv, vzdálené diseminace a prodloužení pětiletého přežití je podložen randomizovanými klinickými studiemi. Jako radiosenzitizér je používán 5-fluorouracil (5-FU) v kontinuálním nebo bolusovém podání. Tato léčba je však provázena poměrně vysokou incidencí hematologické a kožní toxicity v porovnání s léčbou předoperační (neoadjuvantní). Výhodou této kombinované léčebné modality je i interakce chemo a radioterapie na různých úrovních heterogenní nádorové populace, čímž se vytváří i předpoklady prevence vzniku rezistentních nádorových buněčných klonů, eliminace případných vzdálených mikrometastáz. Hlavní přínos této modality lze spatřovat ve zvýšení počtu sfinkter šetřících operací regresí nádoru. Z cytotoxických látek zůstává v této indikaci zlatým standardem 5-FU.
Metodika zpracování
Na Klinice komplexní onkologické péče MOÚ byl v roce 2001 vypracován protokol pilotní studie vyhodnocující předoperační RT s radiosenzitizérem kapecitabinem (XELODA®) u pacientů s lokálně pokročilým karcinomem rekta klinického stadia II a III. Cílem studie bylo zjistit frekvenci kompletních histopatologických remisí a podíl sfinkter zachovávajících chirurgických výkonů. Vlastní výsledky byly porovnávány s literárními údaji, kde byl v rámci neoadjuvantní léčby podáván kontinuální 5-FU. Předpokládalo se, že tímto přístupem se nezvýší frekvence lokálních recidiv a nezhorší se celkové přežití nemocných. U léčených pacientů byly hodnoceny vedlejší účinky a toxicita léčby. V průběhu neoadjuvantní léčby byly sledovány změny exprese enzymů TP, DPD, TS ve tkáni primárního nádoru a v makroskopicky nepostižené sliznici rekta. Byla analyzována možná souvislost exprese těchto parametrů s léčebnou odpovědí a prognózou. Podmínkou zařazení do neoadjuvantní léčby byla tato vstupní kritéria: histologicky verifikovaný adenokarcinom rekta, lokálně pokročilé onemocnění – klinické stadium cT3, cT4, event. N+ stanoveno pomocí transrektální sonografie rotační sondou (TRUS), pacienti bez předchozí radioterapie nebo chemoterapie pro karcinom rekta, věk 18-75 let, performance status: 0-2, hematologické a biochemické parametry: neutrofily > 2x109/L, trombocyty > 100x109/L, bilirubin < 1,5 násobek horní hranice normy, transaminasy (AST, ALT) < 2,5 násobek horní hranice normy, kreatinin v séru < 140 umol/L nebo clearence kreatininu > 60 ml/min, předpoklad přežití minimálně 3 měsíce, předpoklad spolupráce pacienta, podpis informovaného souhlasu, nepřítomnost aktivní infekce, nepřítomnost nádorové duplicity v posledních pěti letech, vyloučení těhotenství a kojení, vyloučení městnavé srdeční slabosti, anginy pectoris, infarktu myokardu v posledním roce před zařazením do studie, klinicky závažné arytmie, nekontrolovatelná hypertenze.
• Léčebné schéma chemoradioterapie:
Kapecitabin byl podáván v dávce 825 mg/m2 dvakrát denně, přičemž první dávka 2 hodiny před radioterapií, druhá dávka za 12 hodin po dávce první, kontinuálně po celou dobu radioterapie, 38 dnů. Standardní dávka radioterapie na oblast nádoru a svodných lymfatických uzlin byla 180 cGy denně. V 25 frakcích tak bylo dosaženo celkové dávky na oblast pánve 45,0 Gy, s následujícím boostem ve třech frakcích do celkové dávky 50,4 Gy. Přibližná doba celkové radioterapie byla 5,5 týdne.
• Chirurgická léčba:
Operace s definitivním histopatologickým zpracováním resekátu následovala za 6 týdnů od skončené předoperační léčby. Cílem operace byl kurativní chirurgický výkon s odstraněním veškerého makroskopicky patrného nádoru dostatečně daleko do zdravé tkáně, tedy dosažení R0 podle TNM. Operace se zachováním svěrače – přední resekce rekta (LAR) byla prováděna za předpokladu, že bylo možné dodržet bezpečný resekční okraj kdy minimální vzdálenost resekční linie činila 1 – 2 cm od aborálního makroskopického okraje nádoru. V případě nemožnosti dodržení bezpečného resekčního okraje se prováděla operace bez zachování sfinkteru, abdomino-perienální amputace rekta (operace dle Milese) včetně totální mezorektální excize. Volba mezi přední resekcí rekta a abdominoperineální amputací probíhala individuálně na základě výsledků předoperačních vyšetření, pohovoru s pacientem a peroperačního nálezu. K ověření dostatečného makroskopického resekčního okraje byl resekát ihned po resekci na operačním sále rozstřižen a při makroskopickém postižení byla distální část rekta doresekována. V případě, že byl při histopatologickém vyšetření konstatován postižený resekční okraj, byl postup volen individuálně, s preferencí re-resekce (Milesovy operace).
• Hodnocení toxicity:
K posouzení toxicity uvedené konkomitantní léčby byly u všech nemocných monitorovány týdně vitální funkce, hematologické a biochemické parametry a sledována reakce kůže v ozařovaném poli, dle závažnosti zaznamenané toxicity byla CHT, případně RT přechodně přerušena do úpravy stavu nebo byla redukována dávka kapecitabinu.
Léčebné výsledky
Předmětem analýzy je 76 pacientů léčených na Klinice komplexní onkologické péče MOÚ od října 2001 do prosince 2004. V souboru převažovali muži, kterých bylo 55, medián věku byl 59 let (rozmezí 33-76 let).
- U 74 (97%) nemocných byla po ukončení konkomitantní předoperační léčby indikována resekce reziduálního nádoru.
- U 2 pacientů nebyla operace indikována vzhledem k dosažení kompletní remise onemocnění na základě CT, TRUS a PET vyšetření. Opakované histologické vyšetření mikroexcize z místa původního nádoru neprokázalo neoplazii. U neresekovaných pacientů trvá kompletní remise 41 a 17 měsíců.
- Radikální (R0) resekce byla provedena u 71 (96%) nemocných, u 3 (4%) nemocných byla operace hodnocena jako neradikální (1x lokální excize, ve dvou případech provedené nízké přední resekce rekta byl patologem popsán pozitivní distální resekční okraj (R1), následná amputace rekta byla ze strany pacientů odmítnuta).
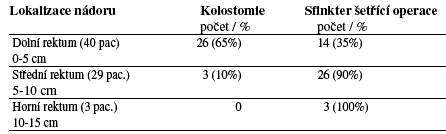
- Sfinkter šetřící operace byla provedena u 43 (60%) nemocných, kolostomie u 29 (40%) pacientů. Zastoupení jednotlivých chirurgických zákroků vzhledem k lokalizaci karcinomu rekta je uvedeno podrobněji v tabulce.
- Patologická kompletní remise (ypCR) byla zaznamenána u 13 (18%) pacientů, mikroskopické reziduum nádoru (ypR1) s průkazem ojedinělé viabilní buňky bylo nalezeno u 10 (14%) pacientů. Celkově bylo neoadjuvantní chemoradioterapií dosaženo kompletní nebo téměř kompletní remise onemocnění u 32% nemocných.
- U 27 (36%) nemocných s patologickým stadiem pT3, pT4, event. pN+ byly podány 4 cykly adjuvantní chemoterapie s kapecitabinem v dávce 2500 mg/m2 denně, po dobu dvou týdnů, interval mezi cykly byl 3 týdny.
- Nejčastějšími nežádoucími účinky léčby byla hematologická a slizniční toxicita 1. a 2. stupně a kožní reakce v ozařovaném poli. Neutropenie 3. stupně se vyskytla jen u 3 (4%) pacientů, trombocytopenie 4. stupně u 1 (1%) pac., anemie 4. stupně u 1 (1%) pacienta, lokální dermatitida 3. stupně u 2 (3%) pacientů, průjem 3. stupně rovněž u 3 (4%) pacientů, radiační dermatitida 3. stupně u 9 (12%) pacientů.
Tab. č 1.
Zastoupení jednotlivých chirurgických zákroků vzhledem k lokalizaci karcinomu rekta
Závěr
Analýza souboru 76 nemocných léčených předoperační RT s kapecitabinem v MOÚ od 10/2001 do 12/2004 nám umožňuje alespoň částečně odpovědět na základní otázky:
- Neoadjuvantní podání kapecitabinu s předoperační RT má
přinejmenším srovnatelnou účinnost jako dosud standardně užívaný
radiosenzitizér 5-FU, při kterém je popisováno 10-30% ypCR. V našem
souboru bylo dosaženo kompletní nebo téměř kompletní patologické
remise onemocnění (ypCR a ypR1) u 32% pacientů a sfinkter šetřící
operace byla možná u 60% nemocných.
- Odpovědět na otázku, zda prognóza nemocných léčených
kapecitabinem nebude horší než při standardním užití 5-FU, tzn.
nezvýší se incidence lokálních recidiv či vzdálených metastáz,
vyžaduje delší čas sledování. V současnosti lze jen konstatovat, že
prognózu nemocných vedle použitého cytostatika ovlivňuje i celá
řada tzv. negativních prognostických znaků. Mezi nejdůležitější z
nich ověřené ve velkých studiích patří vedle pT, pN, gradingu,
invaze do krevních cév také předoperační elevace CEA a zejména
nedostatečná radikalita chirurgického výkonu (pozitivita resekčních
okrajů a reziduum po resekci). Proto i přes výrazný downstaging
nádorů po předoperační chemoradioterapii by měl být stále platným
standardním doporučením radikální chirurgický zákrok s dosažením R0
resekce.
- Vzhledem k selektivní aktivaci zkoušeného přípravku přímo v
nádorové tkáni a nižší koncentraci cytostatické látky v systémovém
řečišti se předpokládal prokazatelně lepší bezpečnostní profil
léčby než při předoperační aplikaci 5-FU, kdy je incidence toxicity
stupně 3 uváděna od 15 % do 25 %. V našem souboru byla kumulativní
hematologická toxicita třetího a čtvrtého stupně stupně přítomná u
6% léčených a nehematologická toxicita G3/4 u 21% léčených
pacientů..
- Tento režim představoval jednoznačně zlepšení kvality života léčených tím, že umožňoval ambulantní léčbu bez nutnosti zavádění centrálního žilního katetru se všemi potenciálními komplikacemi, které se vyskytují až u 40% pacientů léčených kontinuálním 5-FU (infekce, krvácení, trombóza, pneumothorax).
Literatura
- Gastrointestinal Tumor Study Group. Survival after
postoperative combination treatment of rectal cancer. N Engl J Med
315:1294-1295, 1986.
- Tepper JE, O’Connell MJ, Petroni GR, et al. Adjuvant
postoperative fluorouracil-modulated chemotherapy combined with
pelvic radiation therapy for rectal cancer: initial results of
Intergroup 0114. J Clin Oncol 997;15:2030.
- O’Connell MJ, Martenson JA, Weiand HS, et al. Improving
adjuvant therapy for rectal cancer by combining protracted infusion
fluorouracil with radiation therapy after curative surgery. N Engl
J Med 1994;331:502.
- Wolmark N, Wieand HS, Hyams DM, et al.: Randomized trial of
postoperative adjuvant chemotherapy with or without radiotherapy
for carcinoma of the rectum: NSABP protocol R-02. Journal of the
National Cancer Institute 92(5): 388-396, 2000.
- Minsky BD, Cohen AM, Enker WE, et al. Combined modality therapy
of rectal cancer: Decreased acute toxicity with the preoperative
approach. J Clin Oncol 1992;10:1218-1224.
- Hyams DM, Mamounas EP, Petrelli N, et al. A clinical trial to
evaluate the worth of preoperative multimodality therapy in
patients with operable carcinoma of the rectum. A progress report
of the National Surgical Adjuvant Breast and Bowel Project protocol
R0-3. Dis Colon Rectum 1997;40:131-139
- Chen ET, Mohiuddin M, Brodovsky H. Ishikawa T, Sawada N,
Sekiguchi F, et al. Xeloda (capecitabine), a new oral
fluoropyrimidine carbamate with an improved efficacy profile ;over
other fluoropyrimidines. Proc Am Soc Clin Oncol
1997A79:6(abst).
- Ishikawa T, Utoh M, Sawada N et al. Tumor selective delivery of
5-fluorouracil by capecitabine, a new oral fluoropyrimidine
carbamate, in human cancer xenografts. Biochem Pharmacol
1998;55:1091.
- Schüller J, Cassidy J, Dumont E, et al. Preferential activation
of capecitabine in tumor following oral administration in
colorectal cancer patients. Cancer Chemother
- Chen T et al., Downstaging of advanced rectal cancer following
combined preoperative chemotherapy and high dose radiation. Int J
Radiat Oncol Biol Phys 30:169-175, 1994.
- Sawada N et al. (1999) X-ray irradiation induces thymidine phosphorylase and enhances the efficacy of capecitabine (Xeloda) in human cancer xenografts. Clinical Cancer Research Vol 5, 2948-2953
Datum přednesení příspěvku: 11. 5. 2006
