Konference: 2006 XXX. Brněnské onkologické dny a XX. Konference pro sestry a laboranty
Kategorie: Gastrointestinální nádory
Téma: Nádory trávícího traktu
Číslo abstraktu: 123p
Autoři: doc. MUDr. Ilona Kocáková, Ph.D.; MUDr. Stanislav Špelda; MUDr. Ivo Kocák, Ph.D.; MUDr. Jan Možný; doc. MUDr. Zdeněk Řehák, Ph.D.; MUDr. Miloš Pacal; prof. MUDr. Rostislav Vyzula, CSc.
Ačkoliv jsou gastrointestinální stromální nádory (GIST) nejčastějšími sarkomy trávicího ústrojí, z celkového počtu sarkomů představují přibližně jen 5%. Roční incidence se odhaduje na 10-20 případů na 106 obyvatel. GIST bývají diagnostikovány v různě pokročilých stadiích s odlišnými biologickými vlastnostmi: od malých indolentních nádorů, které jsou léčitelné pouhou excizí až po nádory maligní povahy, které představují 20-30%. GIST jsou nejčastěji lokalizovány v žaludku (40-70%) a tenkém střevě (20-40%), vzácně v mezenteriu a omentu. Nejčastějšími místy metastáz jsou játra a peritoneum. Histopatologicky jsou definovány jako vřetenobuněčné nebo epiteloidní, vyjímečně pleiomofní mezenchymální nádory. Nádory exprimující protein KIT, transmembránově uložený receptor pro cytokin, známý jako růstový faktor pro kmenové buňky s intracytoplasmatickou tyrosinkinázovou aktivitou. Tento protein má významnou úlohu v hemopoeze, melaninogenezi, gametogenezi a ve vývoji intersticiálních Cajalových buněk. Přibližně 5% nádorů má mutaci PDGF-R, ale časté jsou i jiné imunofenotypické a cytogenetické rysy. Chirurgický výkon patří mezi standardní postup v léčbě nemetastatického onemocnění a radikální resekce nádoru s negativními resekčními okraji představuje nejdůležitější prognostický faktor. Pětileté přežití se pohybuje kolem 50%. Mezi další prognostické faktory patří: velikost nádoru (prognóza se zhoršuje u nádorů 5 cm), ruptura tumoru při operaci s krvácením do peritoneální dutiny a velikost reziduálního onemocnění, vysoký mitotický index a absence mutace KIT genu. GIST se řadí mezi radiorezistentní a chemorezistentní nádory, procento léčebných odpovědí na konvenční cytostatika (RR) nepřesahuje 10%. Příčinou může být i častá exprese P-glykoproteinu. Pro stanovení rozsahu nemoci se vedle klasických metod (rentgenové vyšetření s dvojím kontrastem, endoskopické a endosonografické vyšetření) uplatňuje pro diagnózu metastáz počítačová tomografie (CT), nukleární magnetická rezonance (MR) a pozitronová emisní tomografie (PET).
Glivec (Imatinib mesylát) je kompetitivní inhibitor určitých tyrozinkináz včetně KIT a receptorů pro destičkový růstový faktor. Preparát vykázal ve studii provedené v USA a ve Finsku (CSTI571 B2222 protokol) vysoké procento léčebných odpovědí u c-KIT pozitivních metastatických nebo inoperabilních GIST.
Metodika zpracování
Od zaři 2003 bylo v MOÚ konzultováno 46 pacientů s histologicky verifikovaným GIST. Pozitivita c-kit byla prokázána u 42pacientů. Třiceti sedmi pacientům s metastatickým nebo lokálně pokročilým, inoperabilním onemocnění s pozitivitou c-KIT byla zahájena léčba imatinib mesylátem. Efekt léčby byl hodnocen pomoci CT a PET. Vyšetření byla provedena před zahájením léčby imatinib mesylatem a nasledně se opakovala ve 2 měsíčních intervalech. Kontrolní vyšetření PET bylo opakovaně provedeno u 25 pacientů. Denní dávka imatinib mesylátu byla 400 – 600 mg.
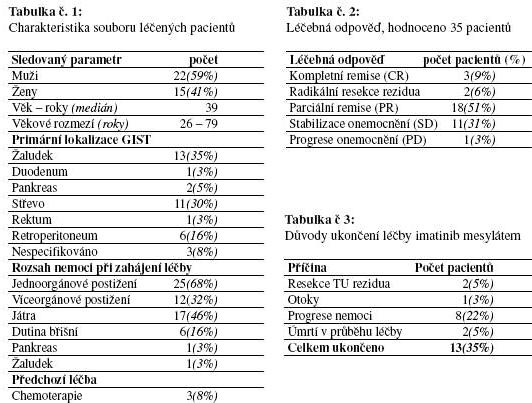
Charakteristika souboru
Podrobný rozbor 37 léčených nemocných je uvedená v tabulce č. 1. Léčebná odpověď byla dosud vyhodnocena u 35 (95%) pacientů. Výsledky léčby shrnuje tabulka č.2. V 1 případě byla CR verifikována histologicky, když v resekovaném reziduu nebyly prokázány maligní buňky. U 2 (6%) pacientů byla dosažena výrazná parciální remise původně inoperabilního tumoru. Následné reziduum bylo radikálně resekováno. Léčba byla dosud ukončena u 13 (35%) pacientů, 24 (65%) pacientů v léčbě pokračuje. Důvody ukončení léčby shrnuje tabulka č. 3.
Relaps onemocnění
Relaps onemocnění dosud nastal u 8 (23%) pacientů. Medián času do progrese od zahájení léčby je 9 měsíců (min. 0,5 měs., max. 27 měs.). Celkové přežití nelze statisticky hodnotit. K úmrtí v průběhu léčby došlo u 2 (5%) pacientek za 5 a 20 měsíců po zahájení léčby imatinib mesylátem. V 1 případě došlo k úmrtí v důsledku progrese GIST, u 2. pacientky není příčina úmrtí známá. Pět pacientů po ukončení léčby pro progresi nebo nežádoucí účinky bylo dále léčeno symptomaticky mimo MOÚ a není známo zdali žijí nebo zemřeli.
Nežádoucí účinky
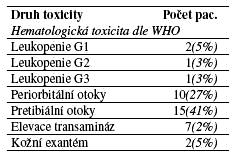
Toxicita léčby dle WHO byla mírná. Pro otoky byla léčba ukončena u 1 (3%) pacienta. U všech ostatních pacientů nebyly vedlejší účinky důvodem k přerušení léčby. Nejčastějším vedlejším účinkem byly periorbitální a pretibiální otoky, které se objevily celkem u 25 (68%) pacientů. Z důvodu elevace transamináz a vzniku kožního exantému byla dávka imatinib mesylátu redukována u 3 (8%) pacientů. Toxicitu léčby shrnuje tabulka č. 4.
Tabulka č. 4:
Toxicita léčby imatinib mesylátem
Závěr
Imatinib mesylát je na molekulární úrovní první cílenou kauzální látkou, která je vysoce efektivní v léčbě GIST. Tato léčba se u indikovaných pacientů jeví jako účinná a dobře tolerovaná.
Datum přednesení příspěvku: 11. 5. 2006
